1 . 根据所学化学知识回答下列问题:
(1)基态铁原子的价电子排布式为_______ 。基态硫原子的最外层电子排布的轨道表示式 为_______ 。
(2) 可以与
可以与 形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验
形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验 的存在,KSCN中四种元素的电负性最大的是
的存在,KSCN中四种元素的电负性最大的是_______ (用元素符号表示)。
(3) 中S的价层电子对数为
中S的价层电子对数为_______ , 的键角
的键角_______  的键角(填“>”、“<”或“=”)。
的键角(填“>”、“<”或“=”)。
(4)单质铜及镍都是由_______ 键形成的晶体;某镍铜合金的立方晶胞结构如下图所示。

晶胞中铜原子与镍原子的个数比为_______ 。
(5)SiC的晶体结构与晶体硅类似。SiC的晶体类型为_______ ,晶体中Si原子与Si-C键的数目之比为_______ 。
(1)基态铁原子的价电子排布式为
(2)
 可以与
可以与 形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验
形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验 的存在,KSCN中四种元素的电负性最大的是
的存在,KSCN中四种元素的电负性最大的是(3)
 中S的价层电子对数为
中S的价层电子对数为 的键角
的键角 的键角(填“>”、“<”或“=”)。
的键角(填“>”、“<”或“=”)。(4)单质铜及镍都是由

晶胞中铜原子与镍原子的个数比为
(5)SiC的晶体结构与晶体硅类似。SiC的晶体类型为
您最近一年使用:0次
名校
解题方法
2 . 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外有7个电子,基态Y原子无未成对电子,Z与X为同族元素,W最高价含氧酸为二元酸,下列说法正确的是
A.原子半径: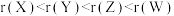 |
| B.元素Y、W的简单离子具有相同的电子层结构 |
| C.Z的最高价氧化物对应水化物的酸性比X的强 |
| D.电负性大小:Y<Z<W |
您最近一年使用:0次
2022-03-03更新
|
347次组卷
|
3卷引用:天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题
名校
3 . 下列说法不正确的是
| A.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道 |
B.s-s 键与s-p 键与s-p 键的电子云形状的对称性相同 键的电子云形状的对称性相同 |
| C.电负性大于1.8的为非金属,小于1.8的为金属 |
| D.共价键是原子间通过共用电子对所形成的相互作用 |
您最近一年使用:0次
4 . 下列各项叙述中,正确的是
| A.N、P、As的电负性随原子序数的增大而增大 |
| B.价电子排布为3d54s2的元素位于第四周期VA族,是p区元素 |
| C.2p和3p轨道形状均为哑铃形,能量也相等 |
D.氮原子的最外层电子排布图: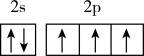 |
您最近一年使用:0次
2022-02-28更新
|
156次组卷
|
2卷引用:天津市第九十五中益中学校2021-2022学年高三上学期第二次月考化学试题
名校
5 . R、X、Y、Z、W为原子序数依次增大的短周期主族元素,且Y、Z位于同主族。由R、X、Y、Z组成的有机物M是日用化妆品冷烫精的主要原料,其结构如图所示。下列说法正确的是


| A.电负性:Y>Z>R>X |
| B.XZ2、XW4、XR4都是非极性分子 |
| C.简单离子结合质子能力:W>Z |
| D.1molM含7molσ键 |
您最近一年使用:0次
2022-02-20更新
|
516次组卷
|
3卷引用:天津市第一中学2021-2022学年高三下学期4月月考化学试题
解题方法
6 . 短周期主族元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数之和为18,X、Z基态原子的p轨道上均有2个未成对电子,W与X位于同一主族。下列说法正确的是
| A.WX2分子为极性分子 |
| B.元素电负性:Z>W |
| C.原子半径:r(W)>r(Z)>r(Y) |
| D.最高价氧化物水化物的酸性:Z>W |
您最近一年使用:0次
2022-01-22更新
|
551次组卷
|
3卷引用:天津市和平区2022届高三一模化学试题
天津市和平区2022届高三一模化学试题江苏省苏北四市(徐州、淮安、宿迁、连云港)2021-2022学年高三上学期期末调研考试化学试题(已下线)押江苏卷第5题 物质结构与元素周期律 -备战2022年高考化学临考题号押题(江苏卷)
7 . 根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是___________ ,占据该能层电子的电子云轮廓图形状为___________ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:___________ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是___________ 。
(4)已知铁是26号元素,写出Fe的价层电子排布式___________ ;在元素周期表中,该元素在_____________ 填“s”“p”“d”“f”或“ds”)区。
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为___________ 。电负性的顺序是___________ 。
(6)写出C的核外电子排布图为:___________ 。
(7)Zn2+的核外电子排布式为___________ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布式为4s24p4,该元素的名称是
(4)已知铁是26号元素,写出Fe的价层电子排布式
(5)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(6)写出C的核外电子排布图为:
(7)Zn2+的核外电子排布式为
您最近一年使用:0次
2022-01-19更新
|
654次组卷
|
8卷引用:天津市红桥区2021-2022学年高二上学期期末考试化学试题
名校
8 . 下列说法正确的是
| A.电负性:Se>As | B.离子半径:Na+>Cl− |
| C.第一电离能:Al>Mg | D.键长:Cl−Cl>Br−Br |
您最近一年使用:0次
2022-01-07更新
|
488次组卷
|
6卷引用:天津市南开区2021-2022学年高三上学期期末考试化学试卷
名校
9 . 下列说法正确的是
| A.2px、2py、2pz轨道相互垂直,能量不等 |
| B.元素周期表各周期总是从ns能级开始,以np能级结束 |
| C.电负性越大,元素的非金属性越强,第一电离能也越大 |
| D.d区、ds区全部是金属元素 |
您最近一年使用:0次
2021-12-10更新
|
444次组卷
|
2卷引用:天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题
名校
10 . 如图为长式周期表的一部分,其中的编号代表对应的元素。
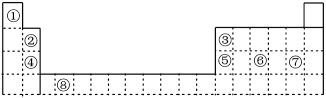
请回答下列问题:
(1)表中属于d区元素的是___ (填元素符号)。
(2)⑧的基态原子最高能层的电子占据能级的电子云轮廓图为___ 。
(3)下列③原子电子排布图表示的状态中,能量最高的为___ (填选项字母)。
(4)元素④的第一电离能___ 元素⑤(选填“>”、“=”或“<”)的第一电离能;元素⑥的电负性___ 元素⑦(选填“>”、“ = ”或“<”)的电负性。
(5)⑥和⑦的最高价氧化物对应的水化物酸性强弱比较___ >___ (填分子式)。
(6)某些不同族元素的性质也有一定的相似性,如表中元素②与元素⑤的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的化学方程式___ 。
(7)铟(In)与③同主族,InF3和InI3的熔点分别是1170℃和210℃,熔点差异的原因是___ 。

请回答下列问题:
(1)表中属于d区元素的是
(2)⑧的基态原子最高能层的电子占据能级的电子云轮廓图为
(3)下列③原子电子排布图表示的状态中,能量最高的为
A.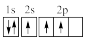 | B.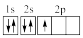 | C. | D.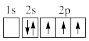 |
(5)⑥和⑦的最高价氧化物对应的水化物酸性强弱比较
(6)某些不同族元素的性质也有一定的相似性,如表中元素②与元素⑤的氢氧化物有相似的性质。写出元素②的氢氧化物与NaOH溶液反应的化学方程式
(7)铟(In)与③同主族,InF3和InI3的熔点分别是1170℃和210℃,熔点差异的原因是
您最近一年使用:0次



