名校
解题方法
1 . X、Y、Z、W为原子序数依次增大的前两周期元素,基态Y原子的s能级电子数是p能级的2倍,基态W原子有两个未成对电子,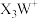 是10电子微粒,可形成离子液体
是10电子微粒,可形成离子液体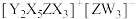 。下列说法正确的是
。下列说法正确的是
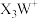 是10电子微粒,可形成离子液体
是10电子微粒,可形成离子液体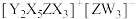 。下列说法正确的是
。下列说法正确的是A.电负性: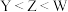 |
B.简单气态氢化物稳定性: |
C.键能: |
D. 中所有原子最外层均满足8电子结构 中所有原子最外层均满足8电子结构 |
您最近半年使用:0次
名校
解题方法
2 . 已知P4单质的结构如下,P4在KOH溶液中的变化是:P4+3KOH+3H2O=3KH2PO2+PH3下列说法正确的是
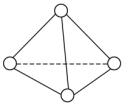
| A.31gP4含有1.5NA个P−P键 | B.产物PH3分子中所有的原子可能共平面 |
| C.P4中P原子为sp2杂化 | D.相关元素的电负性大小顺序:P>O>H>K |
您最近半年使用:0次
名校
3 . 元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。下列判断正确的是
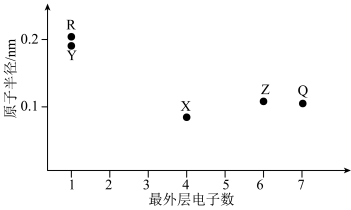

| A.X的电负性比Q的大 |
| B.R和Q形成的化合物固态时为分子晶体 |
| C.Z的简单离子半径比R的大 |
| D.Z的简单气态氢化物的热稳定性比Q的强 |
您最近半年使用:0次
解题方法
4 . 氧和硫是元素周期表中第ⅥA族元素。下列说法正确的是
| A.电负性:O<S | B.沸点: |
C. 是极性分子 是极性分子 | D. 空间构型为平面三角形 空间构型为平面三角形 |
您最近半年使用:0次
名校
解题方法
5 . 已知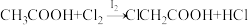 ,
, 的酸性比
的酸性比 强。下列有关说法正确的是
强。下列有关说法正确的是
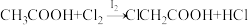 ,
, 的酸性比
的酸性比 强。下列有关说法正确的是
强。下列有关说法正确的是A.HCl的电子式为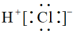 | B.Cl-Cl键的键长比I-I键长 |
C. 分子中只有σ键 分子中只有σ键 | D. 的酸性比 的酸性比 强 强 |
您最近半年使用:0次
2024-04-05更新
|
175次组卷
|
2卷引用:天津市第四十七中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
6 . 钛被誉为太空金属和亲生物金属,拥有卓越的金属特性。它在特定温度下能与多种物质发生反应,在生产和日常生活中都能找到它的踪影。
(1)Ti元素在周期表中的位置是______ ,基态Ti原子的价电子占据原子轨道数目是______ 。
(2) 熔点是
熔点是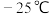 ,沸点136.4℃,可溶于苯或
,沸点136.4℃,可溶于苯或 ,该晶体属于
,该晶体属于______ 晶体; 的制备是以单质Ti和
的制备是以单质Ti和 通过化合反应制得,已知,每转移0.2mol电子放出40.2kJ热量(恢复至室温),请写出该反应的热化学方程式
通过化合反应制得,已知,每转移0.2mol电子放出40.2kJ热量(恢复至室温),请写出该反应的热化学方程式______ ;以 为原料制备
为原料制备 的原理为
的原理为______ (用化学方程式表示)。
(3)已知TiC在碳化物中硬度最大,工业上一般在真空和高温 条件下用C还原
条件下用C还原 制取
制取 。该反应中涉及的元素按电负性由大到小的顺序排列为
。该反应中涉及的元素按电负性由大到小的顺序排列为______ 。
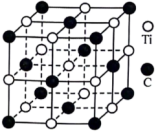
(4)利用钛粉和碳粉反应可生成碳化钛,它在刀具制造领域有重要应用。在该晶体中Ti原子周围紧邻的Ti原子数目为______ 个;设 为阿伏加德罗常数的值,若晶胞边长为
为阿伏加德罗常数的值,若晶胞边长为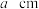 ,则晶体的密度为
,则晶体的密度为______  。(写出表达式)
。(写出表达式)

(1)Ti元素在周期表中的位置是
(2)
 熔点是
熔点是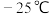 ,沸点136.4℃,可溶于苯或
,沸点136.4℃,可溶于苯或 ,该晶体属于
,该晶体属于 的制备是以单质Ti和
的制备是以单质Ti和 通过化合反应制得,已知,每转移0.2mol电子放出40.2kJ热量(恢复至室温),请写出该反应的热化学方程式
通过化合反应制得,已知,每转移0.2mol电子放出40.2kJ热量(恢复至室温),请写出该反应的热化学方程式 为原料制备
为原料制备 的原理为
的原理为(3)已知TiC在碳化物中硬度最大,工业上一般在真空和高温
 条件下用C还原
条件下用C还原 制取
制取 。该反应中涉及的元素按电负性由大到小的顺序排列为
。该反应中涉及的元素按电负性由大到小的顺序排列为(4)利用钛粉和碳粉反应可生成碳化钛,它在刀具制造领域有重要应用。在该晶体中Ti原子周围紧邻的Ti原子数目为
 为阿伏加德罗常数的值,若晶胞边长为
为阿伏加德罗常数的值,若晶胞边长为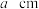 ,则晶体的密度为
,则晶体的密度为 。(写出表达式)
。(写出表达式)
您最近半年使用:0次
解题方法
7 . 氢、氮、硫、氯、铜是元素周期表中前四周期元素。回答下列问题:
(1)氮在元素周期表中的位置_____ 。写出 的电子式
的电子式_____ , 的分子空间构型为
的分子空间构型为_____ , 中心原子的杂化方式为
中心原子的杂化方式为_____ 。
(2)氯与硫相比,非金属性较强的是_____ (用元素符号表示),下列事实能证明这一结论的是_____ (填序号)。
a.常温下氯的单质呈气态,硫的单质呈固态 b.稳定性
c.酸性: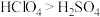 d.氯的电负性大于硫的电负性
d.氯的电负性大于硫的电负性
(3)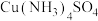 组成元素中,第一电离能最大的元素是
组成元素中,第一电离能最大的元素是_____ (用元素符号表示); 中含有
中含有 键数目为
键数目为_____ 。
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为_____ ;设晶胞边长为 ,该晶体的密度为
,该晶体的密度为_____  (用含a和
(用含a和 的式子表示)。
的式子表示)。
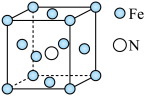
(1)氮在元素周期表中的位置
 的电子式
的电子式 的分子空间构型为
的分子空间构型为 中心原子的杂化方式为
中心原子的杂化方式为(2)氯与硫相比,非金属性较强的是
a.常温下氯的单质呈气态,硫的单质呈固态 b.稳定性

c.酸性:
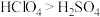 d.氯的电负性大于硫的电负性
d.氯的电负性大于硫的电负性(3)
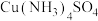 组成元素中,第一电离能最大的元素是
组成元素中,第一电离能最大的元素是 中含有
中含有 键数目为
键数目为(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图所示,则氮化铁的化学式为
 ,该晶体的密度为
,该晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。
您最近半年使用:0次
解题方法
8 . 下列说法或解释错误的是
| A.C、N、O的电负性逐渐增大,其最简单氢化物分子中键角逐渐减小 |
B.可燃冰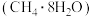 中甲烷分子与水分子间不会形成氢键 中甲烷分子与水分子间不会形成氢键 |
C.漂白粉溶液在空气中失效: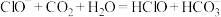 |
D.铜片在 和稀硫酸混合液中溶解: 和稀硫酸混合液中溶解: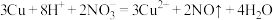 |
您最近半年使用:0次
名校
解题方法
9 . W、X、Y、Z、M、N六种元素的原子序数依次递增,其中W、X、Y、Z为短周期元素,六种元素的元素性质或原子结构特征如下表,回答下列问题。
(1)写出元素Z元素周期表中的位置___________ 。
(2)W、X、Y三种元素的电负性数值由大到小的顺序为___________ (用元素符号作答,下同),这三种元素的第一电离能由大到小的顺序为___________ 。
(3)写出元素M的价层电子排布式___________ 。
(4)写出元素N的N3+最外层电子排布式___________ 。
| 元素 | 元素性质或原子结构特征 |
| W | 原子p轨道的电子数为2 |
| X | 原子中最高能级的不同轨道都有电子,且自旋方向相同 |
| Y | 最外能层电子数是最内能层电子数的3倍 |
| Z | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都高于同周期相邻元素 |
| M | 第24号元素 |
| N | 一种常见的金属元素,正三价离子遇硫氰化钾显红色 |
(2)W、X、Y三种元素的电负性数值由大到小的顺序为
(3)写出元素M的价层电子排布式
(4)写出元素N的N3+最外层电子排布式
您最近半年使用:0次
2024-02-22更新
|
102次组卷
|
2卷引用:天津市耀华中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
10 . 氮硼烷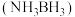 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
(1)基态N原子中电子占据最高能级的电子云轮廓图为_____ 形,基态N原子的电子排布式为_____ 。
(2)B的第一电离能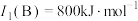 ,判断
,判断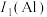
_____  (填“
(填“ ”或“
”或“ ”)。
”)。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:
。在H、B、N三种元素中:
①电负性由大到小的顺序是_____ 。
②原子半径由大到小的顺序是_____ 。
③在元素周期表中的分区与其他两种不同的元素是_____ 。
(4) 、
、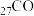 、
、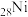 、
、 是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
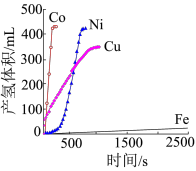
①催化效果最好的金属基态原子中未成对的电子数为_____ 。
②催化效果最差的金属基态原子的价层电子排布式为_____ 。
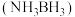 含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:(1)基态N原子中电子占据最高能级的电子云轮廓图为
(2)B的第一电离能
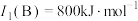 ,判断
,判断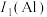
 (填“
(填“ ”或“
”或“ ”)。
”)。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。在H、B、N三种元素中:
。在H、B、N三种元素中:①电负性由大到小的顺序是
②原子半径由大到小的顺序是
③在元素周期表中的分区与其他两种不同的元素是
(4)
 、
、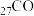 、
、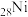 、
、 是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
是目前氨硼烷水解产氢催化剂研究的热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。这四种催化剂中:
①催化效果最好的金属基态原子中未成对的电子数为
②催化效果最差的金属基态原子的价层电子排布式为
您最近半年使用:0次



