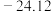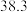1 . 下列关于元素或物质性质的比较中,不正确 的是
A.稳定性: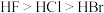 | B.第一电离能: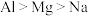 |
C.酸性: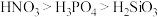 | D.电负性: |
您最近半年使用:0次
名校
2 . 下列对事实的分析正确的是
| 选项 | 事实 | 分析 |
| A | 键角: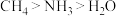 | 电负性:C<N<O |
| B | 第一电离能:P>S | 原子半径:P>S |
| C | 沸点:CO> | CO为极性分子, 为非极性分子 为非极性分子 |
| D | 热稳定性:HF>HCl | HF中存在氢键,HCl中不存在氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
3 . 硼及其化合物在科研、工业等方面有许多用途。
(1)基态B原子价层电子排布式是___________ 。
(2)六方氮化硼晶体也被称为“白石墨”,具有和石墨晶体相似的层状结构,如图所示。___________ 。
②分析六方氮化硼晶体层间是否存在化学键并说明依据:___________ 。
(3)氮化硼量子点(粒径大小为2~10nm)可用于检测金属离子,如Fe2+或Fe3+的检测原理如下图。___________ 。
②n=___________ (填数字)。
(4)NaBH4是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图所示。___________ 。
②已知阿伏加德罗常数为NA,该晶体的密度为___________ g·cm-3。(1nm=10-7cm)
(1)基态B原子价层电子排布式是
(2)六方氮化硼晶体也被称为“白石墨”,具有和石墨晶体相似的层状结构,如图所示。

②分析六方氮化硼晶体层间是否存在化学键并说明依据:
(3)氮化硼量子点(粒径大小为2~10nm)可用于检测金属离子,如Fe2+或Fe3+的检测原理如下图。

②n=
(4)NaBH4是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图所示。

②已知阿伏加德罗常数为NA,该晶体的密度为
您最近半年使用:0次
名校
解题方法
4 . 卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。下列判断不正确的是
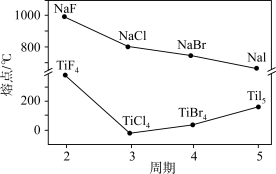
| A.NaX随X-半径增大,离子键减弱 |
| B.四氯化钛中存在共价键和分子间作用力 |
| C.TiF4的熔点反常升高是由于氢键的作用 |
| D.由图可看出F的电负性强于Cl、Br、I |
您最近半年使用:0次
名校
解题方法
5 . 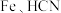 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: ,下列说法正确的是
,下列说法正确的是
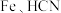 与
与 在一定条件下发生如下反应:
在一定条件下发生如下反应: ,下列说法正确的是
,下列说法正确的是A.此化学方程式中涉及的第二周期元素的电负性大小的顺序为 |
B.配合物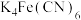 中心离子的配位数是10 中心离子的配位数是10 |
C.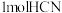 分子中含有 分子中含有 键的数目为 键的数目为 |
D. 中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 中阴离子的空间构型为三角锥形,其中碳原子的价层电子对数为4 |
您最近半年使用:0次
名校
解题方法
6 . 合成氨是人类科学技术发展史上的一项重大成就,在很大程度上解决了地球上因粮食不足而导致的饥饿问题,是化学和技术对社会发展与进步的巨大贡献。
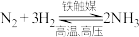
(1)基态氢原子中,核外电子的电子云轮廓图形状为___________ 。
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为___________ 。 分子的电子式为
分子的电子式为___________ 。
② 分子中,与
分子中,与 原子相连的
原子相连的 显正电性。则电负性:
显正电性。则电负性:
___________  。(填“>”或“<”)。
。(填“>”或“<”)。 分子的VSEPR模型的名称为
分子的VSEPR模型的名称为___________ ,其分子的空间结构为___________ 。
(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。
①上述氧化物所涉及的元素中,处于元素周期表中 区的元素是
区的元素是___________ 。
②比较第一电离能的大小:
___________  (填“>”或“<”)。
(填“>”或“<”)。
③下表的数据从上到下是三种金属元素逐级失去电子的电离能。
(a)请解释:为什么原子的逐级电离能越来越大:___________ 。
(b)元素B的常见化合价为:___________ 。
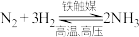
(1)基态氢原子中,核外电子的电子云轮廓图形状为
(2)自然界中的氮元素主要以分子的形式存在于空气中,是人工固氮的主要来源。
①基态氮原子的轨道表示式为
 分子的电子式为
分子的电子式为②
 分子中,与
分子中,与 原子相连的
原子相连的 显正电性。则电负性:
显正电性。则电负性:
 。(填“>”或“<”)。
。(填“>”或“<”)。 分子的VSEPR模型的名称为
分子的VSEPR模型的名称为(3)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有
 、
、 、
、 、
、 、
、 等氧化物中的几种。
等氧化物中的几种。①上述氧化物所涉及的元素中,处于元素周期表中
 区的元素是
区的元素是②比较第一电离能的大小:

 (填“>”或“<”)。
(填“>”或“<”)。③下表的数据从上到下是三种金属元素逐级失去电子的电离能。
| 元素 | A | B | C |
电离能 | 496 | 738 | 578 |
| 4562 | 1451 | 1817 | |
| 6912 | 7733 | 2745 | |
| 9543 | 10540 | 11575 |
(b)元素B的常见化合价为:
您最近半年使用:0次
名校
7 . 下列关于同主族元素 、
、 及其化合物的性质比较和原因分析不正确的是
及其化合物的性质比较和原因分析不正确的是
 、
、 及其化合物的性质比较和原因分析不正确的是
及其化合物的性质比较和原因分析不正确的是| 选项 | 性质比较 | 原因分析 |
| A | 熔点: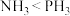 | 摩尔质量: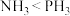 |
| B | 电负性: | 原子半径: |
| C | 酸性: | 非金属性: |
| D | 热稳定性: | 键能: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 硅是电子工业的重要材料。利用石英砂(主要成分为 )和镁粉模拟工业制硅的流程示意图如下。
)和镁粉模拟工业制硅的流程示意图如下。
已知:电负性:
 )和镁粉模拟工业制硅的流程示意图如下。
)和镁粉模拟工业制硅的流程示意图如下。已知:电负性:


| A.I中引燃时用镁条,利用了镁条燃烧放出大量的热 |
B.Ⅱ中主要反应有: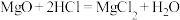 、 、 |
C.为防止 自燃,Ⅱ需隔绝空气 自燃,Ⅱ需隔绝空气 |
| D.过程中含硅元素的物质只体现氧化性 |
您最近半年使用:0次
名校
解题方法
9 . 钙钛矿( )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
Ⅰ. 为制备
为制备 的一种原料。
的一种原料。
(1)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是______ 。
Ⅱ.一类有机一无机杂化材料 具有与
具有与 相同的晶体结构。
相同的晶体结构。
(2)①有机阳离子 中C原子和N原子的电负性大小比较:C
中C原子和N原子的电负性大小比较:C______ N(填“ ”、“
”、“ ”或“
”或“ ”),从原子结构的角度说明理由
”),从原子结构的角度说明理由______ 。
②若将晶胞中的A坐标定义为 ,B坐标定义为
,B坐标定义为 ,则离A最近的微粒的坐标为
,则离A最近的微粒的坐标为______ (任写其一)。若将晶胞中心微粒的坐标定义为 ,则与其紧邻的
,则与其紧邻的 的坐标为
的坐标为______ (任写其一)。 键角大小比较:
键角大小比较:
______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是______ 。
(3) 晶体生长过程中容易产生晶体缺陷,造成
晶体生长过程中容易产生晶体缺陷,造成 空位。用
空位。用 替换
替换 可改善这种情况的可能原因是
可改善这种情况的可能原因是______ 。
 )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:Ⅰ.
 为制备
为制备 的一种原料。
的一种原料。(1)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是化合物 |
|
|
|
|
熔点 | 377 |
|
| 155 |
Ⅱ.一类有机一无机杂化材料
 具有与
具有与 相同的晶体结构。
相同的晶体结构。(2)①有机阳离子
 中C原子和N原子的电负性大小比较:C
中C原子和N原子的电负性大小比较:C ”、“
”、“ ”或“
”或“ ”),从原子结构的角度说明理由
”),从原子结构的角度说明理由②若将晶胞中的A坐标定义为
 ,B坐标定义为
,B坐标定义为 ,则离A最近的微粒的坐标为
,则离A最近的微粒的坐标为 ,则与其紧邻的
,则与其紧邻的 的坐标为
的坐标为
 键角大小比较:
键角大小比较:
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是(3)
 晶体生长过程中容易产生晶体缺陷,造成
晶体生长过程中容易产生晶体缺陷,造成 空位。用
空位。用 替换
替换 可改善这种情况的可能原因是
可改善这种情况的可能原因是
您最近半年使用:0次
名校
10 . 我国科学家通过机械化学方法,在氢化镧(LaH1.95~3)晶格中制造大量的缺陷和纳米微晶,研发出首个室温环境下超快氢负离子(H−)导体。下列说法不正确 的是
| A.电负性:La > H | B.氢属于s区元素 |
| C.H−具有还原性 | D.超快氢负离子导体有望用于新型电池研发 |
您最近半年使用:0次
2024-04-15更新
|
167次组卷
|
2卷引用:北京市丰台区2023-2024学年高三下学期综合练习(一)化学试题