名校
1 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:_______ ,B:_______ ,E_______ ,G:_______ 。
(2)C、D、E三种元素的原子半径由大到小的顺序为_______ (用元素符号表示)。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:_______ ,_______ ,_______ 。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为_______ 。
(5)G元素可形成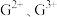 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:_______ 。
(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是_______ 化合物(填“离子”或“共价”)。根据“对角线规则”,元素周期表中某些处于对角的元素,它们的化合物性质具有相似性,则M的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为_______ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: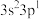 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)C、D、E三种元素的原子半径由大到小的顺序为
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)G元素可形成
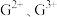 ,其中较稳定的是
,其中较稳定的是 ,试从核外电子排布的角度解释其原因:
,试从核外电子排布的角度解释其原因:(6)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近半年使用:0次
2 . 根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)已知铬是24号元素,画出Cr的价层电子排布图:_______ 。
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序是_______ 。
(5)Zn2+的核外电子排布式为_______ 。
(1)基态N原子中,核外电子占据的最高能层的符号是L,占据该能层电子的原子轨道形状为
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)已知铬是24号元素,画出Cr的价层电子排布图:
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(5)Zn2+的核外电子排布式为
您最近半年使用:0次
解题方法
3 . 下列陈述Ⅰ和陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 三氟乙酸酸性强于三氯乙酸 | F原子电负性大于 原子,吸电子能力强 原子,吸电子能力强 |
| B | 常温下,铜与稀硫酸不反应,与稀硝酸反应 | 硝酸酸性强于硫酸 |
| C | 缺角的氯化钠晶体在饱和 溶液 溶液中慢慢变为完美的立方体块 | 晶体有各向异性 |
| D | 利用 除去废水中的 除去废水中的 |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
4 . 一种因具有成本低廉及反应性质多样等优点被用作有机合成的缩合试剂,其由4种短周期非金属元素组成,结构如图所示,其中W、X、Y为同一周期,X与Z为同一主族。下列说法正确的是
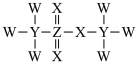
| A.简单氢化物的沸点:Y>W | B.电负性:X>W>Y>Z |
| C.XW2中元素X为sp3杂化 | D.YX2是含极性键的极性分子 |
您最近半年使用:0次
5 . 由原子序数依次增大的短周期主族元素X、Y、Z、W构成的离子化合物结构如下图所示,Y、Z相邻且与X、W均不同周期。下列说法不正确的是
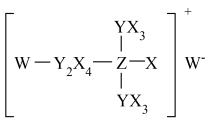
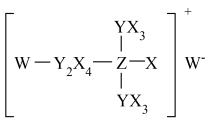
A.元素电负性: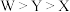 |
B. 的VSEPR模型为四面体形 的VSEPR模型为四面体形 |
| C.Y和Z的简单氢化物都是由极性键构成的极性分子 |
D.第一电离能: |
您最近半年使用:0次
解题方法
6 . 2024年是元素周期表诞生的第155周年。已知短周期主族元素X、Y、Z、M、N,其原子序数与其对应的0.1mol/L最高价氧化物的水化物溶液,在常温下的pH关系如图所示。下列说法中正确的是

| A.X和Y元素均在p区 | B.元素的电负性:Z>M>N |
| C.M的含氧酸根离子的中心原子为sp2杂化 | D.XN3和ZN3的空间构型均为三角锥形 |
您最近半年使用:0次
7 . 下列对价电子构型为2s22p5的元素描述正确的是
| A.电负性最大 | B.最高正价为+7 |
| C.同周期中第一电离能最大 | D.同周期中原子半径最大 |
您最近半年使用:0次
名校
解题方法
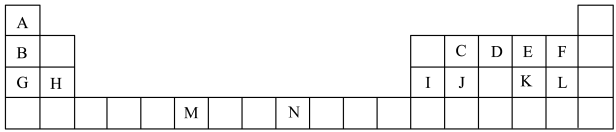
8 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)表中元素,电负性最强的是___________ (填元素符号),J的元素名称为___________ 。N基态原子核外能级上有___________ 未成对电子。
(2)D元素原子的价电子排布图为___________ ,核外有___________ 种不同运动状态的电子。
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是___________ (填“极性”或“非极性”)分子。
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是___________ (填字母)。
(1)表中元素,电负性最强的是
(2)D元素原子的价电子排布图为
(3)ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
(4)C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
a.  b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
b. CH4 c.CH2=CHCH3 d. CH3CH2C≡CH
您最近半年使用:0次
名校
9 . 下列说法正确的是
| A.Ge(锗)、As(砷)、Se(硒)的电负性依次增大 |
B.硼原子核外电子由 ,原子释放能量 ,原子释放能量 |
| C.C、N、O三种元素第一电离能从大到小的顺序是O>N>C |
D.基态某原子的价层电子排布式为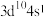 ,推断该元素位于第四周期第ⅠA族 ,推断该元素位于第四周期第ⅠA族 |
您最近半年使用:0次
2024-04-05更新
|
200次组卷
|
2卷引用:广东省广州市真光中学2023-2024学年高二下学期3月阶段性质量检测化学试题
解题方法
10 . 化合物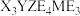 所含的5种元素均为短周期主族元素,
所含的5种元素均为短周期主族元素, 、
、 和
和 为同周期元素,原子序数依次增加,
为同周期元素,原子序数依次增加, 的基态原子价层电子排布式为
的基态原子价层电子排布式为 ,
, 的基态原子价层
的基态原子价层 轨道半充满,
轨道半充满, 是地壳中含量最多的元素,
是地壳中含量最多的元素, 是有机分子的骨架元素,下列说法正确的是
是有机分子的骨架元素,下列说法正确的是
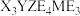 所含的5种元素均为短周期主族元素,
所含的5种元素均为短周期主族元素, 、
、 和
和 为同周期元素,原子序数依次增加,
为同周期元素,原子序数依次增加, 的基态原子价层电子排布式为
的基态原子价层电子排布式为 ,
, 的基态原子价层
的基态原子价层 轨道半充满,
轨道半充满, 是地壳中含量最多的元素,
是地壳中含量最多的元素, 是有机分子的骨架元素,下列说法正确的是
是有机分子的骨架元素,下列说法正确的是A.元素电负性: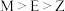 |
B.简单氢化物沸点: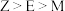 |
C.第一电离能: |
D. 和 和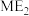 的空间结构均为直线形 的空间结构均为直线形 |
您最近半年使用:0次
2024-04-04更新
|
707次组卷
|
2卷引用:广东省广州市2024届高三下学期一模考试化学试题



