名校
解题方法
1 . 已知: 与
与 在一定条件下可以发生如下反应,
在一定条件下可以发生如下反应,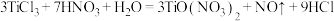 .回答下列问题:
.回答下列问题:
(1)基态钛原子的核外电子排布式为_____________ .
(2)N、H、O三种元素的电负性由大到小的顺序为_____________ .
(3)上述方程式中涉及的元素中属于P区元素的是_____________ (填元素符号).
(4) 的空间结构为
的空间结构为_____________ .
(5)肼 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被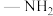 (氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下:
(氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下: .若该反应中有
.若该反应中有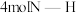 键断裂,则形成的
键断裂,则形成的 键有
键有_____________  .
.
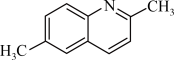
(6)由C、H、N三种元素形成的一种有机物的结构简式如下,则该物质中N原子的杂化方式为_____________ ,C原子的杂化方式为_____________ .
 与
与 在一定条件下可以发生如下反应,
在一定条件下可以发生如下反应,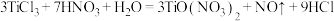 .回答下列问题:
.回答下列问题:(1)基态钛原子的核外电子排布式为
(2)N、H、O三种元素的电负性由大到小的顺序为
(3)上述方程式中涉及的元素中属于P区元素的是
(4)
 的空间结构为
的空间结构为(5)肼
 分子可视为
分子可视为 分子中的一个氢原子被
分子中的一个氢原子被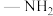 (氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下:
(氨基)取代形成的另一种氮的氢化物.肼可用作火箭燃料,燃烧时发生的反应如下: .若该反应中有
.若该反应中有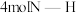 键断裂,则形成的
键断裂,则形成的 键有
键有 .
.(6)由C、H、N三种元素形成的一种有机物的结构简式如下,则该物质中N原子的杂化方式为
您最近半年使用:0次
2 . 短周期主族元素X、Y、Z、W、Q原子序数依次增大,其中Q是元素周期表中电负性最大的元素,由这五种元素组成的某药物结构如图所示。下列有关说法正确的是

A.电负性: |
B.第一电离能: |
| C.该分子中所有原子都满足8电子稳定结构 |
D.基态Z原子电子轨道表示式为: |
您最近半年使用:0次
名校
3 . TFMT因具有成本低廉及反应性质多样等优点被用作有机合成的缩合试剂,其结构如图所示,其中W、X、Y、Z为原子半径依次增大的短周期非金属元素,W位于元素周期表的p区。下列说法错误的是
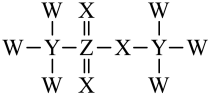
| A.元素电负性:W>X>Y | B.基态原子未成对电子数:Y=Z>W |
| C.所有原子都满足8电子结构 | D.简单氢化物沸点:X>W>Y |
您最近半年使用:0次
4 . 离子液体是指由体积较大的阴、阳离子组成,并且在室温或接近室温下呈液态的盐,也称为低温熔融盐。有许多优点,例如难挥发,有良好的导电性,可作溶剂、电解质、催化剂等。1-正丁基-3-甲基咪唑六氟磷酸盐是一种离子液体,结构简式如图,下列关于它的叙述正确的是
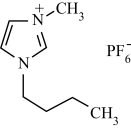 或
或
A.该新型化合物含有的C、N、P元素均为 杂化 杂化 |
| B.1-正丁基-3-甲基咪唑六氟磷酸盐属于含共价键的离子化合物 |
| C.电负性:F>N>H>C |
| D.该新型化合物的组成元素全部位于元素周期表p区 |
您最近半年使用:0次
名校
解题方法
5 . 前四周期元素X、Y、Z、W的原子序数依次增大,X原子中有6个运动状态不同的电子,Y是地壳中含量最多的元素,基态Z原子K、L层上的电子总数是3p原子轨道上电子数的两倍,基态W原子中有6个未成对电子。下列说法不正确的是
| A.电负性: X < Y,原子半径: X < Y |
| B.同周期中,除稀有气体外元素Z的第一电离能最大 |
| C.在一定条件下,X与氢元素形成的某些化合物与Z的单质及氢化物均能反应 |
D.在一定条件下,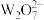 和 和 可以相互转化,且二者均具有强氧化性 可以相互转化,且二者均具有强氧化性 |
您最近半年使用:0次
6 . 以下有关元素性质的说法正确的是
| A.①Na、K、Rb;②N、P、As;③O、S、Se;④P、S、Cl,元素的电负性随原子序数增大而递增的是③ |
| B.某元素的逐级电离能分别为738、1451、7733、10540、13630、17995、21703,该元素一定在第三周期第ⅢA族 |
| C.下列基态原子中,①1s22s22p63s23p1 ②1s22s22p63s23p2 ③1s22s22p63s23p3 ④1s22s22p63s23p5,对应的第一电离能最大的是④ |
| D.以下原子中,①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p1,半径最大的是① |
您最近半年使用:0次
名校
解题方法
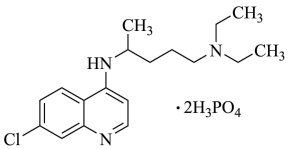
7 . 2020年2月15日,由国家科研攻关组的主要成员单位的专家组共同研判磷酸氯喹在细胞水平上能有效抑制新型冠状病毒(2019-nCoV)的感染。
(1)已知磷酸氯喹的结构如图所示,则一个磷酸氯喹分子中含___________ 个 杂化的碳原子;分子中N原子的杂化方式为
杂化的碳原子;分子中N原子的杂化方式为___________ ;基态磷原子核外电子的空间运动状态有___________ 种。
(2) 与金刚石均为碳的单质,从结构与性质之间的关系解释
与金刚石均为碳的单质,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是___________ 。
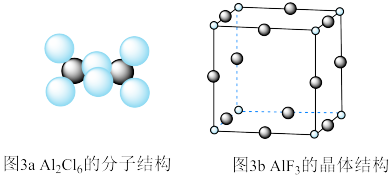
(3)气态 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为
的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为___________ 。 结构属立方晶系,晶胞如图3b所示,
结构属立方晶系,晶胞如图3b所示, 的配位数为
的配位数为___________ 。若晶胞参数为apm,晶体密度ρ=___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(4)吡啶(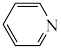 )分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是
)分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是___________ (填代号)。
a.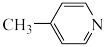 b.
b.  c.
c. 
(1)已知磷酸氯喹的结构如图所示,则一个磷酸氯喹分子中含
 杂化的碳原子;分子中N原子的杂化方式为
杂化的碳原子;分子中N原子的杂化方式为
(2)
 与金刚石均为碳的单质,从结构与性质之间的关系解释
与金刚石均为碳的单质,从结构与性质之间的关系解释 的熔点远低于金刚石的原因是
的熔点远低于金刚石的原因是(3)气态
 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为
的形式存在,其空间结构如图3a所示,二聚体中Al的轨道杂化类型为 结构属立方晶系,晶胞如图3b所示,
结构属立方晶系,晶胞如图3b所示, 的配位数为
的配位数为 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(4)吡啶(
 )分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是
)分子中氮原子电子云密度越大,碱性越强。下列物质的碱性由强到弱的排序是a.
 b.
b.  c.
c. 
您最近半年使用:0次
名校
8 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素。请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向,C的简单离子核外有___________ 种运动状态不同的电子。
(2)已知氮元素与A形成的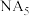 为离子化合物,写出其电子式
为离子化合物,写出其电子式___________ 。
(3) 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由___________ 。
(4) 分子的空间构型为
分子的空间构型为___________ , 分子的VSEPR模型名称为
分子的VSEPR模型名称为___________ 。
(5)下列气态分子 、
、 、
、 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为___________ 。
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外p电子数与s电子数相等 |
| C | 基态原子的价电子排布为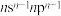 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)已知氮元素与A形成的
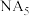 为离子化合物,写出其电子式
为离子化合物,写出其电子式(3)
 难溶于二硫化碳,简要说明理由
难溶于二硫化碳,简要说明理由(4)
 分子的空间构型为
分子的空间构型为 分子的VSEPR模型名称为
分子的VSEPR模型名称为(5)下列气态分子
 、
、 、
、 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近半年使用:0次
9 . 剪纸艺术遗产经国务院批准列入第一批国家级非物质文化遗产名录,剪纸定稿后可利用“赤血盐”等物质通过“晒蓝图”的方法多量复制。“赤血盐”学名“铁氰化钾”,是一种无机物,化学式为 ,红色晶体,可溶于水,水溶液带有黄绿色荧光,含有铁氰根配离子
,红色晶体,可溶于水,水溶液带有黄绿色荧光,含有铁氰根配离子 。下列说法正确的是
。下列说法正确的是
 ,红色晶体,可溶于水,水溶液带有黄绿色荧光,含有铁氰根配离子
,红色晶体,可溶于水,水溶液带有黄绿色荧光,含有铁氰根配离子 。下列说法正确的是
。下列说法正确的是A.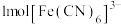 中含有 中含有 键的数目为 键的数目为 |
B. 属于离子晶体,含有两种阳离子 属于离子晶体,含有两种阳离子 |
C. 所含元素中第一电离能和电负性最大的均是碳元素 所含元素中第一电离能和电负性最大的均是碳元素 |
D. 中心离子的配位数为6 中心离子的配位数为6 |
您最近半年使用:0次
名校
10 . 现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5,则下列有关比较中正确的是
| A.第一电离能:④>③>②>① | B.最高正化合价:④>③=②>① |
| C.电负性:④>③>②>① | D.原子半径:①>②>③>④ |
您最近半年使用:0次



