解题方法
1 . 现有10种元素,其中X、Y、Z、A、E为短周期主族元素,原子序数依次增大;M、R、Q为第4周期元素。X元素原子的核外电子只有一种自旋取向;Y的基态原子核外2个能级上有电子,且每个能级上的电子数相等;Z原子核外有6种运动状态不同的电子。A元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素;E元素原子半径在同周期元素中最大;M是第四周期最外层只有一个电子的元素中原子序数最大的。R的3价阳离子遇KSCN溶液显红色。Q是ds区元素,基态原子核外7个能级上的电子均充满。请根据相关信息回答问题。
(1)Y、Z、A、E四种元素电负性由大到小的顺序:___________ (填元素符号)。Y、Z、A、E四种元素原子半径由大到小的顺序:___________ (填元素符号)。
(2)R元素的基态原子的电子排布式___________ ,占据最高能级电子的电子云轮廓图为___________ 形。Q在周期表中位于第四周期第___________ 族。
(3)X与Z形成的化合物的相对分子质量是26,其分子中σ键与π键的数目之比为___________ 。
(4)Y的氧化物与E的氢氧化物发生化学反应的离子方程式:___________ 。
(5)E在火焰上灼烧产生的黄光是一种___________ 光谱(填“发射”“吸收”)。
(6)从结构角度看,R2+易被氧化成R3+的原因是___________ 。
(7)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[R(H2O)6]3+显棕黄色。据此判断,[Q(H2O)4]2+___________ (填“无”或“有”)颜色。
(1)Y、Z、A、E四种元素电负性由大到小的顺序:
(2)R元素的基态原子的电子排布式
(3)X与Z形成的化合物的相对分子质量是26,其分子中σ键与π键的数目之比为
(4)Y的氧化物与E的氢氧化物发生化学反应的离子方程式:
(5)E在火焰上灼烧产生的黄光是一种
(6)从结构角度看,R2+易被氧化成R3+的原因是
(7)过渡元素的金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色,为d1~d9排布时,有颜色,如[R(H2O)6]3+显棕黄色。据此判断,[Q(H2O)4]2+
您最近半年使用:0次
名校
2 . 下列关于物质结构和性质的说法正确的是
A.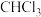 的球棍模型为 的球棍模型为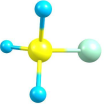 |
B.二氯化二硫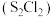 的电子式为 的电子式为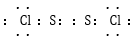 |
C. 的 的 模型与空间结构名称均为正四面体形 模型与空间结构名称均为正四面体形 |
D.酸性: |
您最近半年使用:0次
名校
3 . 某含铜催化剂的阳离子的结构如下图所示。X、Y、Z、W是原子序数依次增大的短周期元素,其中Y、Z、W位于同一周期,基态Y原子的价层电子排布式为nsnnpn。下列说法错误的是

| A.元素电负性:W>Z>Y |
| B.Z、W的最简单氢化物可形成氢键 |
| C.W元素的氧化物对应的水化物能与CuO反应 |
| D.W元素的单质与水反应属于置换反应 |
您最近半年使用:0次
4 . 我国某有机所研究团队合成一种盐,其阴离子结构如图所示。短周期主族元素X、Y、Z、R的原子序数依次增大,X、Y、Z的原子序数之和为23,下列有关叙述不正确的是
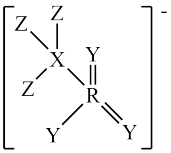
| A.电负性:Z>Y>R | B.简单氢化物的稳定性:Z>Y>X |
C.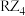 的键角和 的键角和 的键角相等 的键角相等 | D.X的单质可能是共价晶体 |
您最近半年使用:0次
名校
解题方法
5 . 钝、钒、铬、铁、镍、铜等过渡金属及其化合物在工业上有重要用途。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。 元素在元素周期表中的位置是
元素在元素周期表中的位置是_______ 。
(2)制备CrO2Cl2的反应为 。
。
①上述化学方程式中非金属元素电负性由小到大的顺序为_______ (用元素符号表示)。
②COCl2分子中所有原子均满足8电子稳定结构,COCl2分子中π键和σ键的个数比为_______ ,中心原子的杂化方式为_______ 。
(3)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:_______ 。
②该钒的硫化物的晶体中,与每V原子最近且等距S原子的个数是_______ 。
(1)钛铁合金具有放氢温度低、价格适中等优点,是钛系储氢合金的代表。
 元素在元素周期表中的位置是
元素在元素周期表中的位置是(2)制备CrO2Cl2的反应为
 。
。①上述化学方程式中非金属元素电负性由小到大的顺序为
②COCl2分子中所有原子均满足8电子稳定结构,COCl2分子中π键和σ键的个数比为
(3)一种钒的硫化物的晶体结构(图a)及其俯视图(图b)如图所示:
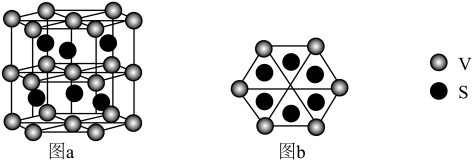
②该钒的硫化物的晶体中,与每V原子最近且等距S原子的个数是
您最近半年使用:0次
名校
解题方法
6 . 氟元素可形成多种有工业价值和科研价值的化合物,如OF2、(CF)x、XeF2、HF、NH4BF4、CaF2等。
(1)基态F原子核外电子有______ 种空间运动状态,下列为氟原子激发态的电子排布式的是_____ (填序号)。
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p2 D.1s22s22p33p2
(2)F2通入稀NaOH溶液中可生成OF2,其中氧原子的杂化方式为_________ 。
(3)AlF3的熔点为1090℃,远高于AlCl3的熔点(192℃),其原因是___________ 。
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,(CF)x的导电性________ (填“增强”或“减弱”),(CF)x中C-C键的键长比石墨中C-C键的_______ (填“长”或“短”)。

(5)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂HF、NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为________ ,1mol氟硼酸铵(NH4BF4)中含有_______ mol配位键。
(1)基态F原子核外电子有
A.1s22s22p43s1 B.1s22s22p43d2 C.1s22s12p2 D.1s22s22p33p2
(2)F2通入稀NaOH溶液中可生成OF2,其中氧原子的杂化方式为
(3)AlF3的熔点为1090℃,远高于AlCl3的熔点(192℃),其原因是
(4)石墨与F2在450℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具有润滑性,其单层局部结构如图所示。与石墨相比,(CF)x的导电性

(5)芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。其中“刻蚀”过程可能用到刻蚀剂HF、NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为
您最近半年使用:0次
7 . 下列事实的解释错误的是
| 事实 | 解释 | |
| A | 酸性:CH3COOH<CCl3COOH<CF3COOH | H的电负性小于氯原子,氯原子小于氟原子,电负性越强羟基上的氢原子越容易电离,酸性越强 |
| B | 第一电离能: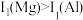 | Mg为3p轨道全空的稳定电子构型,而Al失去一个电子变为3p轨道全空的稳定电子构型 |
| C | O2与O3分子极性相同 | 二者都是由非极性键构成的分子 |
| D | 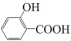 的沸点比 的沸点比 低 低 | 前者形成了分子内氢键,后者形成分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
8 . 工业制取氮化硼的反应原理: 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是
| A.电负性:B>N>H |
| B.键角:NH3>BCl3 |
| C.NH3与BCl3都是非极性分子 |
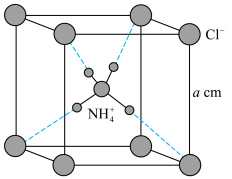
D.NH4Cl晶胞如图所示,则距离 最近的Cl-有8个 最近的Cl-有8个 |
您最近半年使用:0次
解题方法
9 . 离子液体在化工领域具有广泛的应用前景。一种离子液体的结构如图所示,下列有关说法不正确的是
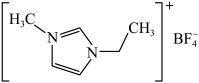
A.电负性: |
B.第一电离能: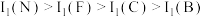 |
| C.该化合物的离子键弱,熔点低 |
D.该化合物中N原子发生 和 和 杂化 杂化 |
您最近半年使用:0次
名校
10 . 天然独居石中,铈( ,
,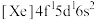 )主要以
)主要以 形式存在,还含有
形式存在,还含有 ,
, ,
, 等物质,下列说法不正确的是
等物质,下列说法不正确的是
 ,
,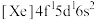 )主要以
)主要以 形式存在,还含有
形式存在,还含有 ,
, ,
, 等物质,下列说法不正确的是
等物质,下列说法不正确的是A. 和 和 属于s区元素 属于s区元素 |
B.基态 原子有4个运动状态不同的价电子 原子有4个运动状态不同的价电子 |
C.上述元素中,电负性最大的是 |
D.同周期中,比 第一电离能大的元素有2种 第一电离能大的元素有2种 |
您最近半年使用:0次



