名校
1 . 下列对有关事实的解释错误的是
| 选项事实 | 解释 | |
| A | 酸性:CF3COOH>CH3COOH | F电负性更大使羟基极性变强 |
| B | 金刚石的熔点高于单晶硅 | 金刚石的C-C比单晶硅的Si-Si键能大 |
| C | 稳定性:H2O>H2S | H-O键的键能比H-S键的键能大 |
| D | SiO2的熔点比干冰高 | SiO2比CO2相对分子质量大,分子间作用力大 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 某离子液体结构如图所示。W、X、Y、Z原子序数依次增大,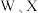 和
和 的原子序数之和为
的原子序数之和为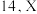 和
和 基态原子的核外未成对电子数之和为
基态原子的核外未成对电子数之和为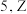 是第四周期元素。下列说法不正确的是
是第四周期元素。下列说法不正确的是
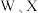 和
和 的原子序数之和为
的原子序数之和为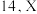 和
和 基态原子的核外未成对电子数之和为
基态原子的核外未成对电子数之和为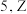 是第四周期元素。下列说法不正确的是
是第四周期元素。下列说法不正确的是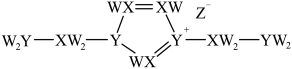
A.该物质的熔点低于 |
B.电负性: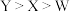 |
| C.W、Y、Z可形成既含离子键又含共价键的化合物 |
| D.已知阳离子环与苯环的结构相似,则环上的两个Y原子的杂化方式不同 |
您最近半年使用:0次
3 . 下列说法正确的是
①非极性分子往往具有高度对称性,如 、
、 、
、 、
、 这样的分子
这样的分子
②同一周期从左到右,元素的第一电离能、电负性都是越来越大
③等离子体是由阴阳离子直接构成的气体
④ 分子中键角小于
分子中键角小于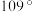 是因为孤电子对对键合电子对排斥力大
是因为孤电子对对键合电子对排斥力大
⑤ 溶沸点高于
溶沸点高于 是因为
是因为 电负性大,形成的
电负性大,形成的 更稳定
更稳定
⑥熔融状态下能导电的化合物一定是离子化合物
⑦含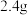 碳原子的金刚石晶体中共价键个数为
碳原子的金刚石晶体中共价键个数为
①非极性分子往往具有高度对称性,如
 、
、 、
、 、
、 这样的分子
这样的分子②同一周期从左到右,元素的第一电离能、电负性都是越来越大
③等离子体是由阴阳离子直接构成的气体
④
 分子中键角小于
分子中键角小于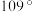 是因为孤电子对对键合电子对排斥力大
是因为孤电子对对键合电子对排斥力大⑤
 溶沸点高于
溶沸点高于 是因为
是因为 电负性大,形成的
电负性大,形成的 更稳定
更稳定⑥熔融状态下能导电的化合物一定是离子化合物
⑦含
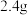 碳原子的金刚石晶体中共价键个数为
碳原子的金刚石晶体中共价键个数为
| A.①②⑥⑦ | B.④⑥⑦ | C.④⑤⑥ | D.③④⑦ |
您最近半年使用:0次
名校
4 . X、Y、Z、W、Q五种短周期主族元素在元素周期表中的相对位置如下表所示。已知:①Y元素的最高价氧化物对应水化物与其简单气态氢化物通过化合反应生成一种盐;②通常情况下,W与Q形成的化合物甲为白色晶体,常作调味品。下列判断错误的是
| …… | X | Y | Z | ||
| W | …… | Q |
| A.第一电离能:Y<Z |
| B.电负性:X<Q |
| C.Y形成的双原子分子中σ键与π键的个数之比为1∶2 |
| D.甲的一个晶胞中含4个阳离子 |
您最近半年使用:0次
名校
解题方法
5 . 已知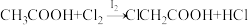 ,
, 的酸性比
的酸性比 强。下列有关说法正确的是
强。下列有关说法正确的是
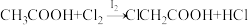 ,
, 的酸性比
的酸性比 强。下列有关说法正确的是
强。下列有关说法正确的是A.HCl的电子式为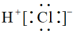 | B.Cl-Cl键的键长比I-I键长 |
C. 分子中只有σ键 分子中只有σ键 | D. 的酸性比 的酸性比 强 强 |
您最近半年使用:0次
2024-04-05更新
|
174次组卷
|
2卷引用:湖南省绥宁县第一中学2022-2023学年高二下学期期中考试化学试题
名校
解题方法
6 . 碳氢氟氮硅等非金属元素与人类的生产生活息息相关。回答下列问题:
(1)写出硅原子的电子排布式___________ 。C、Si、N的电负性由大到小的顺序是___________ 。
(2)氟化氢水溶液中存在氢键有___________ 种。
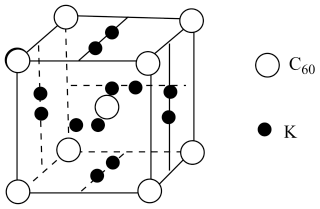
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为___________ 。
(4)继C60后,科学家又合成了Si60、N60.请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量:N60>C60>Si60,其原因是:___________ 。
(1)写出硅原子的电子排布式
(2)氟化氢水溶液中存在氢键有
(3)科学家把C60和K掺杂在一起制造了一种富勒烯与钾的化合物,该物质在低温时是一种超导体,其晶胞如图所示,该物质中K原子和C60分子的个数比为

(4)继C60后,科学家又合成了Si60、N60.请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量:N60>C60>Si60,其原因是:
您最近半年使用:0次
名校
解题方法
7 . A、B、C、D、E分别代表五种短周期元素,且原子序数依次增大,已知:B的最外层电子排布是nsnnpn+1;C的p能级上未成对的电子比B少一个;D的二价阳离子与C的阴离子具有相同的电子层结构;E与D同周期且E在该周期中原子半径最小;B与A的单质能生成具有刺激性气味的气体,该气体极易溶于水。)
(1)B原子核外电子排布式为___________ 。
(2)A与E化合时原子间以___________ 键相结合,D与C化合时原子间以___________ 键相结合。
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:___________ 。
(4)A与B形成化合物时,中心原子采取___________ 杂化成键,其立体结构为___________ ,属于___________ (填“极性”或“非极性”)分子。
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:___________ 。
(6)五种元素中电负性最大的是___________ (填元素名称)。
(1)B原子核外电子排布式为
(2)A与E化合时原子间以
(3)写出A、C的单质直接化合形成的化合物与E单质反应的离子方程式:
(4)A与B形成化合物时,中心原子采取
(5)将白色的无水CuSO4溶解于A2C中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:
(6)五种元素中电负性最大的是
您最近半年使用:0次
名校
解题方法
8 . 下列关于物质的结构或性质及解释都正确的是
选项 | 物质的结构或性质 | 解释 |
A | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH的羧基中O—H的极性更大 |
B | 熔点:SiO2>CO2 | 相对分子质量:SiO2大于CO2 |
C | O2与O3分子极性相同 | 二者都是由非极性键构成的分子 |
D | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛分子间范德华力更强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-03更新
|
403次组卷
|
3卷引用:湖南省长郡中学2023-2024学年高二下学期寒假检测(开学考试)化学试题
9 . 胆矾是一种中药,有催吐、祛腐、解毒等功效,其晶体的结构如图所示。下列说法正确的是


| A.该晶体中所有元素的基态原子里都含有单电子 |
| B.原子电负性从大到小的顺序为:O>S>H>Cu |
| C.晶体中存在的化学键为:离子键、极性共价键、氢键和配位键 |
D. 的沸点高于 的沸点高于 的原因是O的非金属性强于S 的原因是O的非金属性强于S |
您最近半年使用:0次
名校
解题方法
10 . 物质的结构决定其性质。下列实例与解释合理的是
| 选项 | 实例 | 解释 |
| A |  易溶于 易溶于 |  和 和 均含有硫元素 均含有硫元素 |
| B |  比 比 熔点高 熔点高 | 键能: 键大于 键大于 键 键 |
| C |  中氢显 中氢显 价、 价、 中氢显 中氢显 价 价 | 电负性: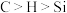 |
| D |  的酸性大于 的酸性大于 |  的相对分子质量大于 的相对分子质量大于 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



