名校
1 . 原子结构与元素周期表存在着内在联系。根据已学知识,请回答下列问题:
(1)基态N原子电子占据___________ 个能层,电子占据的最高能级的符号是___________ ;基态N原子共有___________ 种不同空间运动状态的电子。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:___________ ,位于元素周期表的___________ 区。
(3)比较Cu和Zn的第二电离能大小[用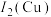 和
和 表示]:
表示]:___________ 。
(4)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填选项)。
(5)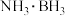 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(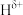 ),与B原子相连的H负电性(
),与B原子相连的H负电性(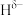 )。在H、B、N三种元素中,电负性由大到小的顺序是
)。在H、B、N三种元素中,电负性由大到小的顺序是___________ 。
(1)基态N原子电子占据
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(3)比较Cu和Zn的第二电离能大小[用
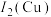 和
和 表示]:
表示]:(4)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填选项)。
A.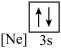 | B.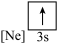 | C. | D.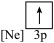 |
(5)
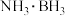 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(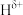 ),与B原子相连的H负电性(
),与B原子相连的H负电性(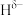 )。在H、B、N三种元素中,电负性由大到小的顺序是
)。在H、B、N三种元素中,电负性由大到小的顺序是
您最近半年使用:0次
名校
解题方法
2 . 下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)表中元素,电负性最强的是___________ (填元素符号);J的元素名称为___________ ;N基态原子价电子层上有___________ 个未成对电子。
(2) 的稳定性比
的稳定性比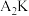
___________ (填写“大”或“小”):原因是___________ 。
(3)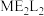 常温下为深红色液体,能与
常温下为深红色液体,能与 、
、 等互溶,据此可判断
等互溶,据此可判断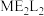 是
是___________ (填“极性”或“非极性”)分子。
(4)① ②
② ③
③ ④
④ ,这四种物质中碳原子采取
,这四种物质中碳原子采取 杂化的是
杂化的是___________ (填序号);乳酸分子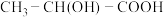 中有
中有___________ 个手性碳原子。
(5)J、K、L元素的电负性由大到小的顺序为___________ (用元素符号表示);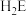 的键角比
的键角比
___________ (填写“大”或“小”):原因是___________ 。

(1)表中元素,电负性最强的是
(2)
 的稳定性比
的稳定性比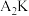
(3)
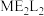 常温下为深红色液体,能与
常温下为深红色液体,能与 、
、 等互溶,据此可判断
等互溶,据此可判断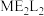 是
是(4)①
 ②
② ③
③ ④
④ ,这四种物质中碳原子采取
,这四种物质中碳原子采取 杂化的是
杂化的是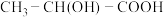 中有
中有(5)J、K、L元素的电负性由大到小的顺序为
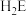 的键角比
的键角比
您最近半年使用:0次
名校
3 . 下列事实与元素的电负性无关的是
A. 分子中 分子中 元素显-1价, 元素显-1价, 元素显+1价 元素显+1价 | B. 分子中的键角小于 分子中的键角小于 分子中的键角 分子中的键角 |
C. 是极性分子,可溶于水 是极性分子,可溶于水 | D. 易形成分子间氢键 易形成分子间氢键 |
您最近半年使用:0次
4 . 消毒液的主要成分为NaClO,现按要求回答下列问题:
(1)消毒液的组成元素中,基态O原子的价电子排布式是___________ ,基态Cl原子未成对电子数为___________ 个。
(2)医用酒精主要成分为C2H5OH,其分子中碳原子的杂化方式为___________ ,组成元素电负性大小顺序为___________ ,1mol C2H5OH分子中含有σ键数目为___________ 。
(3)干冰升华时克服的作用力是___________。
(4)H2O2也可以做消毒液,其电子式为___________ ,利用所学试着解释为什么H2O2难溶于CS2?___________
(1)消毒液的组成元素中,基态O原子的价电子排布式是
(2)医用酒精主要成分为C2H5OH,其分子中碳原子的杂化方式为
(3)干冰升华时克服的作用力是___________。
| A.离子键 | B.共价键 | C.氢键 | D.范德华力 |
您最近半年使用:0次
名校
5 . 回答下列问题:
(1)第四周期未成对电子数最多的元素是___________ (填元素符号),该元素基态原子核外电子共有___________ 种不同能量的电子。
(2)丁二酮(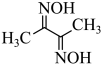 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为___________ ,该物质中,σ键与π键数目之比为___________ 。
(3)比较键角大小:AsO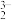
___________ AsO (填>、<或=)。
(填>、<或=)。
(4)铜的下列状态中,失去最外层一个电子所需能量最小的是___________。
(1)第四周期未成对电子数最多的元素是
(2)丁二酮(
 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为(3)比较键角大小:AsO
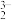
 (填>、<或=)。
(填>、<或=)。(4)铜的下列状态中,失去最外层一个电子所需能量最小的是___________。
| A.[Ar]3d104p1 | B.[Ar]3d10 | C.[Ar]3d94s1 | D.[Ar]3d104s1 |
您最近半年使用:0次
名校
解题方法
6 . 过渡元素在现代工农业生产和科技发展方面具有重要的用途。回答下列问题:
(1)已知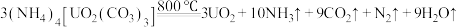 。
。
①基态U原子的外围电子排布式为 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是___________ (填标号)。
A. B.
B. 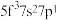 C.
C. 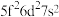 D.
D. 
②反应中断裂的化学键有___________ (填标号)。
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是___________ (填化学式,下同);氢化物中更易与 形成配离子的是
形成配离子的是___________ 。向 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式___________ 。
(2)一个配体中有两个配位原子的配体叫双齿配体,C2O 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为___________
(3)四羰基镍 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是___________ 。
(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为___________ (保留三位小数)。

(1)已知
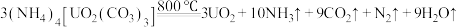 。
。①基态U原子的外围电子排布式为
 ,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是
,则处于下列状态的铀原子或离子失去一个电子所需能量最高的是A.
 B.
B. 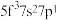 C.
C. 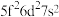 D.
D. 
②反应中断裂的化学键有
a.氢键 b.极性键 c.非极性键 d.离子键 e.配位键
③反应所得的气态产物中属于非极性分子的是
 形成配离子的是
形成配离子的是 溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式
溶液中滴加少量氨水,产生蓝色沉淀,继续滴加氨水可得到深蓝色透明溶液,写出该反应的离子方程式(2)一个配体中有两个配位原子的配体叫双齿配体,C2O
 就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为
就是一种双齿配体。Fe3+的配位数是6,硫酸铁溶液中加入H2C2O4后生成配离子的化学式为(3)四羰基镍
 是制备铂镍合金的重要原料之一,
是制备铂镍合金的重要原料之一, 为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是
为无色有挥发性的剧毒液体,呈四面体构型。熔点25℃,沸点42℃。四羰基镍的晶体类型是(4)铑掺杂SrTiO3形成的催化剂,在光催化CO2还原反应中有很高的催化效率。SrTiO3的晶胞结构如图所示。其中Sr2+位于晶胞的体心,当有1%的Ti4+被Rh3+替代后,晶体中会失去部分O2-产生缺陷,此时平均每个晶胞所含O2-数目为

您最近半年使用:0次
2024-04-03更新
|
232次组卷
|
2卷引用:宁夏银川市银川一中2024届高三一模理综-化学试题
名校
解题方法
7 .  能形成结构式如图所示的离子。所含的4种元素位于主族,在每个短周期均有分布,
能形成结构式如图所示的离子。所含的4种元素位于主族,在每个短周期均有分布, 和
和 同族,
同族, 和
和 同周期。
同周期。 的
的 轨道有2个未成对电子,下列说法正确的是
轨道有2个未成对电子,下列说法正确的是
 能形成结构式如图所示的离子。所含的4种元素位于主族,在每个短周期均有分布,
能形成结构式如图所示的离子。所含的4种元素位于主族,在每个短周期均有分布, 和
和 同族,
同族, 和
和 同周期。
同周期。 的
的 轨道有2个未成对电子,下列说法正确的是
轨道有2个未成对电子,下列说法正确的是
A.元素电负性: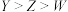 | B.原子半径: |
C.最简单氢化物沸点: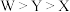 | D. 和 和 中 中 的杂化轨道类型相同 的杂化轨道类型相同 |
您最近半年使用:0次
2024-04-02更新
|
521次组卷
|
3卷引用:宁夏吴忠市青铜峡市宁朔中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
8 . X、Y、Z、W四种短周期主族元素的原子序数依次增大。其中仅有X、Y与Z位于同一周期,且只有X、Y元素相邻。基态X原子核外有2个未成对电子,W原子的原子半径在同周期中最大。下列说法正确的是
| A.最简单氢化物沸点:X>Y | B.第一电离能:Y>Z>X |
| C.电负性:Z>Y>X>W | D.X、Y、Z均有对应的最高价含氧酸 |
您最近半年使用:0次
2024-04-02更新
|
195次组卷
|
2卷引用:宁夏吴忠市青铜峡市宁朔中学2023-2024学年高二下学期3月月考化学试题
9 . 下列四种元素中,单质氧化性最强的是
| A.原子中p能级有3个电子的元素 |
| B.原子最外层电子排布为2s22p5的元素 |
| C.原子核外电子排布为[Ne]3s23p5的元素 |
| D.位于周期表中第三周期ⅢA族的元素 |
您最近半年使用:0次
名校
解题方法
10 . 2023年诺贝尔化学奖颁给合成量子点的三位科学家。量子点是一种重要的低维半导体材料,常由硅(Si)、磷(P)、硫(S)、硒(Se)等元素组成。下列说法正确的是
| A.原子半径:r(Si)>r(S)>r(Se) |
| B.电负性:χ(Se)>χ(S)>χ(Si) |
| C.第一电离能:I1(P)>I1(S)>I1(Si) |
| D.氢化物的稳定性:H2Se>H2S>PH3 |
您最近半年使用:0次
2024-01-20更新
|
199次组卷
|
3卷引用:宁夏吴忠市青铜峡市宁朔中学2023-2024学年高二下学期3月月考化学试题



