1 . 某液晶分子结构如图所示,X、Y、Z、W为原子序数依次增大的短周期非金属元素,基态X原子的电子只有一种自旋取向,基态W原子核外s能级上的电子总数与p能级上的电子总数相等,Y与W的质子数之和等于Z的质子数的2倍。下列说法错误的是
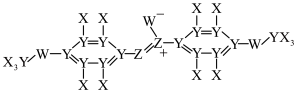
| A.电负性:W>Z>Y | B.第一电离能:Z>W>Y |
| C.常见单质分子键能:X>W>Z | D.简单氢化物沸点:W>Z>Y |
您最近半年使用:0次
名校
2 . 推理是一种重要的思维方法。下列推理合理的是
| 已知 | 推论 | |
| A. | 电负性: | 键能: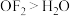 |
| B. | 键能: | 酸性: |
| C. | 溶解性: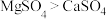 | 溶解性: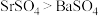 |
| D. | 极性: | 极性: |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
3 .  是宇宙中最丰富的元素,
是宇宙中最丰富的元素, 位于第四周期且基态原子中有5个未成对电子,基态
位于第四周期且基态原子中有5个未成对电子,基态 原子的
原子的 能级与
能级与 能级的电子数相等,
能级的电子数相等,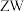 是
是 的等电子体,四种元素形成的配合物
的等电子体,四种元素形成的配合物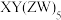 结构如下图所示,下列说法错误的是
结构如下图所示,下列说法错误的是
 是宇宙中最丰富的元素,
是宇宙中最丰富的元素, 位于第四周期且基态原子中有5个未成对电子,基态
位于第四周期且基态原子中有5个未成对电子,基态 原子的
原子的 能级与
能级与 能级的电子数相等,
能级的电子数相等,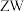 是
是 的等电子体,四种元素形成的配合物
的等电子体,四种元素形成的配合物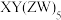 结构如下图所示,下列说法错误的是
结构如下图所示,下列说法错误的是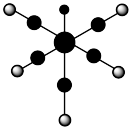
A.第一电离能: | B.电负性: |
| C.配体ZW中配位原子为Z | D.Y的最高价氧化物为碱性氧化物 |
您最近半年使用:0次
2024-04-11更新
|
325次组卷
|
2卷引用:湖北省圆创联盟2024届高三三月联合测评(一模)化学试卷
解题方法
4 . 推理是一种重要的思维方法。下列推理合理的是
| 已知 | 推论 | |
| A | 电负性:F>O>H | 键角:OF2>H2O |
| B | 键能:H-Cl>H-Br | 酸性:HCl>HBr |
| C | 溶解性:MgSO4>CaSO4 | 溶解性:SrSO4>BaSO4 |
| D | 极性:NH3>PH3 | 极性:NCl3>PCl3 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . 氨硼烷(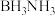 )是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下:
)是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下: 。下列说法错误的是
。下列说法错误的是
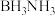 )是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下:
)是一种重要的储氢材料。1955年,Shore和Parry首次合成出氨硼烷。其反应如下: 。下列说法错误的是
。下列说法错误的是A.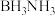 和 和 中均含有配位键 中均含有配位键 |
B.基态N原子核外价层电子排布图: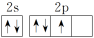 |
| C.上述反应涉及的第二周期元素中,电负性最大的是N |
D. 和 和 中, 中, 与 与 具有相似的空间结构 具有相似的空间结构 |
您最近半年使用:0次
2024-04-07更新
|
338次组卷
|
4卷引用:湖北省九师联盟2024届高三下学期3月质量检测(W-G)化学试卷
名校
解题方法
6 . 石灰氮(CaCN2)是一种氮素肥效长的固态肥料,同时也是一种低毒、无残留的农药。工业上合成方法之一为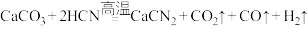 。回答下列问题:
。回答下列问题:
(1)已知Sn和C同主族,Sn的原子序数为50,基态Sn原子的价层电子排布图为_______ ,沸点比较:CH4_______ SnH4(填>、=、<),理由是:_______ 。
(2)N原子核外不同运动状态的电子有_______ 种;下列状态的氮中再失去一个电子所需能量最大的是_______ 。
A. [He]2s22p3 B. [He]2s22p13s1 C. [He]2s22p33s1 D. [He]2s22p2
(3)上述制备反应涉及到元素及化合物中属于非极性分子的有_______ ,电负性最大的元素是_______ 。
(4)固态CO2俗称干冰,干冰中的作用力有_______ 。
①范德华力 ②离子键 ③共价键 ④非极性键
(5)已知等电子原理是指原子总数相同、价电子总数相同的分子或离子具有相同的结构特征,其性质相近。这样的粒子互称为等电子体,例如CO和N2互为等电子体,请写出CO的电子式:_______ 。
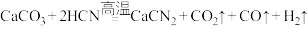 。回答下列问题:
。回答下列问题:(1)已知Sn和C同主族,Sn的原子序数为50,基态Sn原子的价层电子排布图为
(2)N原子核外不同运动状态的电子有
A. [He]2s22p3 B. [He]2s22p13s1 C. [He]2s22p33s1 D. [He]2s22p2
(3)上述制备反应涉及到元素及化合物中属于非极性分子的有
(4)固态CO2俗称干冰,干冰中的作用力有
①范德华力 ②离子键 ③共价键 ④非极性键
(5)已知等电子原理是指原子总数相同、价电子总数相同的分子或离子具有相同的结构特征,其性质相近。这样的粒子互称为等电子体,例如CO和N2互为等电子体,请写出CO的电子式:
您最近半年使用:0次
解题方法
7 . X、Y、Z、W是原子序数依次增大的短周期主族元素,X原子有两个单电子且电负性是四种元素中最大的,Y原子的最外层电子数是X原子内层电子数的2倍,Z原子s能级上电子数与p能级上电子数之比为2:3,W第一电离能大于Z。下列说法正确的是
| A.电负性:Y<Z<W |
| B.原子半径:X<Z<W<Y |
| C.四种元素基态原子的未成对电子数:Y<Z<W |
| D.简单氢化物的稳定性:Z<Y<W<X |
您最近半年使用:0次
2024-04-02更新
|
216次组卷
|
2卷引用:2024届湖北省十一校高三下学期第二次联考化学试卷
名校
8 . 某种离子液体的结构如图示,X、Y、Z、M、R为原子序数依次增大的短周期元素,Z的质子数等于X、Y的质子数之和,R为电负性最大的元素。下列说法正确的是
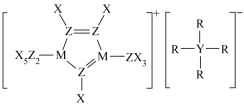
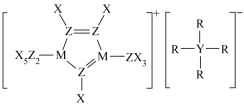
| A.Y的电负性大于Z |
| B.M、X形成的化合物分子间易形成氢键 |
| C.阴离子的空间构型为平面四边形 |
| D.分子的极性:MR3<YR3 |
您最近半年使用:0次
名校
9 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(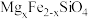 )。回答下列问题:
)。回答下列问题:
(1)基态 原子的价电子排布式为
原子的价电子排布式为___________ 。橄榄石中,各元素电负性由大到小的顺序为___________ 。
(2)已知一些物质的熔点数据如下表:
① 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是___________ 。
②分析同族元素的氯化物 、
、 、
、 熔点变化趋势的原因
熔点变化趋势的原因___________ 。 的空间结构为
的空间结构为___________ ,其中 的轨道杂化形式为
的轨道杂化形式为___________ 。
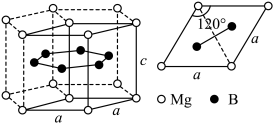
(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有___________ 个 。该物质化学式为
。该物质化学式为___________ ,B-B最近距离为___________ 。
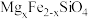 )。回答下列问题:
)。回答下列问题:(1)基态
 原子的价电子排布式为
原子的价电子排布式为(2)已知一些物质的熔点数据如下表:
| 物质 | NaCl | SiCl4 | GeCl4 | SnCl4 |
| 熔点/℃ | 800.7 | -68.8 | -51.5 | -34.1 |
 与
与 均为第三周期元素,
均为第三周期元素, 熔点明显高于
熔点明显高于 ,原因是
,原因是②分析同族元素的氯化物
 、
、 、
、 熔点变化趋势的原因
熔点变化趋势的原因 的空间结构为
的空间结构为 的轨道杂化形式为
的轨道杂化形式为(3)一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示,晶胞中含有
 。该物质化学式为
。该物质化学式为
您最近半年使用:0次
10 . 天然气的无机成因说十分诱人。据称,地幔主成分之一的橄榄石与水和 反应可生成
反应可生成 ,反应可表示为
,反应可表示为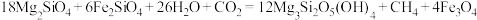 。下列说法错误的是
。下列说法错误的是
 反应可生成
反应可生成 ,反应可表示为
,反应可表示为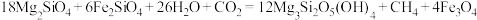 。下列说法错误的是
。下列说法错误的是A.电负性: | B. 的空间结构为正四面体形 的空间结构为正四面体形 |
C.沸点: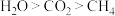 | D.基态 原子核外存在15种能量不同的电子 原子核外存在15种能量不同的电子 |
您最近半年使用:0次



