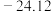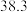1 . 某元素基态原子的电子排布式为
 。下列描述中,正确的是
。下列描述中,正确的是

 。下列描述中,正确的是
。下列描述中,正确的是| A.该元素的电负性比溴元素的电负性大 |
| B.该元素位于元素周期表VA族 |
| C.4p能级上的3个电子能量相等,但自旋状态不同 |
| D.该元素的原子有5个价电子 |
您最近半年使用:0次
7日内更新
|
51次组卷
|
2卷引用:上海交通大学附属中学2023-2024学年高二下学期期中考试化学试题
解题方法
2 . 尿素 可与正烷烃形成超分子,原理如图所示。下列说法错误的是
可与正烷烃形成超分子,原理如图所示。下列说法错误的是
 可与正烷烃形成超分子,原理如图所示。下列说法错误的是
可与正烷烃形成超分子,原理如图所示。下列说法错误的是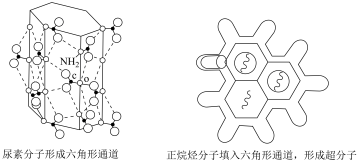
| A.尿素分子中各元素的电负性:O>N>C>H |
| B.尿素分子通过分子间氢键形成六角形通道结构 |
| C.依据分子直径的大小差异可分离同碳数正烷烃和支链烷烃 |
| D.该超分子能稳定存在的原因是尿素分子和正烷烃分子通过共价键结合使能量降低、熵减小 |
您最近半年使用:0次
2024-04-18更新
|
95次组卷
|
2卷引用:2024届“3+3+3”高考备考诊断性联考卷(二)理科综合试题-高中化学
3 . 硅是电子工业的重要材料。利用石英砂(主要成分为 )和镁粉模拟工业制硅的流程示意图如下。
)和镁粉模拟工业制硅的流程示意图如下。
已知:电负性:
 )和镁粉模拟工业制硅的流程示意图如下。
)和镁粉模拟工业制硅的流程示意图如下。已知:电负性:


| A.I中引燃时用镁条,利用了镁条燃烧放出大量的热 |
B.Ⅱ中主要反应有: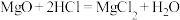 、 、 |
C.为防止 自燃,Ⅱ需隔绝空气 自燃,Ⅱ需隔绝空气 |
| D.过程中含硅元素的物质只体现氧化性 |
您最近半年使用:0次
2024·吉林·三模
4 . 冠醚因分子结构形如皇冠而得名,某冠醚分子c可识别K+,其合成方法如下。下列说法错误的是
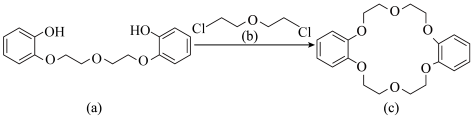
| A.(a)能与浓溴水发生取代反应 |
| B.(b)中各元素电负性大小关系为:O>Cl>C>H |
| C.(c)的一氯代物有3种 |
| D.(c)可增加KI在苯中的溶解度 |
您最近半年使用:0次
5 . 邻二氮菲能与Fe2+发生显色反应,生成橙红色螯合物,用于Fe2+检验,化学反应如下。下列说法正确的是
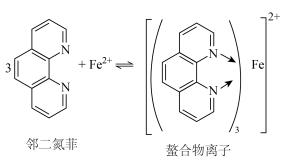
| A.邻二氮菲的核磁共振氢谱有6组吸收峰 |
| B.元素的电负性顺序:N>H>C>Fe |
| C.每个螯合物离子中含有2个配位键 |
| D.用邻二氮菲检验Fe2+时,需要调节合适的酸碱性环境 |
您最近半年使用:0次
2024-04-17更新
|
700次组卷
|
3卷引用:东北三省三校(哈师大附中、东北师大附中、辽宁省实验中学)2023-2024学年高三下学期第一次联合模拟考化学试卷
东北三省三校(哈师大附中、东北师大附中、辽宁省实验中学)2023-2024学年高三下学期第一次联合模拟考化学试卷河北省承德市部分高中2024届高三下学期二模化学试题(已下线)题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
6 . 某有机物在合成中具有重要作用,其分子结构如下图所示。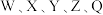 是核电荷数依次增大的短周期元素。
是核电荷数依次增大的短周期元素。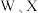 原子序数之和等于Y的原子序数,
原子序数之和等于Y的原子序数,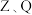 原子价电子数相同。下列说法
原子价电子数相同。下列说法错误 的是
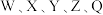 是核电荷数依次增大的短周期元素。
是核电荷数依次增大的短周期元素。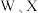 原子序数之和等于Y的原子序数,
原子序数之和等于Y的原子序数,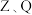 原子价电子数相同。下列说法
原子价电子数相同。下列说法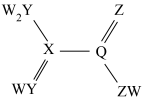
A. 元素的氢化物沸点最高的是Z 元素的氢化物沸点最高的是Z | B. 元素电负性最大的是Z 元素电负性最大的是Z |
| C.Q的最高价氧化物是酸性氧化物 | D.该有机物具有碱性 |
您最近半年使用:0次
2024·山东淄博·一模
名校
7 . X、Y、Z、W为原子序数依次增大的短周期元素,基态Y原子的s能级电子数是p能级的2倍,基态W原子的电子总数是其最高能级电子数的2倍,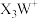 是10电子微粒,可形成离子液体
是10电子微粒,可形成离子液体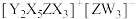 。下列说法正确的是
。下列说法正确的是
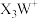 是10电子微粒,可形成离子液体
是10电子微粒,可形成离子液体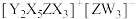 。下列说法正确的是
。下列说法正确的是| A.第一电离能:Y<W<Z | B. 与 与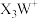 的空间结构相同 的空间结构相同 |
C.键能: | D. 中存在 中存在 键、氢键和配位键 键、氢键和配位键 |
您最近半年使用:0次
2024-04-17更新
|
576次组卷
|
3卷引用:题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)
(已下线)题型5 物质结构与性质 有机物的结构与性质(25题)-2024年高考化学常考点必杀300题(新高考通用)四川省射洪中学校2023-2024学年高二下学期4月月考化学试题山东省淄博市2024届高三一模化学试题
8 . 短周期主族元素X、Y、Z、W、Q原子序数依次增大,其中Q是元素周期表中电负性最大的元素,由这五种元素组成的某药物结构如图所示。下列有关说法正确的是

A.电负性: |
B.第一电离能: |
| C.该分子中所有原子都满足8电子稳定结构 |
D.基态Z原子电子轨道表示式为: |
您最近半年使用:0次
名校
解题方法
9 . 钙钛矿( )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
Ⅰ. 为制备
为制备 的一种原料。
的一种原料。
(1)Ti的四卤化物熔点如下表所示, 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是______ 。
Ⅱ.一类有机一无机杂化材料 具有与
具有与 相同的晶体结构。
相同的晶体结构。
(2)①有机阳离子 中C原子和N原子的电负性大小比较:C
中C原子和N原子的电负性大小比较:C______ N(填“ ”、“
”、“ ”或“
”或“ ”),从原子结构的角度说明理由
”),从原子结构的角度说明理由______ 。
②若将晶胞中的A坐标定义为 ,B坐标定义为
,B坐标定义为 ,则离A最近的微粒的坐标为
,则离A最近的微粒的坐标为______ (任写其一)。若将晶胞中心微粒的坐标定义为 ,则与其紧邻的
,则与其紧邻的 的坐标为
的坐标为______ (任写其一)。 键角大小比较:
键角大小比较:
______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是______ 。
(3) 晶体生长过程中容易产生晶体缺陷,造成
晶体生长过程中容易产生晶体缺陷,造成 空位。用
空位。用 替换
替换 可改善这种情况的可能原因是
可改善这种情况的可能原因是______ 。
 )型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:
)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料。回答下列问题:Ⅰ.
 为制备
为制备 的一种原料。
的一种原料。(1)Ti的四卤化物熔点如下表所示,
 熔点高于其他三种卤化物,自
熔点高于其他三种卤化物,自 至
至 熔点依次升高,原因是
熔点依次升高,原因是化合物 |
|
|
|
|
熔点 | 377 |
|
| 155 |
Ⅱ.一类有机一无机杂化材料
 具有与
具有与 相同的晶体结构。
相同的晶体结构。(2)①有机阳离子
 中C原子和N原子的电负性大小比较:C
中C原子和N原子的电负性大小比较:C ”、“
”、“ ”或“
”或“ ”),从原子结构的角度说明理由
”),从原子结构的角度说明理由②若将晶胞中的A坐标定义为
 ,B坐标定义为
,B坐标定义为 ,则离A最近的微粒的坐标为
,则离A最近的微粒的坐标为 ,则与其紧邻的
,则与其紧邻的 的坐标为
的坐标为
 键角大小比较:
键角大小比较:
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是(3)
 晶体生长过程中容易产生晶体缺陷,造成
晶体生长过程中容易产生晶体缺陷,造成 空位。用
空位。用 替换
替换 可改善这种情况的可能原因是
可改善这种情况的可能原因是
您最近半年使用:0次
2024·贵州黔西·一模
10 . 根据表中短周期元素的有关信息判断,下列说法错误的是
元素编号 | E | F | G | H | I | J | K | L |
原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.160 | 0.186 |
| 最高化合价或最低化合价 |
|
|
|
|
|
|
|
|
| A.电负性大小:F>H>I |
| B.简单离子半径:K>F>L |
| C.第一电离能:K>J>L |
| D.L、K、J的最高价氧化物对应水化物碱性逐渐减弱 |
您最近半年使用:0次