23-24高三上·北京顺义·阶段练习
名校
1 . 下列事实不能 用元素周期律解释的是
| A.电负性:N<O<F | B.酸性:H2SiO3<H2SO3<HClO4 |
| C.稳定性:HI<HBr<HCl | D.碱性:Al(OH)3<Mg(OH)2<NaOH |
您最近半年使用:0次
2023-10-17更新
|
220次组卷
|
3卷引用:选择题1-5
2023·山东·高考真题
真题
解题方法
2 . 三氯甲硅烷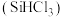 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,熔点为 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
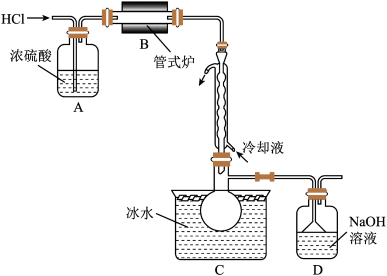
(1)制备 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为_____ ;判断制备反应结束的实验现象是_____ 。图示装置存在的两处缺陷是_____ 。
(2)已知电负性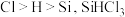 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为_____ 。
(3)采用如下方法测定溶有少量 的
的 纯度。
纯度。
 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____ ,②_____ (填操作名称),③称量等操作,测得所得固体氧化物质量为 ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为_____ (填标号)。测得样品纯度为_____ (用含 、
、 的代数式表示)。
的代数式表示)。

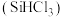 是制取高纯硅的重要原料,常温下为无色液体,沸点为
是制取高纯硅的重要原料,常温下为无色液体,沸点为 ,熔点为
,熔点为 ,易水解。实验室根据反应
,易水解。实验室根据反应 ,利用如下装置制备
,利用如下装置制备 粗品(加热及夹持装置略)。回答下列问题:
粗品(加热及夹持装置略)。回答下列问题:
(1)制备
 时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入
时进行操作:(ⅰ)……;(ⅱ)将盛有硅粉的瓷舟置于管式炉中;(ⅲ)通入 ,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为
,一段时间后接通冷凝装置,加热开始反应。操作(ⅰ)为(2)已知电负性
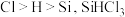 在浓
在浓 溶液中发生反应的化学方程式为
溶液中发生反应的化学方程式为(3)采用如下方法测定溶有少量
 的
的 纯度。
纯度。 样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①
样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:① ,从下列仪器中选出①、②中需使用的仪器,依次为
,从下列仪器中选出①、②中需使用的仪器,依次为 、
、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
2023-06-19更新
|
10365次组卷
|
16卷引用:T26-工业流程题
(已下线)T26-工业流程题(已下线)2023年高考山东卷化学真题变式题(实验综合题)(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)考点12 硅及其无机非金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第10讲 硅及其化合物(已下线)专题15 化学实验综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点13 硅及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点46 定量分析实验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2023年高考山东卷化学真题(已下线)第18练 化学实验综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)2024届河北省实验中学高三年级上学期第一次月考化学试题
2023·北京东城·模拟预测
名校
解题方法
3 . 重金属元素具有毒性,常用含巯基(-SH)的有机化合物作为解毒剂。例如,解毒剂化合物I与氧化汞生成化合物II。
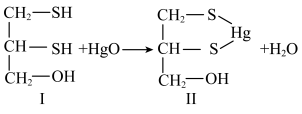
(1)汞的原子序数为80,位于元素周期表第___________ 周期第IIB族。
(2)基态硫原子价电子排布式为___________ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为___________ 。
(4)化合物III也是一种汞解毒剂。下列说法正确的是___________。

(5)理论预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
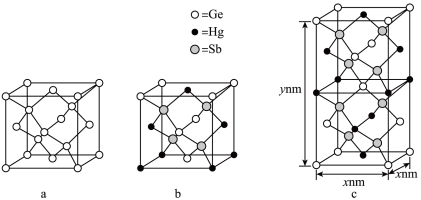
①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是___________ 。
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_______ ;该晶胞中粒子个数比Hg:Ge:Sb = _______ 。
③设X的最简式的式量为M,阿伏加德罗常数为NA.则X晶体的密度为______ g/cm3(列出算式)。

(1)汞的原子序数为80,位于元素周期表第
(2)基态硫原子价电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)化合物III也是一种汞解毒剂。下列说法正确的是___________。

| A.在I中,O和S原子都采取sp3杂化 |
| B.在II中S元素的电负性最大,更易与Hg结合成键 |
| C.在III中,C-C-C键角是180° |
| D.与化合物I相比,III的水溶性更好 |

①图b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是
②图c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为
③设X的最简式的式量为M,阿伏加德罗常数为NA.则X晶体的密度为
您最近半年使用:0次
22-23高二下·黑龙江哈尔滨·期中
名校
解题方法
4 . 解释下列现象的原因不正确的是
| 选项 | 现象 | 原因 |
| A |  中含有共价键 中含有共价键 | Al与Cl元素间的电负性差值小于1.7 |
| B | 碘在 中的溶解度比在水中大 中的溶解度比在水中大 | 碘和 均为非极性分子,水是极性分子 均为非极性分子,水是极性分子 |
| C | 对羟基苯甲醛的熔沸点比邻羟基苯甲醛的高 | 对羟基苯甲醛形成分子间氢键,而邻羟基苯甲醛形成分子内氢键 |
| D | HF的稳定性强于HCl | HF分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023·北京房山·二模
解题方法
5 . 下列关于第ⅣA族元素及其化合物的性质比较中,不正确 的是
| A.原子半径:C<Si<Ge |
| B.电负性:C<Si<Ge |
C.热稳定性: |
D.酸性: |
您最近半年使用:0次
22-23高二下·重庆·期中
6 . 下列结论与解释不匹配的是
| 选项 | 结论 | 解释 |
| A | CH4的稳定性强于SiH4的 | C-H键键长比Si-H键的短,C-H键键能更大 |
| B | 冰中1个水分子周围只有4个紧邻分子 | 水分子之间存在氢键,氢键具有方向性 |
| C | 氟乙酸的酸性强于氯乙酸的 | 氟的电负性大于氯的电负性 |
| D | CH3CH2OH的沸点比CH3OCH3的沸点高 | CH3CH2OH是极性分子,CH3OCH3是非极性分子 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-04-30更新
|
320次组卷
|
3卷引用:2023年北京卷高考真题变式题(选择题6-10)
22-23高二下·河北唐山·期中
名校
7 . 下列对一些事实的理论解释正确的是
| 选项 | 事实 | 理论解释 |
| A | 硫酸铵晶体中存在氢键 |  中的H与 中的H与 中的O之间的作用力大小在范德华力和共价键之间 中的O之间的作用力大小在范德华力和共价键之间 |
| B | 熔融NaCl可以导电 | 熔融态NaCl中有自由移动的电子 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是共价晶体 |
| D | HF的沸点高于HCl | F的电负性大于Cl |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-04-29更新
|
155次组卷
|
3卷引用:2023年北京卷高考真题变式题(选择题6-10)
(已下线)2023年北京卷高考真题变式题(选择题6-10)河北省唐山市十县一中联盟2022-2023学年高二下学期期中考试化学试题江西省高安市灰埠中学2022-2023学年高二下学期5月期中考试化学试题
22-23高二下·北京顺义·期中
解题方法
8 . 下列对物质性质的解释不合理的是
选项 | 性质 | 解释 |
A | 熔点:晶体硅>白磷 | 晶体硅属于共价晶体、白磷属于分子晶体 |
B | 密度:干冰>冰 |  的分子量大于 的分子量大于 的,干冰中分子采取密堆积排列,冰中分子采取非密堆积排列 的,干冰中分子采取密堆积排列,冰中分子采取非密堆积排列 |
C | 酸性: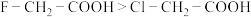 | 电负性: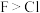 |
D | 氧化性: | 键能: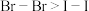 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
21-22高二下·北京昌平·期末
名校
解题方法
9 . 对下列事实的解释不正确 的是
| 选项 | 事实 | 解释 |
| A | 金属银具有良好的导电性 | 金属银中有“自由电子” |
| B | ICl中I表现为正价 | 电负性:Cl>I |
| C | 碘易溶于四氯化碳 | 碘分子和四氯化碳分子都是非极性分子 |
| D | Cl2、Br2、I2的熔沸点依次升高 | Cl2、Br2、I2中共价键强度依次减小 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-04-26更新
|
184次组卷
|
5卷引用:2023年北京卷高考真题变式题(选择题6-10)
22-23高二下·浙江·期中
名校
解题方法
10 . 下列对有关事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 酸性:CF3COOH>CCl3COOH | 氟的电负性大于氯的电负性 |
| B | O3在水中的溶解度比O2大 | O3是极性分子,O2是非极性分子 |
| C | 水晶在不同方向上导热性不同 | 晶体具有各向异性的特点 |
| D | 水的沸点比乙醇的沸点高 | 水分子间存在氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



