名校
解题方法
1 . 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+原子核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)E元素在周期表中的位置为_______ ,属于_______ 区。
(2)B、C、D三种元素的第一电离能最大的是_______ (填元素符号),第一电离能最大的原因是_______ 。
(3)D元素与氟元素相比,电负性:D_______ F(填“>”“=”或“<”),下列表述中能证明这一事实的是_______ (填字母)。
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物CA5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,其电子式为_______ 。
(1)E元素在周期表中的位置为
(2)B、C、D三种元素的第一电离能最大的是
(3)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物CA5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,其电子式为
您最近半年使用:0次
2022-08-28更新
|
306次组卷
|
3卷引用:四川省眉山北外附属东坡外国语学校2023-2024学年高二下学期开学化学试题
名校
解题方法
2 . 某种合成医药、农药的中间体W结构如图所示,其中X、Y、Z、M、R均为短周期元素,原子序数依次增大。下列说法错误的是
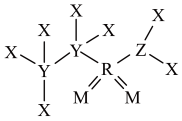
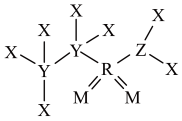
| A.简单氢化物沸点:Y<Z | B.电负性:M>Z>Y |
| C.第一电离能:Y<Z<M | D.W分子中R的杂化方式为sp3 |
您最近半年使用:0次
名校
3 . 下列说法中正确的是
| A.电子云图中的小黑点密表示该核外空间的电子多 |
B.电子排布式 违反了洪特规则 违反了洪特规则 |
| C.原子序数为7、8、9的三种元素,其第一电离能和电负性均依次增大 |
| D.电子仅由激发态跃迁到基态时才会产生原子光谱 |
您最近半年使用:0次
2024-04-04更新
|
197次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高二下学期开学化学试题
名校
4 . 下列有关说法中合理的是
A.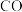 与 与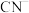 结构相似,含有的 结构相似,含有的 键与 键与 键个数比均为1∶2 键个数比均为1∶2 |
B.根据 理论可知 理论可知 、 、 、 、 分子内键角依次减小 分子内键角依次减小 |
| C.铜的电负性为1.9,氯的电负性为3.0,氯化铜为离子化合物,溶于水能完全电离 |
| D.元素周期表中第ⅠA族和第ⅦA族元素原子间不可能形成共价键 |
您最近半年使用:0次
2024-04-03更新
|
243次组卷
|
2卷引用:黑龙江省齐齐哈尔市讷河市第一中学2023-2024学年高二下学期开学考试化学试题
名校
5 . 下列与分子性质有关的说法正确的是
| A.氟代丙二酸(HOOC—CF2—COOH)的酸性强于丙二酸(HOOC—CH2—COOH)是因为—CF2—的极性大于—CH2—的极性,导致氟代丙二酸羧基中—OH的极性更大更易电离出H+ |
B.邻硝基苯酚(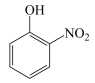 )的沸点高于对硝基苯酚( )的沸点高于对硝基苯酚(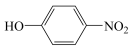 )是因为后者形成了分子间氢键 )是因为后者形成了分子间氢键 |
| C.C的电负性强于Si,所以CH4的熔沸点高于SiH4 |
| D.I2受热易升华,是因为分子内共价键键能较小所致 |
您最近半年使用:0次
名校
解题方法
6 . 某种离子液体的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与Q同主族。下列说法错误的是


| A.简单离子半径:Q>Z>W | B.简单氢化物键角:Y>Z>Q |
| C.最高价氧化物对应水化物的酸性:Z<Q | D.元素的电负性:Z>Y>X |
您最近半年使用:0次
名校
解题方法
7 . 中国科学家首次在月球上发现新矿物,并将其命名为“嫦娥石 ”。Y(钇)是金属元素。下列说法
”。Y(钇)是金属元素。下列说法
A.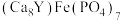 是一种磷酸盐 是一种磷酸盐 |
| B.电负性O>P,嫦娥石中P显正价,O显负价 |
| C.在元素周期表中,O、P、Fe均属于s区元素 |
| D.原子半径:O<P |
您最近半年使用:0次
2024-03-24更新
|
209次组卷
|
3卷引用:北京市第九中学2023-2024学年高二下学期2月开学考化学试题
8 . 已知 、
、 、
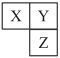
、 三种短周期元素在周期表中的相对位置如图所示,
三种短周期元素在周期表中的相对位置如图所示, 基态原子
基态原子 能级和
能级和 能级的电子数相等,下列说法错误的是
能级的电子数相等,下列说法错误的是
 、
、 、
、 三种短周期元素在周期表中的相对位置如图所示,
三种短周期元素在周期表中的相对位置如图所示, 基态原子
基态原子 能级和
能级和 能级的电子数相等,下列说法错误的是
能级的电子数相等,下列说法错误的是
A.在三种元素形成的气态氢化物中, 的气态氢化物最稳定 的气态氢化物最稳定 |
B.简单氢化物的沸点: |
C.三种元素原子半径的大小顺序: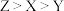 |
D. 、 、 元素原子的电负性: 元素原子的电负性: , , 元素原子的第一电离能: 元素原子的第一电离能: |
您最近半年使用:0次
名校
9 . 下列说法不正确的是
A.HClO分子空间构型为直线形,沸点: > >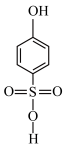 |
| B.NCl3和PCl3分子中,电负性:N>P,键角:∠Cl-N-Cl>∠Cl-P-Cl |
| C.Mg原子的两种激发态[Ne]3s13p1和[Ne]3p2中,前者第二电离能更大 |
| D.O3是空间结构为V形的弱极性分子,水中的溶解度大于O2,基态S原子核外电子的空间运动状态有9种 |
您最近半年使用:0次
名校
解题方法
10 . 某种镁盐具有良好的电化学性能,其阴离子结构如下图所示。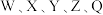 是核电荷数依次增大的短周期元素,
是核电荷数依次增大的短周期元素,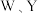 原子序数之和等于
原子序数之和等于 原子价电子数是Q原子价电子数的2倍。下列说法错误的是
原子价电子数是Q原子价电子数的2倍。下列说法错误的是
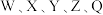 是核电荷数依次增大的短周期元素,
是核电荷数依次增大的短周期元素,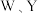 原子序数之和等于
原子序数之和等于 原子价电子数是Q原子价电子数的2倍。下列说法错误的是
原子价电子数是Q原子价电子数的2倍。下列说法错误的是
| A.Q和Z的基态原子核外未成对电子数相同 | B.电负性大小: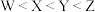 |
| C.Q的氯化物为离子晶体 | D.沸点: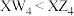 |
您最近半年使用:0次
2024-03-08更新
|
559次组卷
|
4卷引用:辽宁省铁岭市调兵山市第二高级中学2023-2024学年高二下学期开学考试化学试题



