1 . 中国科学院化学研究所有机固体院重点实验室合成了适用于非卤溶剂加工的“巨分子受体”,对于推动聚合物太阳电池受体光伏材料的发展具有重要意义。目前可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1) 在元素周期表中的位置为
在元素周期表中的位置为_______ ,其基态原子有_______ 种不同运动状态的电子。
(2)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为_______ ,其核外电子占据的最高能级的电子云轮廓图为_______ 。
(3)第一电子亲和能 是指基态的气态原子得到一个电子形成气态
是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
_______ (填“ ”或“
”或“ ”)
”)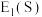 。
。
(4) 和
和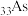 (与
(与 同主族)两种元素中第一电离能较大的是
同主族)两种元素中第一电离能较大的是_______ (填元素符号),试解释其原因:_______ 。
(5)根据对角线规则可知, 与铝在性质上具有相似性。已知
与铝在性质上具有相似性。已知 ,
, 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
(1)
 在元素周期表中的位置为
在元素周期表中的位置为(2)Te位于元素周期表第五周期第ⅥA族,其基态原子的价层电子轨道表示式为
(3)第一电子亲和能
 是指基态的气态原子得到一个电子形成气态
是指基态的气态原子得到一个电子形成气态 价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
价离子时所放出的热量。元素的电子亲和能越大,表示原子得到电子的倾向越大,电负性一般也越大。则
 ”或“
”或“ ”)
”)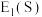 。
。(4)
 和
和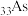 (与
(与 同主族)两种元素中第一电离能较大的是
同主族)两种元素中第一电离能较大的是(5)根据对角线规则可知,
 与铝在性质上具有相似性。已知
与铝在性质上具有相似性。已知 ,
, 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为
您最近半年使用:0次
2 . X、Y、Z、M、N是原子序数依次增大的5种短周期主族元素,其元素性质或原子结构如表,下列说法正确的是
| 元素 | 元素性质或原子结构 |
 | 电子只有一种自旋取向 |
 | 基态原子核外价层电子排布满足 |
 | 基态原子核外 能级上的电子总数与 能级上的电子总数与 能级上的电子总数相等 能级上的电子总数相等 |
 | 与基态 原子的价层电子数相同 原子的价层电子数相同 |
 | 基态原子核外只有一个未成对电子 |
A.电负性: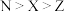 |
B.简单离子半径: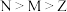 |
C. 的第一电离能高于同周期相邻元素 的第一电离能高于同周期相邻元素 |
D. 与 与 能形成两种化合物,且所有原子均满足8电子稳定结构 能形成两种化合物,且所有原子均满足8电子稳定结构 |
您最近半年使用:0次
3 . 四川简称“川”或“蜀”,古就有“天府之国”之美誉,是中国西部门户,大熊猫的故乡。下列说法正确的是
| A.宜宾长江大桥在江水中的钢铁部分主要发生电化学腐蚀 |
| B.三星堆出土的斧形金器中,Au电负性大于1.8 |
| C.制作开元米粉的酱油属于弱电解质 |
D.攀枝花的钛探明储量居世界第一位,基态 原子的价层电子排布式为 原子的价层电子排布式为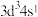 |
您最近半年使用:0次
名校
解题方法
4 . 某种合成医药、农药的中间体W结构如图所示,其中X、Y、Z、M、R均为短周期元素,原子序数依次增大。下列说法错误的是
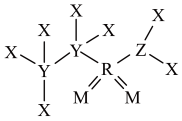
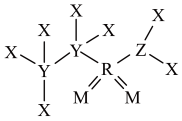
| A.简单氢化物沸点:Y<Z | B.电负性:M>Z>Y |
| C.第一电离能:Y<Z<M | D.W分子中R的杂化方式为sp3 |
您最近半年使用:0次
名校
5 . 在1778年,法国马厚比无意中发现用硫酸钠、木炭和铁(后改用氧化铁)一起灼烧,再用水滗取可得到纯碱。这一发明使他建立起世界上第一座纯碱工厂。
2Fe2O3+3NazSO4+16C Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+O2+2CO2 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3
回答下列问题:
(1)基态铁原子的价层电子排布式为_______ ,其3d能级上有_______ 个运动状态不同的电子。
(2)基态 原子核外有
原子核外有_______ 对自旋方向相反的电子对。基态钠原子核外电子占据能量最高的能级符号是_______ 。
(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是_______ (填化学式)。C、O、F三种元素中,电负性由大到小的顺序为_______ 。
(4)某同学书写的基态碳原子轨道表示式为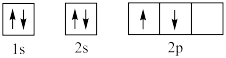 ,他违背了
,他违背了_______ 。
2Fe2O3+3NazSO4+16C
 Na6Fe4S3+ 14CO↑+2CO2↑
Na6Fe4S3+ 14CO↑+2CO2↑Na6Fe4S3+O2+2CO2
 Na2Fe4S3+2Na2CO3
Na2Fe4S3+2Na2CO3回答下列问题:
(1)基态铁原子的价层电子排布式为
(2)基态
 原子核外有
原子核外有(3)在氧、硫、钠、碳、铁元素中,金属性最强的元素与非金属性最强的元素组成的化合物是
(4)某同学书写的基态碳原子轨道表示式为
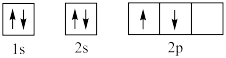 ,他违背了
,他违背了
您最近半年使用:0次
名校
6 . 短周期主族元素X、Y、Z、W的原子半径依次增大,且原子最外层电子数之和为15.基态Y原子的最外层电子数是其内层电子数的3倍,Y与Z同主族,Z与W同周期。下列说法正确的是
| A.简单氢化物的沸点:H2Z>H2Y |
| B.电负性由大到小的顺序是Y>Z>X |
| C.化合物WX2中既存在离子键,又存在共价键 |
| D.W元素基态原子核外M层电子的自旋状态相同 |
您最近半年使用:0次
名校
7 . 下列说法中正确的是
| A.电子云图中的小黑点密表示该核外空间的电子多 |
B.电子排布式 违反了洪特规则 违反了洪特规则 |
| C.原子序数为7、8、9的三种元素,其第一电离能和电负性均依次增大 |
| D.电子仅由激发态跃迁到基态时才会产生原子光谱 |
您最近半年使用:0次
2024-04-04更新
|
194次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高二下学期开学化学试题
名校
8 . 现有三种元素的基态原子的电子排布式如下:①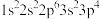 ;②
;②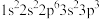 ;③
;③ 。则下列有关比较中正确的是
。则下列有关比较中正确的是
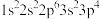 ;②
;②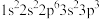 ;③
;③ 。则下列有关比较中正确的是
。则下列有关比较中正确的是A.简单氢化物的还原性: | B.电负性: |
C.阴离子半径: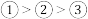 | D.第一电离能: |
您最近半年使用:0次
2024-04-03更新
|
245次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高二下学期开学化学试题
名校
解题方法
9 . 下列关于物质的结构或性质及解释都正确的是
选项 | 物质的结构或性质 | 解释 |
A | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH的羧基中O—H的极性更大 |
B | 熔点:SiO2>CO2 | 相对分子质量:SiO2大于CO2 |
C | O2与O3分子极性相同 | 二者都是由非极性键构成的分子 |
D | 沸点:对羟基苯甲醛>邻羟基苯甲醛 | 对羟基苯甲醛分子间范德华力更强 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-03更新
|
403次组卷
|
3卷引用:湖南省长郡中学2023-2024学年高二下学期寒假检测(开学考试)化学试题
名校
10 . 下列有关说法中合理的是
A.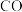 与 与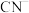 结构相似,含有的 结构相似,含有的 键与 键与 键个数比均为1∶2 键个数比均为1∶2 |
B.根据 理论可知 理论可知 、 、 、 、 分子内键角依次减小 分子内键角依次减小 |
| C.铜的电负性为1.9,氯的电负性为3.0,氯化铜为离子化合物,溶于水能完全电离 |
| D.元素周期表中第ⅠA族和第ⅦA族元素原子间不可能形成共价键 |
您最近半年使用:0次
2024-04-03更新
|
229次组卷
|
2卷引用:黑龙江省齐齐哈尔市讷河市第一中学2023-2024学年高二下学期开学考试化学试题



