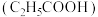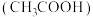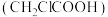23-24高二下·广东珠海·阶段练习
名校
解题方法
1 . 新冠肺炎疫情防控,消毒用品必不可少。试回答下列问题:
(1)过氧乙酸(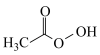 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有___________ ,分子中 键和
键和 键的个数比为
键的个数比为___________ 。
(2)生活中常用的手消毒凝胶,其主要有效成分是三氮羟基二苯醚和乙醇,其中三氯羟基二苯醚是一种广谱抗菌剂,高效、安全。三氯羟基二苯醚的结构简式如图所示。

①组成三氯羟基二苯醚的四种元素H、C、O、Cl的电负性从大到小的顺序为___________ ;基态氯原子的价电子排布图为___________ ,最高能级的原子轨道电子云轮廓图形状为___________ 。
②三氯羟基二苯醚的熔点:55~57℃,沸点:120℃,常态为白色或灰白色晶状粉末,稍有酚臭味,不溶于水,易溶于碱液和有机溶剂,三氯羟基二苯醚属于___________ 晶体。
③乙醇与甲醚 的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是
的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是___________ 。
(3)Na、K等活泼金属在 中燃烧得到的
中燃烧得到的 、
、 具有强氧化性,也常做消毒剂。已知
具有强氧化性,也常做消毒剂。已知 的晶胞如图所示:
的晶胞如图所示:
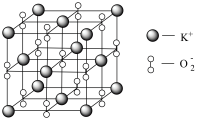
设阿伏加德罗常数的值为 ,晶胞的参数为a nm。晶胞的密度为
,晶胞的参数为a nm。晶胞的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)过氧乙酸(
 )也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有
)也是一种常用消毒剂。在过氧乙酸中碳原子的杂化方式有 键和
键和 键的个数比为
键的个数比为(2)生活中常用的手消毒凝胶,其主要有效成分是三氮羟基二苯醚和乙醇,其中三氯羟基二苯醚是一种广谱抗菌剂,高效、安全。三氯羟基二苯醚的结构简式如图所示。

①组成三氯羟基二苯醚的四种元素H、C、O、Cl的电负性从大到小的顺序为
②三氯羟基二苯醚的熔点:55~57℃,沸点:120℃,常态为白色或灰白色晶状粉末,稍有酚臭味,不溶于水,易溶于碱液和有机溶剂,三氯羟基二苯醚属于
③乙醇与甲醚
 的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是
的分子式相同,但二者的沸点分别为78.4℃、-24.8℃,乙醇沸点高于甲醚的原因是(3)Na、K等活泼金属在
 中燃烧得到的
中燃烧得到的 、
、 具有强氧化性,也常做消毒剂。已知
具有强氧化性,也常做消毒剂。已知 的晶胞如图所示:
的晶胞如图所示:
设阿伏加德罗常数的值为
 ,晶胞的参数为a nm。晶胞的密度为
,晶胞的参数为a nm。晶胞的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近半年使用:0次
23-24高二上·河北石家庄·期末
名校
2 . 光学性能优良的高分子材料聚础酸异山梨醇酯可由如下反应制备。
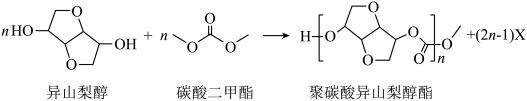
下列说法错误的是
| A.涉及元素的电负性:H<C<O | B.异山梨醇分子中有4个手性碳 |
| C.反应式中化合物X为甲醇 | D.异山梨醇中所有碳原子共平面 |
您最近半年使用:0次
23-24高三上·安徽合肥·阶段练习
名校
解题方法
3 . 某种还原剂可除去污垢、锈迹等,其主要成分为 。已知:W、X、Y、Z为原子序数依次增大的前20号主族元素,W、Z同主族且原子序数之和为20,Z为金属元素;基态X原子的3个能级上电子数相等,常温下Y的单质为气体,且X、Y原子的最外层电子数之和为10,下列说法正确的是
。已知:W、X、Y、Z为原子序数依次增大的前20号主族元素,W、Z同主族且原子序数之和为20,Z为金属元素;基态X原子的3个能级上电子数相等,常温下Y的单质为气体,且X、Y原子的最外层电子数之和为10,下列说法正确的是
 。已知:W、X、Y、Z为原子序数依次增大的前20号主族元素,W、Z同主族且原子序数之和为20,Z为金属元素;基态X原子的3个能级上电子数相等,常温下Y的单质为气体,且X、Y原子的最外层电子数之和为10,下列说法正确的是
。已知:W、X、Y、Z为原子序数依次增大的前20号主族元素,W、Z同主族且原子序数之和为20,Z为金属元素;基态X原子的3个能级上电子数相等,常温下Y的单质为气体,且X、Y原子的最外层电子数之和为10,下列说法正确的是| A.原子半径:Z>Y>X>W | B.电负性:Y>W>X>Z |
| C.Z与水剧烈反应,反应后溶液为红色 | D.Y分别与W、X、Z均能组成两种或两种以上的化合物 |
您最近半年使用:0次
2024-03-05更新
|
220次组卷
|
4卷引用:第一章 原子结构与性质(B卷)
23-24高二下·广东梅州·开学考试
名校
解题方法
4 . X、Y、Z、W均为短周期主族元素,原子序数依次增大。X的P能级上有2个电子,Y是同一周期中原子半径最大的元素,Z单质易溶于CS2,W的单质是双原子分子,下列说法不正确的是
| A.X有多种同素异形体 | B.Y的氧化物对应的水化物具有两性 |
| C.电负性:X<Z<W | D.最简单氢化物的热稳定性:X<Z<W |
您最近半年使用:0次
22-23高一下·江苏南通·期末
解题方法
5 . 短周期主族元素 的原子序数依次增大。
的原子序数依次增大。 是地壳中含量最高的元素,
是地壳中含量最高的元素, 是金属元素且第一电离能比同周期相邻元素大,
是金属元素且第一电离能比同周期相邻元素大, 与
与 同主族。下列有关说法
同主族。下列有关说法不正确 的是
 的原子序数依次增大。
的原子序数依次增大。 是地壳中含量最高的元素,
是地壳中含量最高的元素, 是金属元素且第一电离能比同周期相邻元素大,
是金属元素且第一电离能比同周期相邻元素大, 与
与 同主族。下列有关说法
同主族。下列有关说法A.电负性: | B.离子半径: |
| C.Y位于元素周期表第三周期ⅡA族 | D.Z最高价氧化物对应水化物的酸性比W的弱 |
您最近半年使用:0次
21-22高二下·全国·单元测试
解题方法
6 . 应用
①判断元素的金属性和非金属性强弱
i.金属的电负性一般_______ 1.8,非金属的电负性一般_______ 1.8,而位于非金属三角区边界的“类金属”(如锗、锑等)的电负性则在_______ 左右,它们既有金属性,又有非金属性。
ii.金属元素的电负性_______ ,金属元素越活泼;非金属元素的电负性_______ ,非金属元素越活泼。
②判断元素的化合价
i.电负性数值小的元素在化合物中吸引电子的能力_______ ,元素的化合价为_______ 。
ii.电负性数值大的元素在化合物中吸引电子的能力_______ ,元素的化合价为_______ 。
③判断化合物的类型

如H的电负性为2.1,Cl的电负性为3.0,Cl的电负性与H的电负性之差为3.0-2.1=0.9<1.7,故HCl为共价化合物;如Al的电负性为1.5,Cl的电负性与Al的电负性之差为3.0-1.5=1.5<1.7,因此AlCl3为共价化合物;同理,BeCl2也是共价化合物。
注意:电负性之差大于1.7的元素不一定都形成离子化合物,如F的电负性与H的电负性之差为1.9,但HF为共价化合物。
①判断元素的金属性和非金属性强弱
i.金属的电负性一般
ii.金属元素的电负性
②判断元素的化合价
i.电负性数值小的元素在化合物中吸引电子的能力
ii.电负性数值大的元素在化合物中吸引电子的能力
③判断化合物的类型

如H的电负性为2.1,Cl的电负性为3.0,Cl的电负性与H的电负性之差为3.0-2.1=0.9<1.7,故HCl为共价化合物;如Al的电负性为1.5,Cl的电负性与Al的电负性之差为3.0-1.5=1.5<1.7,因此AlCl3为共价化合物;同理,BeCl2也是共价化合物。
注意:电负性之差大于1.7的元素不一定都形成离子化合物,如F的电负性与H的电负性之差为1.9,但HF为共价化合物。
您最近半年使用:0次
21-22高二下·全国·单元测试
名校
解题方法
7 . 已知下列元素的电负性数据,下列判断不正确的是
| 元素 | Li | Be | C | O | F | Na | Al | Cl | Ge |
| 电负性 | 1.0 | 1.5 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 3 | 1.8 |
| A.Mg元素电负性的最小范围为1.0~1.6 |
| B.Ge既具有金属性,又具有非金属性 |
| C.Be和Cl形成共价键 |
| D.O和F形成的化合物O显正价 |
您最近半年使用:0次
2022-12-13更新
|
1134次组卷
|
4卷引用:【知识图鉴】单元讲练测选择性必修2第1章01讲核心
(已下线)【知识图鉴】单元讲练测选择性必修2第1章01讲核心(已下线)第一章 原子结构与性质(B卷) 广西钦州市第四中学2022-2023学年高二下学期2月考试化学试题黑龙江省大庆市肇州县第二中学2023-2024学年高二上学期12月月考化学试题
21-22高二下·全国·单元测试
解题方法
8 . 有短周期A、B、C、D四种元素,A、B同周期,C、D同主族,已知A的阳离子与D的阴离子具有相同的电子层结构,B的阴离子和C的阴离子电子层结构相同,且C离子的核电荷数高于B离子,电负性顺序正确的是
| A.A>B>C>D | B.D>C>B>A | C.C>D>B>A | D.B>A>C>D |
您最近半年使用:0次
21-22高二下·全国·单元测试
解题方法
9 . 有关概念与意义
(1)键合电子:元素相互化合时,原子中用于形成_______ 的电子称为_______ 。
(2)电负性:用来描述不同元素的原子对键合电子_______ 的大小。电负性越_______ 的原子,对键合电子的吸引力越_______ 。
(3)电负性大小的标准:以氟的电负性为_______ 和锂的电负性为_______ 作为相对标准。
(1)键合电子:元素相互化合时,原子中用于形成
(2)电负性:用来描述不同元素的原子对键合电子
(3)电负性大小的标准:以氟的电负性为
您最近半年使用:0次
2023·广东·模拟预测
名校
10 . 数据是科学推理中的重要证据,出下表中的数据,所得推论正确的是
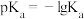
羧酸 |
|
丙酸 | 4.88 |
乙酸 | 4.76 |
甲酸 | 3.75 |
氯乙酸 | 2.86 |
二氯乙酸 | 1.29 |
三氯乙酸 | 0.65 |
三氟乙酸 | 0.23 |
| A.相同浓度下,乙酸的酸性一定强于氯乙酸 |
| B.烃基是吸电子基团,烃基越长,吸电子效应越大,使羧基中的羟基的极性越小,羧酸的酸性越弱 |
| C.卤素原子是推电子基团,卤素原子使得羧基中羟基的极性变小,导致二氯乙酸的酸性强于一氯乙酸 |
D.氟原子的电负性大于氯原子,使 —的极性大于 —的极性大于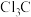 —的极性,使三氟乙酸羧基中羟基的极性增大,导致三氟乙酸容易电离出氢离子 —的极性,使三氟乙酸羧基中羟基的极性增大,导致三氟乙酸容易电离出氢离子 |
您最近半年使用:0次
2022-12-09更新
|
2217次组卷
|
9卷引用:【知识图鉴】单元讲练测选择性必修2第二章02练基础
(已下线)【知识图鉴】单元讲练测选择性必修2第二章02练基础第二章 分子结构与性质(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修2)第一章 有机化合物的结构特点与研究方法(A卷·知识通关练)-【单元测试】2022-2023学年高二化学分层训练AB卷(人教版2019选择性必修3)广东省六校2023届高三第三次联考化学试题广东省六校联盟2022-2023学年高三上学期第三次联考化学试题广东省云浮市罗定中学2022-2023学年高二下学期第2周周测(分子结构与性质)化学试题广东省广州市第二中学等五校2022-2023学年高三上学期12月月考化学试题(已下线)第05讲 分子结构与物质的性质-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)热点05 分子结构与物质的性质