23-24高二下·北京·开学考试
1 . 现有四种元素的基态原子的核外电子排布式如下:
① ;②
;②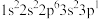 ;③
;③ ;④
;④ 。
。
则下列有关比较中正确的是
①
 ;②
;②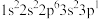 ;③
;③ ;④
;④ 。
。则下列有关比较中正确的是
| A.原子半径:①>②>③>④ | B.第一电离能:④>③>①>② |
| C.最高正化合价:③>④>②>① | D.电负性:④>③>②>① |
您最近半年使用:0次
23-24高二上·陕西西安·期末
名校
2 . 下列关于物质结构与性质的说法,不正确的是
A. 中的 中的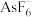 离子的空间结构为正八面体形 离子的空间结构为正八面体形 |
| B.C、H、O三种元素的电负性由小到大的顺序为H<C<O |
C.HClO、 、 、 的中心原子价层电子对数不完全相同 的中心原子价层电子对数不完全相同 |
| D.第四周期元素中,Ga的第一电离能低于Zn |
您最近半年使用:0次
23-24高二上·陕西渭南·期末
解题方法
3 . 1869年门捷列夫编排的元素周期表为我们学习化学提供了理论依据。H、Li、Na、K位于周期表中ⅠA族。下列说法正确的是
| A.元素周期表的每个周期都是从ns能级开始,以mp能级结束 |
B.电负性大小: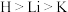 |
C.第一电离能: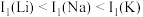 |
D.碱性强弱: |
您最近半年使用:0次
23-24高二上·陕西安康·期末
4 . 下列关于分子的结构和性质的描述中,正确的是
| A.对羟基苯甲酸的熔点比邻羟基苯甲酸的熔点低 |
| B.氨分子间有氢键,故气态氨分子的热稳定性比水蒸气的高 |
| C.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释 |
| D.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性 |
您最近半年使用:0次
23-24高二上·河南南阳·期末
名校
解题方法
5 . 元素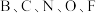 的某性质递变规律如图所示:
的某性质递变规律如图所示:

某性质代表
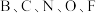 的某性质递变规律如图所示:
的某性质递变规律如图所示:
某性质代表
| A.原子半径 | B.元素的第一电离能 | C.元素的电负性 | D.简单氢化物的稳定性 |
您最近半年使用:0次
2024-02-08更新
|
140次组卷
|
4卷引用:1.2.2 元素周期律(提高)
6 . 四种元素基态原子的电子排布式如下:① ;②
;② ;③
;③ ;④
;④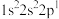 。下列有关比较中正确的是
。下列有关比较中正确的是
 ;②
;② ;③
;③ ;④
;④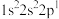 。下列有关比较中正确的是
。下列有关比较中正确的是| A.第一电离能:④>③>②>① | B.原子半径:④>③>①>② |
| C.电负性:③>④>①>② | D.最高正化合价:④=①>③=② |
您最近半年使用:0次
2024-01-24更新
|
134次组卷
|
7卷引用:第一章 本章达标检测2
23-24高二上·宁夏银川·期末
7 . 下列四种元素中,单质氧化性最强的是
| A.原子中p能级有3个电子的元素 |
| B.原子最外层电子排布为2s22p5的元素 |
| C.原子核外电子排布为[Ne]3s23p5的元素 |
| D.位于周期表中第三周期ⅢA族的元素 |
您最近半年使用:0次
23-24高二上·北京丰台·期末
8 . 下列关于 、
、 原子结构的分析中正确的是
原子结构的分析中正确的是
 、
、 原子结构的分析中正确的是
原子结构的分析中正确的是A.原子半径: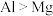 | B.基态原子未成对电子数: |
C.第一电离能: | D.电负性: |
您最近半年使用:0次
23-24高二上·云南昆明·阶段练习
9 . 下列关于元素周期表和元素周期律的说法正确的是
A.在第ⅥA族元素的氢化物( )中,热稳定性最强的其沸点也一定最高 )中,热稳定性最强的其沸点也一定最高 |
| B.第三周期元素的电负性一定小于第二周期元素的 |
| C.第二周期元素的最高正化合价都等于其原子的最外层电子数 |
| D.因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大 |
您最近半年使用:0次
23-24高二上·辽宁盘锦·阶段练习
名校
解题方法
10 . 如图所示为元素周期表中短周期的一部分,下列关于Y、Z、M的说法正确的是
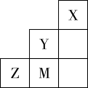

A.电负性: | B.离子半径: |
C.简单氢化物的稳定性: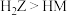 | D.第一电离能: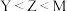 |
您最近半年使用:0次



