名校
解题方法
1 . 由金属钛、铝形成的Tebbe试剂(一种烃基钛茂)常用作有机反应的烯化试剂,其结构如图所示。下列说法错误的是
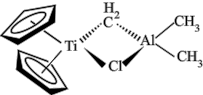
| A.Tebbe试剂为极性分子 | B.该结构中电负性最大的元素是Cl |
C.Tebbe试剂中的Al采取 杂化 杂化 | D.该结构中Al与Cl之间形成配位键 |
您最近半年使用:0次
名校
2 . 2023年诺贝尔化学奖授予蒙吉·G·巴文迪等三位科学家,以表彰他们在发现和合成量子点方面所作出的贡献,碳量子点是一类具有显著荧光性能的零维碳纳米材料,其结构如图所示。回答下列问题:_______ 区,图中C的杂化方式为_______ 。
(2)碳量子点结构包含的元素中电负性由大到小排列为:_______ 。
(3)碳量子点水溶性_______ (选填“>”“<”“=”)石墨水溶性,理由是:_______ 。
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有_______ 种,比较二者C-C共价键的键长:石墨_______ 金刚石(选填“>”“<”“=”)。
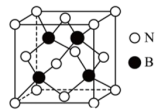
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。_______ ,则立方氮化硼晶体密度为_______ g·cm-3(列出计算式,阿伏加德罗常数的值为NA)。

(2)碳量子点结构包含的元素中电负性由大到小排列为:
(3)碳量子点水溶性
(4)高压合成金刚石的原料是廉价的石墨,用高压釜持续施加高温高压并加入金属镍等金属催化剂,石墨可转化为金刚石。基态镍原子核外电子的空间运动状态有
(5)氮化硼(BN)是一种性能优异、潜力巨大的新型材料,其中一种结构为立方氮化硼(如图),类似于金刚石。
您最近半年使用:0次
名校
3 . 科学家合成了一种含硼阴离子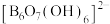 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是
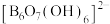 ,其结构如图所示下列叙述错误的是
,其结构如图所示下列叙述错误的是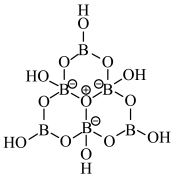
| A.基态硼原子的核外电子的空间运动状态有3种 |
| B.电负性大小为:O>B>H |
| C.该结构中硼原子的杂化方式为sp2、sp3 |
| D.该结构中共有4种不同化学环境的氧原子 |
您最近半年使用:0次
昨日更新
|
150次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷
名校
4 . 下列对事实的分析正确的是
| 选项 | 事实 | 分析 |
| A | 键角: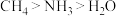 | 电负性:C<N<O |
| B | 第一电离能:P>S | 原子半径:P>S |
| C | 沸点:CO> | CO为极性分子, 为非极性分子 为非极性分子 |
| D | 热稳定性:HF>HCl | HF中存在氢键,HCl中不存在氢键 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
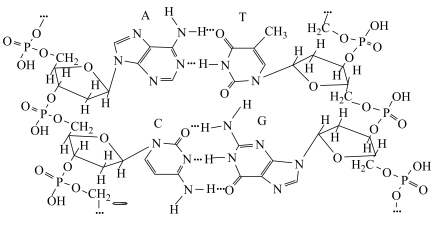
5 . DNA的部分结构如下图所示,其中A为腺嘌呤、G为鸟嘌呤,嘌呤(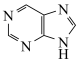 )为平面结构。下列说法正确的是
)为平面结构。下列说法正确的是
 )为平面结构。下列说法正确的是
)为平面结构。下列说法正确的是
A.基态原子电负性: | B.基态原子的价层空轨道数: |
| C.嘌呤中N原子的杂化轨道类型只有一种 | D.图中碱基互补配对时存在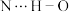 氢键 氢键 |
您最近半年使用:0次
解题方法
6 . 近年来,我国半导体材料市场发展迅速,其中以氮化嫁、碳化硅、氧化锌、金刚石等为主的材料备受关注。回答下列问题:
(1)基态Ga原子的价电子轨道表示式为___________ ,基态N原子核外电子有___________ 种空间运动状态。Zn在元素周期表中位于___________ 区。
(2)C,N、O的第一电离能由大到小的顺序为___________ 。 的空间结构为
的空间结构为___________ 。
(3)SiC的立方晶胞结构如图1所示,已知;1号C原子的坐标参数为( ,
, ,
, ),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
),晶胞参数为apm。则晶胞中2号C原子的坐标参数为___________ ,C和Si原子的最短距离为___________ pm。
①GaN晶体中N原子的杂化轨道类型为___________ 。
②GaN晶体的密度为___________ g/cm3(列出计算式,用含b、c、NA的代数式表示)。
(1)基态Ga原子的价电子轨道表示式为
(2)C,N、O的第一电离能由大到小的顺序为
 的空间结构为
的空间结构为(3)SiC的立方晶胞结构如图1所示,已知;1号C原子的坐标参数为(
 ,
, ,
, ),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
),晶胞参数为apm。则晶胞中2号C原子的坐标参数为
①GaN晶体中N原子的杂化轨道类型为
②GaN晶体的密度为
您最近半年使用:0次
名校
解题方法
7 . 双氰胺( )为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮
)为白色晶体,在冷水中溶解度较小,溶于热水、乙醇,其水溶液在80℃以上会发生分解等副反应,主要用于生产树脂、涂料、含氮复合肥等。实验室以石灰氮 为原料制备双氰胺的流程如下:
为原料制备双氰胺的流程如下:
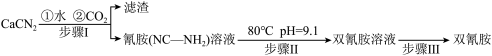
已知氰胺二聚反应机理为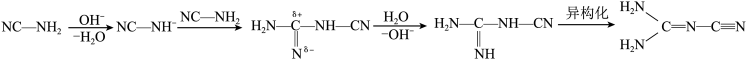
(1)已知:氰基是吸电子基团。氰氨
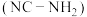 的碱性
的碱性(2)写出步骤Ⅰ的化学反应方程式:
(3)步骤Ⅱ中调节溶液pH为9.1,pH不能过低的原因:
(4)步骤Ⅲ中蒸发浓缩时,常采用真空蒸发浓缩,目的是
(5)凯氏定氮法是测定有机物中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐。
已知:
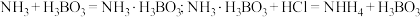

②仪器清洗后,g中加入硼酸
 和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭
和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭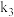 ,d中保留少量水。打开
,d中保留少量水。打开 ,加热b,使水蒸气进入e。
,加热b,使水蒸气进入e。d中保留少量水的目的是
③取双氰胺样品m克进行测定,滴定g中吸收液时消耗浓度为
 的盐酸VmL,则样品中氮的质量分数为
的盐酸VmL,则样品中氮的质量分数为
您最近半年使用:0次
8 . 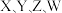 四种短周期元素,
四种短周期元素, 的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
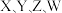 四种短周期元素,
四种短周期元素, 的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是
的一种核素没有中子,其余三种在周期表中位置如图所示,下列判断正确的是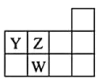
A.单质 与 与 常温下能直接化合 常温下能直接化合 | B.简单氢化物的沸点: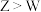 |
C.电负性: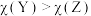 | D. 三种元素组成的化合物是离子化合物 三种元素组成的化合物是离子化合物 |
您最近半年使用:0次
9 . 镓 、铟
、铟 都是典型的稀有分散元素。回答下列问题:
都是典型的稀有分散元素。回答下列问题:
(1)基态 原子的核外价电子排布式为
原子的核外价电子排布式为_____ ,最高能级电子的电子云形状为_____ 。
(2)一种含镓药物的合成方法如图所示: 原子的杂化方式为
原子的杂化方式为_____ , 化合物
化合物 中含有的
中含有的 键的物质的量为
键的物质的量为_____ 。化合物Ⅰ中所含元素的电负性由大到小的顺序为_____ (用元素符号表示)。
②化合物Ⅱ中 的配位数为
的配位数为_____ ,
_____ 。
(3)一种由 组成的晶体属四方晶系,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞棱边夹角均为 ,其晶胞结构如图。
,其晶胞结构如图。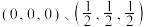 。则C点原子的分数坐标为
。则C点原子的分数坐标为_____ 。
② 表示阿伏加德罗常数的值,该晶体的密度为
表示阿伏加德罗常数的值,该晶体的密度为_____ (用含 的代数式表示)
的代数式表示) 。
。
 、铟
、铟 都是典型的稀有分散元素。回答下列问题:
都是典型的稀有分散元素。回答下列问题:(1)基态
 原子的核外价电子排布式为
原子的核外价电子排布式为(2)一种含镓药物的合成方法如图所示:

 原子的杂化方式为
原子的杂化方式为 化合物
化合物 中含有的
中含有的 键的物质的量为
键的物质的量为②化合物Ⅱ中
 的配位数为
的配位数为
(3)一种由
 组成的晶体属四方晶系,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞棱边夹角均为 ,其晶胞结构如图。
,其晶胞结构如图。
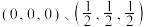 。则C点原子的分数坐标为
。则C点原子的分数坐标为②
 表示阿伏加德罗常数的值,该晶体的密度为
表示阿伏加德罗常数的值,该晶体的密度为 的代数式表示)
的代数式表示) 。
。
您最近半年使用:0次
10 . 短周期主族元素 、
、 、
、 、
、 、
、 的原子序数依次增大,锂离子电池中一种溶剂的结构如图所示。
的原子序数依次增大,锂离子电池中一种溶剂的结构如图所示。 、
、 、
、 位于同周期,基态
位于同周期,基态 原子的价层电子排布式为
原子的价层电子排布式为 。下列说法错误的是
。下列说法错误的是
 、
、 、
、 、
、 、
、 的原子序数依次增大,锂离子电池中一种溶剂的结构如图所示。
的原子序数依次增大,锂离子电池中一种溶剂的结构如图所示。 、
、 、
、 位于同周期,基态
位于同周期,基态 原子的价层电子排布式为
原子的价层电子排布式为 。下列说法错误的是
。下列说法错误的是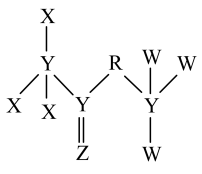
A.简单氢化物的热稳定性: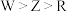 | B.电负性: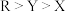 |
C.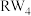 的空间结构为正四面体形 的空间结构为正四面体形 | D. 、 、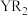 分子中 分子中 原子的杂化方式相同 原子的杂化方式相同 |
您最近半年使用:0次



