名校
解题方法
1 . 已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+原子核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)E元素在周期表中的位置为_______ ,属于_______ 区。
(2)B、C、D三种元素的第一电离能最大的是_______ (填元素符号),第一电离能最大的原因是_______ 。
(3)D元素与氟元素相比,电负性:D_______ F(填“>”“=”或“<”),下列表述中能证明这一事实的是_______ (填字母)。
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物CA5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,其电子式为_______ 。
(1)E元素在周期表中的位置为
(2)B、C、D三种元素的第一电离能最大的是
(3)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物CA5,它的所有原子的最外层都符合相应的稀有气体原子电子层结构,其电子式为
您最近一年使用:0次
2022-08-28更新
|
312次组卷
|
4卷引用:四川省眉山北外附属东坡外国语学校2023-2024学年高二下学期开学化学试题
名校
2 . 下列与分子性质有关的说法正确的是
| A.氟代丙二酸(HOOC—CF2—COOH)的酸性强于丙二酸(HOOC—CH2—COOH)是因为—CF2—的极性大于—CH2—的极性,导致氟代丙二酸羧基中—OH的极性更大更易电离出H+ |
B.邻硝基苯酚(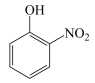 )的沸点高于对硝基苯酚( )的沸点高于对硝基苯酚(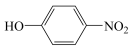 )是因为后者形成了分子间氢键 )是因为后者形成了分子间氢键 |
| C.C的电负性强于Si,所以CH4的熔沸点高于SiH4 |
| D.I2受热易升华,是因为分子内共价键键能较小所致 |
您最近一年使用:0次
名校
3 . 下列有关说法中合理的是
A.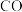 与 与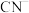 结构相似,含有的 结构相似,含有的 键与 键与 键个数比均为1∶2 键个数比均为1∶2 |
B.根据 理论可知 理论可知 、 、 、 、 分子内键角依次减小 分子内键角依次减小 |
| C.铜的电负性为1.9,氯的电负性为3.0,氯化铜为离子化合物,溶于水能完全电离 |
| D.元素周期表中第ⅠA族和第ⅦA族元素原子间不可能形成共价键 |
您最近一年使用:0次
2024-04-03更新
|
262次组卷
|
2卷引用:黑龙江省齐齐哈尔市讷河市第一中学2023-2024学年高二下学期开学考试化学试题
名校
解题方法
4 . 中国科学家首次在月球上发现新矿物,并将其命名为“嫦娥石 ”。Y(钇)是金属元素。下列说法
”。Y(钇)是金属元素。下列说法
A.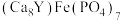 是一种磷酸盐 是一种磷酸盐 |
| B.电负性O>P,嫦娥石中P显正价,O显负价 |
| C.在元素周期表中,O、P、Fe均属于s区元素 |
| D.原子半径:O<P |
您最近一年使用:0次
2024-03-24更新
|
225次组卷
|
3卷引用:北京市第九中学2023-2024学年高二下学期2月开学考化学试题
名校
解题方法
5 . X、Y、Z、R、Q是元素周期表中原子序数依次增大的前四周期元素,X是宇宙中含量最多的元素;Y与Z同周期,Y基态原子有3个未成对电子,Z元素原子的价层电子排布为 ;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法中
;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法中不正确 的是
 ;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法中
;R元素简单离子在同周期离子中半径最小;Q元素最高能层只有1个电子,其余能层均充满电子。下列说法中A.简单气态氢化物的热稳定性: | B.第一电离能: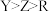 |
| C.Q在周期表的ds区 | D.电负性: |
您最近一年使用:0次
2023-12-23更新
|
539次组卷
|
3卷引用:江西省宜春市丰城中学东校区(九中)2023-2024学年高二下学期开学考试化学试卷
名校
解题方法
6 . 周期表中ⅢA族单质及其化合物应用广泛。BF3极易水解生成HBF4(HBF4在水中完全电离为H+和BF )和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。
)和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。
(1)Ga原子基态外围电子排布式为_____ 。
(2)在第二周期里,第一电离能介于B、N之间的元素有_____ 种;B(OCH3)3分子间_____ (填“能”或“不能”)能形成氢键,GaN属于_____ 晶体。
(3)硼酸是一元弱酸,它的水溶液之所以呈弱酸性并非本身能电离出H+,而是它结合了一个OH-,这种电离方式可表示为B(OH)3+H2O H++
H++_____ 。
(4)硼酸是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是_____(填字母)。

(5)Al2O3的熔点(2054℃)很高,工业冶炼铝时要加入冰晶石(化学式为Na3AlF6)来降低生产成本,如图所示为冰晶石的晶胞。图中“ ”位于大立方体顶点和面心,“
”位于大立方体顶点和面心,“ ”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是
”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是______ (填“Na+”或“AlF63-”),与Na+距离相等且最近的Na+有_____ 个。

 )和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。
)和硼酸(H3BO3),硼酸是一元弱酸,能溶于水。硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯[B(OCH3)3],硼酸甲酯主要用作热稳定剂、木材防腐剂等。GaN的结构与晶体硅类似,是第三代半导体研究的热点。(1)Ga原子基态外围电子排布式为
(2)在第二周期里,第一电离能介于B、N之间的元素有
(3)硼酸是一元弱酸,它的水溶液之所以呈弱酸性并非本身能电离出H+,而是它结合了一个OH-,这种电离方式可表示为B(OH)3+H2O
 H++
H++(4)硼酸是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的是_____(填字母)。

| A.硼酸晶体的熔点比NaBF4低 |
| B.H3BO3分子的热稳定性与氢键有关 |
| C.含1molH3BO3的晶体中有3mol氢键 |
| D.BF3分子中每个原子最外层均满足8电子结构 |
(5)Al2O3的熔点(2054℃)很高,工业冶炼铝时要加入冰晶石(化学式为Na3AlF6)来降低生产成本,如图所示为冰晶石的晶胞。图中“
 ”位于大立方体顶点和面心,“
”位于大立方体顶点和面心,“ ”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是
”位于大立方体的12条棱的中点和8个小立方体的体心。则大立方体的体心处△代表的微粒是
您最近一年使用:0次
2023-12-11更新
|
198次组卷
|
2卷引用:重庆市万州二中2023-2024学年高二下学期开学考试 化学
7 . 已知有3种基态元素原子的核外电子排布式:① ②
② ③
③ ,下列说法错误的是
,下列说法错误的是
 ②
② ③
③ ,下列说法错误的是
,下列说法错误的是| A.①与②可组成空间结构为正四面体形的化合物 |
| B.电负性:②>①>③ |
| C.第一电离能:①>③>② |
| D.三种元素均位于p区 |
您最近一年使用:0次
8 . 日光中用到的某种荧光粉的主要成分为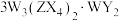 。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为
。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为 。下列说法错误的是
。下列说法错误的是
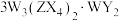 。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为
。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为 。下列说法错误的是
。下列说法错误的是| A.电负性:Y>X>Z>W |
| B.原子半径:Y>X>Z>W |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
您最近一年使用:0次
名校
9 . 下列说法中正确的是
| A.电子云图中的小黑点密表示该核外空间的电子多 |
B.电子排布式 违反了洪特规则 违反了洪特规则 |
| C.原子序数为7、8、9的三种元素,其第一电离能和电负性均依次增大 |
| D.电子仅由激发态跃迁到基态时才会产生原子光谱 |
您最近一年使用:0次
2024-04-04更新
|
199次组卷
|
2卷引用:黑龙江省大庆市大庆中学2023-2024学年高二下学期开学化学试题
名校
解题方法
10 . 某种离子液体的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与Q同主族。下列说法错误的是


| A.简单离子半径:Q>Z>W | B.简单氢化物键角:Y>Z>Q |
| C.最高价氧化物对应水化物的酸性:Z<Q | D.元素的电负性:Z>Y>X |
您最近一年使用:0次



