解题方法
1 . O3分子内部存在“三中心四电子”的离域π键(如图虚线部分所示),由于O3分子的中心氧原子较端位氧原子多提供一个电子,故中心氧原子带部分正电荷,端位氧原子带部分负电荷。___________ (选填“是”或“否”),解释O3在水中溶解度大于O2的可能原因。___________
2.判断并解释反应2O3=3O2是否属于氧化还原反应___________ 。
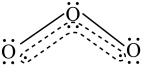
2.判断并解释反应2O3=3O2是否属于氧化还原反应
您最近一年使用:0次
解题方法
2 . 香兰素与2,4-戊二酮(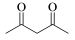 )反应可以合成姜黄素:
)反应可以合成姜黄素:
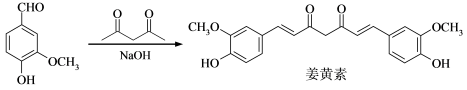
2.参照上述流程,设计以
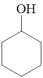 和CH3CHO为原料合成
和CH3CHO为原料合成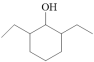 的合成路线
的合成路线(合成路线可表示为:甲
 乙∙∙∙∙∙∙
乙∙∙∙∙∙∙ 目标产物)
目标产物)
您最近一年使用:0次
解题方法
3 . 三乙酸锰([Mn(CH3COO)3])是一种锰的配合物,在有机合成中有重要的应用价值。CH3COO―为该配合物的配体,其所含元素的电负性最大的是___________ ;FCH2COO-、ClCH2COO-也可作为配体使用,相同条件下,FCH2COO-、ClCH2COO-结合H+的能力较强的是___________ 。
您最近一年使用:0次
解题方法
4 . 一种具有高弹性的自修复聚氨酯材料(TPU)结构如下:_______ 碳氮双键的键能。
A.大于 B.等于 C.小于
2.请写出TPU中元素的第一电离能的大小关系_______ 。

该聚合物由X( )和Y(
)和Y( )聚合而成。
)聚合而成。
A.大于 B.等于 C.小于
2.请写出TPU中元素的第一电离能的大小关系
您最近一年使用:0次
名校
解题方法
5 .  和
和 是硫元素的重要氧化物,下列说法中正确的是
是硫元素的重要氧化物,下列说法中正确的是
 和
和 是硫元素的重要氧化物,下列说法中正确的是
是硫元素的重要氧化物,下列说法中正确的是A. 和 和 中S原子杂化方式均为 中S原子杂化方式均为 |
B. 和 和 中S原子杂化方式不同,前者为 中S原子杂化方式不同,前者为 ,后者为 ,后者为 |
C. 的VSFPR模型为平面三角形,键角为120° 的VSFPR模型为平面三角形,键角为120° |
D. 的VSEPR模型为角形,键角小于120° 的VSEPR模型为角形,键角小于120° |
您最近一年使用:0次
名校
解题方法
6 .  与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为_______ ,其空间构型为_______ 。
 与光气
与光气 反应可用于制取四氯化钛。
反应可用于制取四氯化钛。 中σ键和π键的数目比为
中σ键和π键的数目比为
您最近一年使用:0次
名校
7 . 羰基铁[ ]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为
]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为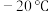 ,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。 晶体类型为___________。
晶体类型为___________。
2.下列说法正确的是___________。
 ]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为
]广泛用于催化剂,汽油抗爆剂等,为黄色粘稠状液体,熔点为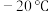 ,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
,沸点为103℃,60℃在空气中可自燃,其结构和部分键长如图所示。
 晶体类型为___________。
晶体类型为___________。| A.分子晶体 | B.离子晶体 | C.金属晶体 | D.共价晶体 |
A.中心Fe原子可能采取 杂化 杂化 |
| B.配体与Fe原子所形成的配位键的键能相同 |
| C.Fe在周期表中位于VIII族,属于d区元素 |
D.制备 应在隔绝空气的条件下进行 应在隔绝空气的条件下进行 |
您最近一年使用:0次
解题方法
8 . 固态NH3晶体中含有的作用力有
| A.非极性键 | B.极性键 | C.配位键 | D.氢键 |
您最近一年使用:0次
名校
解题方法
9 . N和P同处于ⅤA族,其相应物质既有相似性又有差异。已知有关氮、磷的键能数据(kJ/mol)如表:
| N—N |  | P—P |  |
| 193 | 946 | 197 | 489 |
结合计算,从键能角度解释氮的单质以 、而磷单质以
、而磷单质以 (
(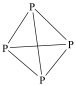 )形式存在的原因
)形式存在的原因
您最近一年使用:0次
名校
10 .  与
与 的中心原子均为
的中心原子均为 杂化,二者键角:
杂化,二者键角:
___________  (填“>”“=”或“<”),从结构角度说明原因:
(填“>”“=”或“<”),从结构角度说明原因:___________ 。
 与
与 的中心原子均为
的中心原子均为 杂化,二者键角:
杂化,二者键角:
 (填“>”“=”或“<”),从结构角度说明原因:
(填“>”“=”或“<”),从结构角度说明原因:
您最近一年使用:0次



