名校
解题方法
1 . 氢氟酸是常见的刻蚀剂,刻蚀玻璃时发生的反应为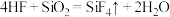 ,下列有关说法错误的是
,下列有关说法错误的是
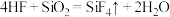 ,下列有关说法错误的是
,下列有关说法错误的是A. 的电离方程式为 的电离方程式为 | B. 的 的 模型为 模型为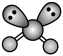 |
C. 的电子式为 的电子式为 | D. 的空间填充模型为 的空间填充模型为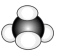 |
您最近一年使用:0次
名校
解题方法
2 . 关于物质结构和性质分析正确的是
| A.键角大小关系:CH4>SO3>H2O |
| B.沸点大小关系:邻羟基苯甲酸<对羟基苯甲酸 |
| C.在化合物K3[Fe(CN)6]中,N原子提供孤电子对形成配位键 |
| D.酸性强弱比较:乙酸>甲酸>碳酸 |
您最近一年使用:0次
名校
解题方法
3 . 下列说法不正确的是
A. 的价层电子轨道式 的价层电子轨道式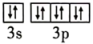 |
B. 的电子式 的电子式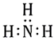 |
C. 的VSEPR模型为: 的VSEPR模型为: |
D.基态Ca原子占据的最高能级原子轨道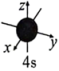 |
您最近一年使用:0次
4 . 稀有气体氙的氟化物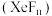 与
与 溶液反应剧烈,与水反应则较为温和,反应式如下:
溶液反应剧烈,与水反应则较为温和,反应式如下:
下列说法正确的是
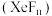 与
与 溶液反应剧烈,与水反应则较为温和,反应式如下:
溶液反应剧烈,与水反应则较为温和,反应式如下:| 与水反应 | 与 溶液反应 溶液反应 |
i.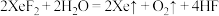 | ii.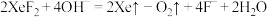 |
iii. | Ⅳ.  |
A. 具有平面三角形结构 具有平面三角形结构 | B. 的还原性比 的还原性比 强 强 |
C.反应 均为氧化还原反应 均为氧化还原反应 | D.反应iv每生成 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
名校
解题方法
5 . 按要求完成下列问题:
(1)写出CCl4中心原子成键时采取的杂化轨道类型及分子中共价键的键角:___________ 、___________ 。
(2)气态 分子的空间构型为
分子的空间构型为___________ , 离子的空间构型为
离子的空间构型为___________ ;
(3)写出基态铁原子的简化电子排布式和Mg2+的核外电子排布式:___________ 、___________ 。
(1)写出CCl4中心原子成键时采取的杂化轨道类型及分子中共价键的键角:
(2)气态
 分子的空间构型为
分子的空间构型为 离子的空间构型为
离子的空间构型为(3)写出基态铁原子的简化电子排布式和Mg2+的核外电子排布式:
您最近一年使用:0次
解题方法
6 . 下列表示反应中相关微粒的化学用语正确的是
A.基态氧原子的轨道表示式: | B.中子数为18的氯原子: |
C. 的空间填充模型: 的空间填充模型: 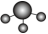 | D. 的电子式: 的电子式: |
您最近一年使用:0次
名校
7 . 光伏材料又称太阳能材料,是指能将太阳能直接转换成电能的材料。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAlAs、InP、CdS 等。回答下列问题:
(1)基态Cr原子的价电子排布式为___________ 。
(2)原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则基态S原子中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态S原子中电子自旋磁量子数的代数和为___________ 。
(3)基态P原子中电子占据的最高能层符号为___________ ; 的空间结构为
的空间结构为___________ 。
(4)砷化镓薄膜太阳能电池被用来为“天宫”空间站的核心舱供电。已知砷化镓的熔点为1238℃,其晶胞结构如下图所示。___________ 。
②该晶体的类型为___________ ;若晶胞密度为d  ,摩尔质量为M
,摩尔质量为M  ,阿伏加德罗常数的值用NA表示,则晶胞中最近的As和Ga原子核间距为
,阿伏加德罗常数的值用NA表示,则晶胞中最近的As和Ga原子核间距为___________ nm(只列计算式)。
(1)基态Cr原子的价电子排布式为
(2)原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则基态S原子中电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态S原子中电子自旋磁量子数的代数和为(3)基态P原子中电子占据的最高能层符号为
 的空间结构为
的空间结构为(4)砷化镓薄膜太阳能电池被用来为“天宫”空间站的核心舱供电。已知砷化镓的熔点为1238℃,其晶胞结构如下图所示。
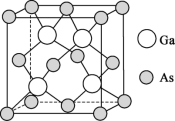
②该晶体的类型为
 ,摩尔质量为M
,摩尔质量为M  ,阿伏加德罗常数的值用NA表示,则晶胞中最近的As和Ga原子核间距为
,阿伏加德罗常数的值用NA表示,则晶胞中最近的As和Ga原子核间距为
您最近一年使用:0次
名校
解题方法
8 . 根据杂化轨道理论和价层电子对互斥模型,判断下列分子或者离子的立体构型正确的是
| 选项 | 分子式 | 中心原子杂化方式 | 价层电子对互斥模型 | 分子或离子的立体构型 |
| A |  | sp | 直线形 | 直线形 |
| B |  |  | 平面三角形 | 三角锥形 |
| C |  |  | 四面体形 | 平面三角形 |
| D |  |  | 四面体形 | 正四面体形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列粒子的 模型为四面体且所有原子在同一平面的是
模型为四面体且所有原子在同一平面的是
 模型为四面体且所有原子在同一平面的是
模型为四面体且所有原子在同一平面的是A. | B. | C. | D. |
您最近一年使用:0次
名校
10 . 下列各组微粒的空间构型相同的是
①NH3和H2O ②NH 和H3O+ ③NH3和H3O+ ④BF3和NO
和H3O+ ③NH3和H3O+ ④BF3和NO ⑤CO2和BeCl2 ⑥PO
⑤CO2和BeCl2 ⑥PO 和SO
和SO ⑦O3和SO2
⑦O3和SO2
①NH3和H2O ②NH
 和H3O+ ③NH3和H3O+ ④BF3和NO
和H3O+ ③NH3和H3O+ ④BF3和NO ⑤CO2和BeCl2 ⑥PO
⑤CO2和BeCl2 ⑥PO 和SO
和SO ⑦O3和SO2
⑦O3和SO2| A.全部 | B.除④⑥⑦以外都相同 | C.②⑤⑥ | D.③④⑤⑥⑦ |
您最近一年使用:0次



