名校
1 . 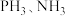 和
和 的分子空间结构和相应的键角如图所示。下列说法
的分子空间结构和相应的键角如图所示。下列说法不正确 的是
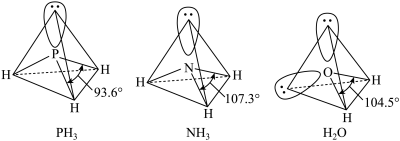
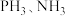 和
和 的分子空间结构和相应的键角如图所示。下列说法
的分子空间结构和相应的键角如图所示。下列说法
| A.N、O、P都是周期表中的p区元素 |
B. 相对分子质量大于 相对分子质量大于 ,故沸点: ,故沸点: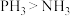 |
C. 的键角小于 的键角小于 是因为孤电子对之间的斥力更大 是因为孤电子对之间的斥力更大 |
| D.上述分子的VSEPR模型均为四面体 |
您最近一年使用:0次
2023-04-28更新
|
337次组卷
|
2卷引用:北京师范大学第二附属中学2022-2023学年高二下学期期中考试化学试题
2 . 下列说法正确的是
| A.HF、HCl、HBr的沸点依次增大 | B.H原子的1s电子云轮廓图为球形 |
| C.CH2Cl2分子中的碳原子为手性碳原子 | D.H2O分子的VSEPR模型是平面三角形 |
您最近一年使用:0次
名校
解题方法
3 . 气态 分子的空间构型是
分子的空间构型是
 分子的空间构型是
分子的空间构型是| A.直线形 | B.平面三角形 | C.四面体形 | D.三角锥形 |
您最近一年使用:0次
解题方法
4 . 下列分子的空间结构中,属于H2O的分子结构模型的是
A. | B. | C. | D. |
您最近一年使用:0次
2021-02-21更新
|
167次组卷
|
2卷引用:北京市大兴区2020-2021学年高一上学期期末考试化学试题
名校
5 . 根据价层电子对互斥理论及杂化轨道理论判断NF3分子的空间构型和中心原子的杂化方式分别为
| A.直线形 sp杂化 | B.三角形 sp2杂化 |
| C.三角锥形 sp2杂化 | D.三角锥形 sp3杂化 |
您最近一年使用:0次
2021-01-29更新
|
1068次组卷
|
12卷引用:北京市第十四中学2021-2022学年高二下学期期中考试化学试题
北京市第十四中学2021-2022学年高二下学期期中考试化学试题四川省巴中市平昌县驷马中学2020-2021学年高二上学期期末测试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构 课时2 杂化轨道理论鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构 第1课时 分子空间结构的理论分析高二选择性必修2(人教版2019)第二章 分子结构与性质 第二节 分子的空间结构 课时2 杂化轨道理论(已下线)作业04 分子的空间结构-2021年高二化学暑假作业(人教版2019)新疆疏勒县第一中学2020--2021学年高二下学期期末考试化学试题(已下线)T9-物质结构与性质2.2.1分子空间结构的理论分析(课后)-鲁科版选择性必修2(已下线)2.2.2 杂化轨道理论(基础)新疆霍尔果斯市苏港中学2023-2024学年高二下学期4月月考化学试题2.2.2 杂化轨道理论-随堂练习
6 . 关于CO2说法正确的是( )
| A.CO2是直线型结构 | B.碳原子采取sp3杂化 |
| C.CO2分子中含非极性键 | D.CO2为极性分子 |
您最近一年使用:0次
2020-11-21更新
|
266次组卷
|
2卷引用:北京市第四十三中学2020-2021学年高二下学期第一次月考化学试题
解题方法
7 . 根据价层电子对互斥理论及原子轨道的杂化理论推测,SO3分子的空间构型和中心原子的杂化方式是
| A.平面三角形,sp2杂化 | B.三角形,sp3杂化 |
| C.正四面体形,sp2杂化 | D.正方形,sp3杂化 |
您最近一年使用:0次
2020-08-06更新
|
367次组卷
|
2卷引用:北京市第四十三中学2020-2021学年高二下学期第一次月考化学试题
名校
8 . 下列对一些实验事实的理论解释正确的是
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | CO2为直线形分子 | CO2分子中C=O之间的夹角为180° |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2013-05-23更新
|
1332次组卷
|
14卷引用:北京市第五十五中学2023-2024学年高二下学期期中调研化学试题
北京市第五十五中学2023-2024学年高二下学期期中调研化学试题(已下线)2012--2013学年新疆乌鲁木齐市一中高二下学期期中考试化学试卷(特长班)(已下线)2013届新疆乌鲁木齐市一中高二下学期特长班期中考试化学试卷2015-2016学年贵州省思南中学高二下期中化学试卷2015-2016学年江苏省启东中学高二下第二次月考化学试卷2016-2017学年宁夏银川市第二中学高二下学期第一次月考化学试卷山西省大同市第一中学2016-2017学年高二5月月考化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题【全国百强校】山西省大同市第一中学2017-2018学年高二5月月考化学试题山西省朔州市怀仁县大地学校2019-2020学年高二下学期期末考试化学试题辽宁省大连市一0三中学2020-2021学年高二4月月考化学试题辽宁省抚顺市重点高中2020-2021学年高二下学期期末考试化学试题重庆市清华中学2021-2022学年高二下学期期第一次月考化学试题吉林省榆树市第一高级中学校2021-2022学年高三上学期第二次模拟考试化学试题



