名校
解题方法
1 . 下列图像正确的是
A. 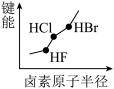 | B. 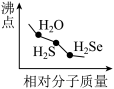 |
C. 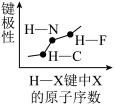 | D. 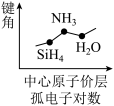 |
您最近一年使用:0次
2023-03-26更新
|
432次组卷
|
9卷引用:江苏省泰州中学2020-2021学年高一下学期期末考试化学试题
江苏省泰州中学2020-2021学年高一下学期期末考试化学试题山东省济宁市兖州区2019-2020学年高二5月阶段性测试化学试题(已下线)第2章 章末综合测评B-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)河北省沧州市2021-2022学年高二下学期期末考试化学试题黑龙江省佳木斯市第十二中学2021-2022学年高二下学期期中考试化学试题河南省洛阳强基联盟2022-2023学年高二下学期3月联考化学试题湖北省宜昌市协作体2022-2023学年高二下学期期中考试化学试题湖南省岳阳市郡华学校2023-2024学年高二下学期入学考试化学试题江西省萍乡市2023-2024学年高二下学期4月期中考试化学试题
2 . 图为周期表中短周期的一部分。若Y原子价电子排布为ns2np3,下列说法正确的是
| X | ||
| Y | Z | W |
| A.X和Z形成的化合物的空间构型一定为V形 |
| B.YW5分子中所有原子均满足8电子稳定结构 |
| C.X的最高正价和最低负价的绝对值之和为8 |
| D.X、Y、Z、W都可以与氢元素形成18电子结构物质 |
您最近一年使用:0次
名校
解题方法
3 . 氮及其化合物在生产生活中应用广泛。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式___ ;基态铬、氮原子的核外未成对电子数之比为___ 。
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为___ ,过硫酸铵的阳离子的空间构型为___ 。
(3) 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为__ ,CP的中心Co3+的配位数为___ 。
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为
(3)
 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为
中孤电子对与π键比值为
您最近一年使用:0次
4 . 有5种元素X、Y、Z、Q、T。X原子M层上有2个未成对电子且无空轨道;Y原子的特征电子构型为3d64s2;Z原子的L电子层的p能级上有一个空轨道;Q原子的L电子层的p能级上只有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述不正确的是( )
| A.元素Y和Q可形成化合物Y3Q4 |
| B.T有一种单质的空间构型为正四面体形 |
| C.X和Q结合生成的化合物为离子化合物 |
| D.ZQ2是由极性键构成的非极性分子 |
您最近一年使用:0次
名校
解题方法
5 . 下列各组微粒的空间构型相同的共有几个( )
①NH3和H2O ②BF3和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥ 和
和 ⑦NF3和Al2Cl6
⑦NF3和Al2Cl6
①NH3和H2O ②BF3和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和BeCl2 ⑥
 和
和 ⑦NF3和Al2Cl6
⑦NF3和Al2Cl6| A.6 | B.5 | C.4 | D.3 |
您最近一年使用:0次
名校
6 . 以下是一些分子的比例模型,其中空间结构和原子大小比例错误 的是
A.NH3 |
B.H2O |
C.HCl |
D.CCl4 |
您最近一年使用:0次
2017-04-22更新
|
203次组卷
|
4卷引用:2016-2017学年江苏省沭阳县高一下学期期中调研测试化学试卷
7 . M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为______ ,晶体中原子间通过_____ 作用形成面心立方密堆积,其中M原子的配位数为______ 。
(2)元素Y基态原子的核外电子排布式为________ ,其同周期元素中,第一电离能最大的是______ (写元素符号)。元素Y的含氧酸中,酸性最强的是________ (写化学式),该酸根离子的立体构型为________ 。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
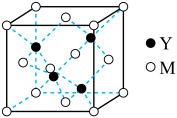
①该化合物的化学式为_______ ,已知晶胞参数a=0.542 nm,此晶体的密度为_______ g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________ 。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______ 。
(1)单质M的晶体类型为
(2)元素Y基态原子的核外电子排布式为
(3)M与Y形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为
②该化合物难溶于水但易溶于氨水,其原因是
您最近一年使用:0次
2016-12-09更新
|
1242次组卷
|
8卷引用:【全国百强校】江苏省海安高级中学2018-2019学年高一(创新班)上学期第一次月考化学试题



