1 . ClNO中N为中心原子,各原子均达到8电子稳定结构,下列说法正确的是
A. 晶体属于分子晶体 晶体属于分子晶体 | B.ClNO的结构式为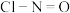 |
C. 中所含键角均为90° 中所含键角均为90° | D. 的配位数为5 的配位数为5 |
您最近一年使用:0次
名校
2 . 某种电化学的电解液的组成如图所示,X、Y、Z、Q、W为原子序数依次增大的短周期元素,下列说法正确的是


A.电解熔融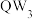 可获得Q的单质 可获得Q的单质 | B.原子半径: |
| C.W的含氧酸均为强酸 | D.QW 的空间构型为正四面体 的空间构型为正四面体 |
您最近一年使用:0次
2023-03-04更新
|
397次组卷
|
4卷引用:江苏省扬州中学2022-2023学年高三上学期11月月考化学试题
名校
解题方法
3 . 二氧化氯(ClO2)是绿色消毒剂,实验室用如下方法制备ClO2:

已知:NCl3为强氧化剂,其中N元素为-3价。下列说法错误的是

已知:NCl3为强氧化剂,其中N元素为-3价。下列说法错误的是
| A.NCl3的空间构型为三角锥形 |
B.电解池中总反应的化学方程式为NH4Cl+2HCl NCl3+3H2↑ NCl3+3H2↑ |
| C.X溶液中主要存在的离子有H+、Na+、Cl- |
| D.饮用水制备过程中残留的ClO2可用适量FeSO4溶液去除 |
您最近一年使用:0次
4 . 碱式碳酸氧钒铵晶体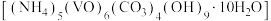 是制备多种含钒产品的原料。有关说法
是制备多种含钒产品的原料。有关说法不正确 的是
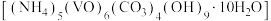 是制备多种含钒产品的原料。有关说法
是制备多种含钒产品的原料。有关说法A. 的空间构型为正四面体形 的空间构型为正四面体形 | B.基态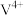 的核外电子排布式为 的核外电子排布式为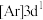 |
C. 中C的轨道杂化类型为 中C的轨道杂化类型为 杂化 杂化 | D. 是非极性分子 是非极性分子 |
您最近一年使用:0次
2023-01-17更新
|
434次组卷
|
4卷引用:江苏省2022年普通高中学业水平选择性考试变式题(选择题1-5)
(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题1-5)(已下线)江苏省南通市如皋市2022-2023学年高三上学期1月期末考试化学试题天津市河北区2022-2023学年高三上学期期末考试化学试题广东省梅州市大埔县2023届高三下学期二模(百所名校冲刺卷2)化学试题
5 . 下列关于Cl−、ClO2、 和
和 的说法
的说法不正确 的是
 和
和 的说法
的说法A.Cl−提供孤电子对与Cu2+可形成CuCl | B.ClO2属于共价化合物 |
C. 的空间结构为三角锥 的空间结构为三角锥 | D. 的键角比 的键角比 的键角大 的键角大 |
您最近一年使用:0次
解题方法
6 . 炼钢厂排放的烟气中主要含SO2、NO、N2等。臭氧(O3)具有强氧化性,可用于烟气的脱硫脱硝,其空间构型与SO2相同。向含NO的模拟烟气中通入足量O3,发生的反应为2NO(g)+3O3(g)=N2O5(g)+3O2(g) ΔH<0,生成的N2O5再用NH3还原为N2;向含SO2的模拟烟气中通入一定量NH3、O3,一段时间后检测到有(NH4)2SO4和少量(NH4)2SO3生成。下列有关O3 、SO 、SO
、SO 和NH3的说法正确的是
和NH3的说法正确的是
 、SO
、SO 和NH3的说法正确的是
和NH3的说法正确的是| A.O3的空间构型为三角锥形 |
B.SO 与SO 与SO 中硫氧键的键角相等 中硫氧键的键角相等 |
| C.氨气易液化是因为NH3与H2O之间形成了分子间氢键 |
| D.NH3能与Ag+、Cu2+形成配合物是因为NH3中的N存在孤电子对 |
您最近一年使用:0次
名校
解题方法
7 . 我国自主设计生产的长征二号火箭使用偏二甲肼和N2O4作推进剂,燃烧时发生反应: 。下列有关说法正确的是
。下列有关说法正确的是
 。下列有关说法正确的是
。下列有关说法正确的是A.偏二甲肼的结构简式: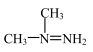 | B.N2的沸点比CO的高 |
| C.CO2的空间构型为V形 | D.H2O是由极性键构成的极性分子 |
您最近一年使用:0次
2022-12-16更新
|
171次组卷
|
2卷引用:江苏省如皋中学2022-2023学年高三上学期第二次阶段考试化学试题
名校
解题方法
8 . 周期表中VIA族元素及其化合物应用广泛。用硫磺熏蒸中药材的传统由来已久; 是一种易燃的有毒气体(燃烧热为
是一种易燃的有毒气体(燃烧热为 ),可制取各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯
),可制取各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯 是重要的化工试剂,常作氯化剂或氯磺化剂。硒
是重要的化工试剂,常作氯化剂或氯磺化剂。硒 和碲(52
和碲(52 的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)为原料回收
的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)为原料回收 ,以电解强碱性
,以电解强碱性 溶液制备
溶液制备 。下列说法正确的是
。下列说法正确的是
 是一种易燃的有毒气体(燃烧热为
是一种易燃的有毒气体(燃烧热为 ),可制取各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯
),可制取各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯 是重要的化工试剂,常作氯化剂或氯磺化剂。硒
是重要的化工试剂,常作氯化剂或氯磺化剂。硒 和碲(52
和碲(52 的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)为原料回收
的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)为原料回收 ,以电解强碱性
,以电解强碱性 溶液制备
溶液制备 。下列说法正确的是
。下列说法正确的是A. 、 、 都是由极性键构成的极性分子 都是由极性键构成的极性分子 |
B. 与 与 微粒中的 微粒中的 夹角都是 夹角都是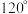 |
C.硒原子基态核外电子排布式为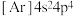 |
| D.VIA族元素氢化物的沸点从上到下依次增大 |
您最近一年使用:0次
2022-12-04更新
|
308次组卷
|
2卷引用:江苏省苏州市八校联盟、南京市第一中学、南京市中华中学2022-2023学年高三上学期12月联考化学试题
9 . 铁及其化合物在生活中用途广泛,绿矾(FeSO4·7H2O)是一种常见的中草药成分,失水后可转为FeSO4·H2O,与FeS2可联合制备铁粉精(FexOy)和H2SO4。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为_________ 。
(2)比较 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:_________ 。
(3) 与
与 和
和 之间的作用力分别为
之间的作用力分别为_________ 。
ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。
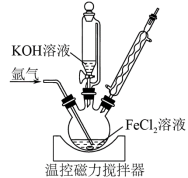
①三颈烧瓶发生反应的离子方程式为_________ 。
②检验反应是否进行完全的操作是_________ 。
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是_________ 。
②计算实验所得产品的产率_________ 。
i.FeSO4·H2O结构如图所示:

(1)Fe2+价层电子排布式为
(2)比较
 和
和 分子中的键角大小并给出相应解释:
分子中的键角大小并给出相应解释:(3)
 与
与 和
和 之间的作用力分别为
之间的作用力分别为ii.实验室以 FeCl2溶液为原料制备高密度磁记录材料 Fe/Fe3O4复合物。
(4)在氩气气氛下,向装有50mL1mol•L−1FeCl2溶液的三颈烧瓶(装置如图)中逐滴加入 100mL14 mol∙L−1KOH溶液,用磁力搅拌器持续搅拌,在100℃下回流3h,得到成分为Fe和Fe3O4的黑色沉淀。

①三颈烧瓶发生反应的离子方程式为
②检验反应是否进行完全的操作是
(5)待三颈烧瓶中的混合物冷却后,过滤,再依次用沸水和乙醇洗涤,在40℃干燥后焙烧3h,得到Fe/Fe3O4复合物产品 3.24g。
①焙烧需在隔绝空气条件下进行,原因是
②计算实验所得产品的产率
您最近一年使用:0次
解题方法
10 . 下列说法正确的是
| A.基态Ca原子的内层电子为全充满 | B.原子半径:r(P)>r(Ca) |
| C.HCHO与H2O分子中的键角相同 | D.PO 的空间结构为正四面体形 的空间结构为正四面体形 |
您最近一年使用:0次



