名校
解题方法
1 . 下列说法正确的是
A. 的第一电离能高于 的第一电离能高于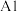 ,则 ,则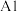 的金属性强于 的金属性强于 |
B. 是非极性分子,则 是非极性分子,则 也是非极性分子 也是非极性分子 |
| C.分子晶体中分子间作用力越大,对应的物质越稳定 |
| D.杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对 |
您最近一年使用:0次
名校
解题方法
2 . 下列化学用语表述正确的是
A. 的价电子排布式: 的价电子排布式: | B. 的球棍模型: 的球棍模型: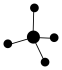 |
C. 的电子式: 的电子式: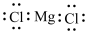 | D. 分子的VSEPR模型: 分子的VSEPR模型: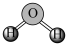 |
您最近一年使用:0次
名校
解题方法
3 . 下列化学用语或图示表达正确的是
A.HCl的电子式: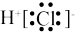 | B.基态碳原子的轨道表示式: |
C.中子数为7的氮原子: | D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
2024-04-01更新
|
420次组卷
|
4卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
解题方法
4 . X、Y、Z、W为原子序数依次增大的短周期主族元素,X、Y、Z位于同周期且相邻,X与W同族,W的核外电子总数等于X和Z的核外电子总数之和。下列说法正确的是
A.元素的第一电离能: |
B.简单氢化物的稳定性: |
C.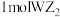 中有 中有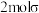 键 键 |
D. 的空间结构为V形,属于含有极性键的极性分子 的空间结构为V形,属于含有极性键的极性分子 |
您最近一年使用:0次
名校
解题方法
5 . NaClO2在工业生产中常用作漂白剂、脱色剂、消毒剂、拔染剂等。实验室中可用H2O2和NaOH混合溶液吸收ClO2的方法制取NaClO2,现利用如下装置及试剂制备NaClO2晶体:
已知:①NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
②ClO2气体浓度较大时易发生爆炸。
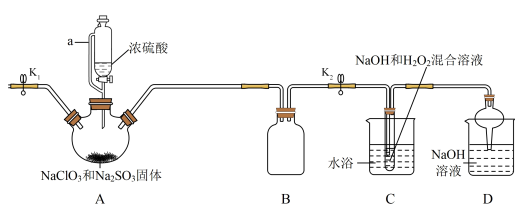
(1)A装置中仪器a的名称为______ 。装置D中NaOH溶液的作用是______ 。
(2)装置A中生成ClO2的化学方程式为______ 。
(3)关于装置C及后续操作的下列说法中,错误的是______ 。
(4)仪器A中NaClO3需稍微过量,原因是______ 。
(5)实验过程中,常需要打开K1,鼓入一定量空气。该操作的目的是______ 。
(6)Cl和O可形成另一种化合物Cl2O,中心原子为O,Cl2O的VSEPR模型是______ ;Cl2O键角比F2O键角______ (填“大”“小”或“相等”)。
(7)NaClO2纯度的测定:用“间接碘量法”测定样品(杂质与I-不发生反应)的纯度,过程如下:取样品1.810g配制成250mL溶液,从中取出25.00mL;加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液(已知:ClO
 +4I-+4H+=2H2O+2I2+Cl-),然后用cmol•L-1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-),然后用cmol•L-1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O =S4O
=S4O +2I-)。样品中NaClO2的纯度为
+2I-)。样品中NaClO2的纯度为______ %(用含c、V的代数式表示)。
已知:①NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
②ClO2气体浓度较大时易发生爆炸。

(1)A装置中仪器a的名称为
(2)装置A中生成ClO2的化学方程式为
(3)关于装置C及后续操作的下列说法中,错误的是
| A.装置C中H2O2作氧化剂 |
| B.为获得NaClO2晶体,可将C试管中的溶液在55℃蒸发浓缩结晶并趁热过滤 |
| C.用50℃左右温水洗涤所得晶体 |
| D.高温烘干过滤后所得滤渣即可得到产物 |
(4)仪器A中NaClO3需稍微过量,原因是
(5)实验过程中,常需要打开K1,鼓入一定量空气。该操作的目的是
(6)Cl和O可形成另一种化合物Cl2O,中心原子为O,Cl2O的VSEPR模型是
(7)NaClO2纯度的测定:用“间接碘量法”测定样品(杂质与I-不发生反应)的纯度,过程如下:取样品1.810g配制成250mL溶液,从中取出25.00mL;加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液(已知:ClO
 +4I-+4H+=2H2O+2I2+Cl-),然后用cmol•L-1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O
+4I-+4H+=2H2O+2I2+Cl-),然后用cmol•L-1Na2S2O3标准溶液滴定至终点,重复2次,测得消耗标准溶液的体积平均值为VmL(已知:I2+2S2O =S4O
=S4O +2I-)。样品中NaClO2的纯度为
+2I-)。样品中NaClO2的纯度为
您最近一年使用:0次
2023-10-27更新
|
1110次组卷
|
5卷引用:广西部分高中2024届高三第一次摸底测试化学试题
广西部分高中2024届高三第一次摸底测试化学试题广西南宁市2024届高三上学期毕业班摸底测试化学试题(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)江西省赣州市全南中学2023-2024学年高三上学期11月期中考试化学试题河北省衡水市武邑中学2023-2024学年高三上学期12月期中考试化学试题
2022高三·全国·专题练习
6 . 某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种短周期元素组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为地壳中含量最多的元素。下列说法正确的是
A.简单氢化物沸点: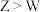 | B.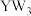 分子的空间构型为三角锥形 分子的空间构型为三角锥形 |
C.原子半径: | D.最高价氧化物对应水化物的碱性: |
您最近一年使用:0次
2023-02-20更新
|
6216次组卷
|
12卷引用:广西大学附属中学2023-2024学年高二下学期4月月考化学试题
广西大学附属中学2023-2024学年高二下学期4月月考化学试题广西区南宁市第三十六中学2022-2023学年高二下学期第三次月考化学试题(已下线)专题06 物质结构元素周期律-2022年高考真题模拟题分项汇编2022年福建省高考真题化学试题(已下线)2022年福建省高考真题变式题(选择题1-5)(已下线)广东省深圳市2022-2023学年高三第一次调研考试变式题(选择题1-16)福建省龙岩市连城县第一中学2022-2023学年高二下学期5月月考化学试题(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)



