解题方法
1 . (1)氮化硼(BN)是一种用途广泛的无机非金属材料,常见有立方氮化硼与六方氮化硼两种结构。六方氮化硼是一种白色难熔的耐高温物质,它具有类似石墨层状结构,被成为白石墨,常用作润滑剂,虽然六方氮化硼结构与石墨相似,但六方氮化硼却并不导电,具有优良的绝缘性能。立方氮化硼是棕色或暗红色的晶体,为闪锌矿结构,硬度仅次于金刚石,具有很高的热稳定性和化学惰性,因此,立方氮化硼磨具的磨削性能十分优异。
①写出氮化硼中B和N的基态电子排布式_______ 。
②氮化硼非常稳定,在红热时才能与水蒸气发生水解反应,写出该化学方程式_______ 。
③H3BO3是一元酸,试从分子结构角度解释原因_______ 。
④判断六方氮化硼中B与N的杂化类型_______ 、_______ 。
⑤从化学键角度解释为什么六方氮化硼的结构与石墨相似,但六方氮化硼却并不导电_______ 。
(2)PH3可由白磷(P4)和氢气反应生成。已知键能:P-P:213kJ·mol-1,H-H:435kJ·mol-1,P-H:326kJ·mol-1。
①画出白磷的结构式(空间结构)_______ 。
②写出所对应反应的化学方程式_______ 。
③根据键能计算该反应的焓变(反应物和产物均为气态,写出简要的计算过程)_______ 。
(3)锡的利用在我国有几千年历史,青铜器中就含有锡,殷墟中还出土过锡制品。锡的熔点232℃,有两种常见的同素异形体一白锡和灰锡,二者在一定温度下可以相互转化。
①锡的密度为7.28g·cm-3,晶胞参数a=583pmc=318pm,延展性好,质软。通过计算求出一个白锡晶胞中的锡原子数_______ 。
②灰锡的密度为5.75g·cm-3,有金刚石的结构。灰锡和白锡的部分热力学数据如下:
通过计算说明常温(25℃)时,灰锡和白锡哪种更稳定_______ ;
③锡做的茶叶罐不能放在冰箱中冷冻保存,通过计算说明原因_______ 。
①写出氮化硼中B和N的基态电子排布式
②氮化硼非常稳定,在红热时才能与水蒸气发生水解反应,写出该化学方程式
③H3BO3是一元酸,试从分子结构角度解释原因
④判断六方氮化硼中B与N的杂化类型
⑤从化学键角度解释为什么六方氮化硼的结构与石墨相似,但六方氮化硼却并不导电
(2)PH3可由白磷(P4)和氢气反应生成。已知键能:P-P:213kJ·mol-1,H-H:435kJ·mol-1,P-H:326kJ·mol-1。
①画出白磷的结构式(空间结构)
②写出所对应反应的化学方程式
③根据键能计算该反应的焓变(反应物和产物均为气态,写出简要的计算过程)
(3)锡的利用在我国有几千年历史,青铜器中就含有锡,殷墟中还出土过锡制品。锡的熔点232℃,有两种常见的同素异形体一白锡和灰锡,二者在一定温度下可以相互转化。
①锡的密度为7.28g·cm-3,晶胞参数a=583pmc=318pm,延展性好,质软。通过计算求出一个白锡晶胞中的锡原子数
②灰锡的密度为5.75g·cm-3,有金刚石的结构。灰锡和白锡的部分热力学数据如下:
 /kJ·mol-1 /kJ·mol-1 |  J/-1·K-1·mol-1 J/-1·K-1·mol-1 | |
| Sn(灰) Sn(白) | -2.12 0 | 44.15 51.55 |
通过计算说明常温(25℃)时,灰锡和白锡哪种更稳定
③锡做的茶叶罐不能放在冰箱中冷冻保存,通过计算说明原因
您最近一年使用:0次
12-13高三·湖北襄阳·阶段练习
2 . VA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含VA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)白磷单质的中P原子采用的轨道杂化方式是______ 。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______ 。
(3)As原子序数为__ ,其核外M层和N层电子的排布式为__ 。
(4)NH3的沸点比PH3___ (填“高”或“低”),原因是__ ,PO 离子的立体构型为
离子的立体构型为___ 。
(5)H3PO4的K1、K2、K3分别为7.6×10﹣3、6.3×10﹣8、4.4×10﹣13.硝酸完全电离,而亚硝酸K=5.1×10﹣4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因___ ;
②硝酸比亚硝酸酸性强的原因___ ;
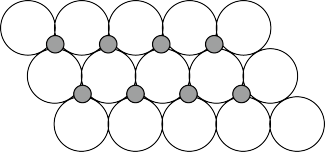
(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为__ cm(用含有a的代数式表示),在一定温度下NiO晶体可以自发地分散并形成“单分子层”(如图),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为__ g(氧离子的半径为1.40×10﹣10m)。
(1)白磷单质的中P原子采用的轨道杂化方式是
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为
(3)As原子序数为
(4)NH3的沸点比PH3
 离子的立体构型为
离子的立体构型为(5)H3PO4的K1、K2、K3分别为7.6×10﹣3、6.3×10﹣8、4.4×10﹣13.硝酸完全电离,而亚硝酸K=5.1×10﹣4,请根据结构与性质的关系解释:
①H3PO4的K1远大于K2的原因
②硝酸比亚硝酸酸性强的原因
(6)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为

您最近一年使用:0次



