1 . 党的二十大报告中强调“实现碳达峰碳中和是一场广泛而深刻的经济社会系统性变革”。 的转化和利用是实现碳中和的有效途径。回答下列问题。
的转化和利用是实现碳中和的有效途径。回答下列问题。
I.利用 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
① ,
,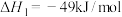
② ,
,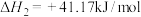
③ ,
,
(1)反应③中
___________ ,若要该反应自发进行,___________ (填“高温”或“低温”)更有利。
(2)在恒温,恒容密闭容器中,对于反应③,下列说法中能说明该反应达到化学平衡状态的是___________(填字母序号)。
(3)在催化剂作用下,按的 比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为6.4MPa,测得不同温度下,反应经过相同时间时
比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为6.4MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:
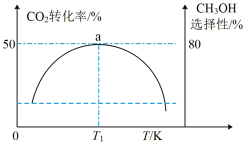
已知:甲醇的选择性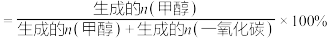
①从图中曲线的变化趋势也可以判断出反应①是放热的,判断的依据是___________ 。
② K时,若反应从开始到达到a点所用时间为5min,
K时,若反应从开始到达到a点所用时间为5min,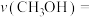
___________  ,反应②的
,反应②的
___________ ( 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数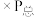 ,最终结果用分数表示)。
,最终结果用分数表示)。
II.
(4)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与 形成黄色的配合物,其同分异构体水杨醛缩对氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩对氨基苯酚(B),沸点较高的是___________ (填“A”或“B”),原因是___________ 。
A.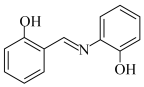 B.
B.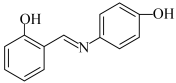
(5)吡啶(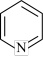 )具有类似于苯环的平面结构,已知N原子电子云密度越大,碱性越强。下列关于吡啶的说法正确的是___________(填标号)。
)具有类似于苯环的平面结构,已知N原子电子云密度越大,碱性越强。下列关于吡啶的说法正确的是___________(填标号)。
(6)2001年德国专家从硫酸铵中检出一种组成为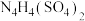 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和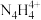 两种离子的形式存在。
两种离子的形式存在。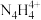 中N原子均为
中N原子均为 杂化,请写出
杂化,请写出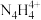 的结构式:
的结构式:___________ 。
 的转化和利用是实现碳中和的有效途径。回答下列问题。
的转化和利用是实现碳中和的有效途径。回答下列问题。I.利用
 合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:
合成淀粉的研究成果已经被我国科学家发表在Nature杂志上。其涉及的关键反应如下:①
 ,
,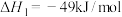
②
 ,
,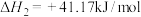
③
 ,
,
(1)反应③中

(2)在恒温,恒容密闭容器中,对于反应③,下列说法中能说明该反应达到化学平衡状态的是___________(填字母序号)。
| A.混合气体的平均相对分子质量不再变化 |
| B.混合气体的密度不再变化 |
C.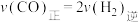 |
D.CO、 、 、 的物质的量之比为1∶2∶1 的物质的量之比为1∶2∶1 |
 比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为6.4MPa,测得不同温度下,反应经过相同时间时
比例向某密闭容器中通入一定量的原料气只发生①②两个反应。维持压强为6.4MPa,测得不同温度下,反应经过相同时间时 的转化率、甲醇的选择性如图所示:
的转化率、甲醇的选择性如图所示:
已知:甲醇的选择性
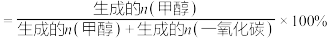
①从图中曲线的变化趋势也可以判断出反应①是放热的,判断的依据是
②
 K时,若反应从开始到达到a点所用时间为5min,
K时,若反应从开始到达到a点所用时间为5min,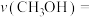
 ,反应②的
,反应②的
 指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数
指用平衡分压代替平衡浓度进行计算的平衡常数,A的平衡分压=A的物质的量分数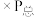 ,最终结果用分数表示)。
,最终结果用分数表示)。II.
(4)水杨醛缩邻氨基苯酚(A)又被称为“锰试剂”,可与
 形成黄色的配合物,其同分异构体水杨醛缩对氨基苯酚(B),沸点较高的是
形成黄色的配合物,其同分异构体水杨醛缩对氨基苯酚(B),沸点较高的是A.
 B.
B.
(5)吡啶(
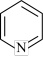 )具有类似于苯环的平面结构,已知N原子电子云密度越大,碱性越强。下列关于吡啶的说法正确的是___________(填标号)。
)具有类似于苯环的平面结构,已知N原子电子云密度越大,碱性越强。下列关于吡啶的说法正确的是___________(填标号)。A.吡啶中含有与苯类似的大π键 |
| B.吡啶中N原子的价层孤电子对占据2p轨道 |
C.3-甲基吡啶( )的碱性大于吡啶 )的碱性大于吡啶 |
| D.吡啶在水中的溶解度大于苯在水中的溶解度 |
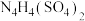 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以 和
和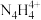 两种离子的形式存在。
两种离子的形式存在。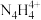 中N原子均为
中N原子均为 杂化,请写出
杂化,请写出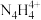 的结构式:
的结构式:
您最近一年使用:0次
解题方法
2 . 劳拉替尼(K)是第三代靶向药,具有抗癌作用,其合成路线如下(部分条件已省略)。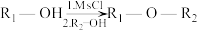
 的反应类型为
的反应类型为___________ 。
(2)E中含氧官能团的名称为___________ 。
(3) 过程中生成
过程中生成 ,其化学方程式为
,其化学方程式为___________ 。
(4)下列说法中正确的是___________ 。(填序号)
a.D中有手性碳原子
b.E既可以与稀HCl反应,也可以与NaOH溶液反应
c.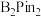 中B(硼)和C(碳)都是
中B(硼)和C(碳)都是 杂化
杂化
(5)由J生成K经历三步反应,具体条件和转化关系如图所示。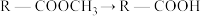 、
、___________ 。
②中间产物2在HATU条件下产生相对分子质量为n、2n、3n、…的不同产物,其中K的相对分子质量为n,K的结构简式为___________ 。
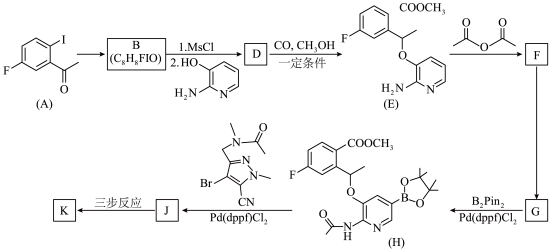
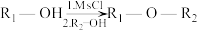
②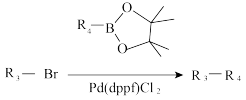
③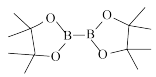 可用
可用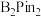 表示
表示
 的反应类型为
的反应类型为(2)E中含氧官能团的名称为
(3)
 过程中生成
过程中生成 ,其化学方程式为
,其化学方程式为(4)下列说法中正确的是
a.D中有手性碳原子
b.E既可以与稀HCl反应,也可以与NaOH溶液反应
c.
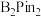 中B(硼)和C(碳)都是
中B(硼)和C(碳)都是 杂化
杂化(5)由J生成K经历三步反应,具体条件和转化关系如图所示。

已知: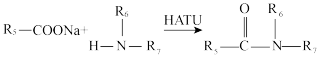 (
(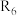 、
、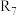 均不为H)
均不为H)
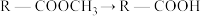 、
、②中间产物2在HATU条件下产生相对分子质量为n、2n、3n、…的不同产物,其中K的相对分子质量为n,K的结构简式为
您最近一年使用:0次
名校
3 . 有机物G是合成中草药活性成分Psoralidin的中间体,其合成路线如下:
(1)化合物A的名称为______ ;C中官能团的名称为______ 。
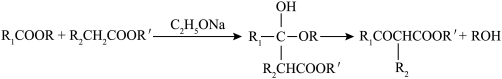
(2)结合已有知识,写出E→F的方程式:______ ;该反应类型为______ 。
(3)下列关于反应F→G的说法中,正确的有______
(4)化合物E的芳香族同分异构体中,同时满足如下条件的有______ 种,
a)只含一种官能团且能与碳酸钠反应生成 ;
;
b)核磁共振氢谱确定分子中有9个化学环境相同的氢原子。
其中核磁共振氢谱有4组峰的结构简式为______ 。(写出一种即可)
(5)对甲氧基苯甲酸(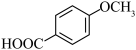 )可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备
)可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备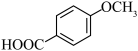 的合成路线
的合成路线____ 。

(1)化合物A的名称为
(2)结合已有知识,写出E→F的方程式:
(3)下列关于反应F→G的说法中,正确的有______
| A.反应过程中有极性键、非极性键的断裂和形成 |
| B.化合物F存在顺反异构体 |
| C.该反应有乙醇生成 |
| D.化合物G中碳原子的杂化方式有两种 |
(4)化合物E的芳香族同分异构体中,同时满足如下条件的有
a)只含一种官能团且能与碳酸钠反应生成
 ;
;b)核磁共振氢谱确定分子中有9个化学环境相同的氢原子。
其中核磁共振氢谱有4组峰的结构简式为
(5)对甲氧基苯甲酸(
 )可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备
)可用作防腐剂或制备香料,结合上述信息,写出以苯酚为主要原料制备 的合成路线
的合成路线
您最近一年使用:0次
2024-04-28更新
|
674次组卷
|
2卷引用:广东省汕头市2024届高三二模考试化学试
解题方法
4 . “超导铜”是一种含1%的纳米碳管和99%的铜的合成材料,该材料的导电率约超出纯铜线缆一倍。回答下列问题:
(1)基态Cu原子的电子排布式为____ ,其在周期表是位置为____ 。
(2)硫酸铜溶于水后形成水合铜离子的结构式为____ ,向硫酸铜溶液中逐滴加入氨水直至过量,观察到的现象为____ 。
(3)氨酸络合剂指含有—N(CH2COOH)2基团的有机化合物,它是一类具有广泛络合性能和强的常合能力的络合剂,I、II、III都可以与Cu2+形成络合物。

①预测____ (填编号“I”、“II”、“III”)与Cu2+形成的络合物最稳定。
②下列说法正确的有____ 。
A.I、II、III中N原子的杂化类型都是sp3
B.III中碳氧键的键能均相等
C.III中C—N—C键角小于107.3°
(4)+1价Cu的化合物CsxCuyXz(X=Cl,Br,I)晶体中阴离子存在如图所示链状结构,该结构是[CuX4]-四面体通过共用____ (填“顶点”或“棱”或“面”)而形成的,该晶体的化学式为____ 。

(1)基态Cu原子的电子排布式为
(2)硫酸铜溶于水后形成水合铜离子的结构式为
(3)氨酸络合剂指含有—N(CH2COOH)2基团的有机化合物,它是一类具有广泛络合性能和强的常合能力的络合剂,I、II、III都可以与Cu2+形成络合物。

①预测
②下列说法正确的有
A.I、II、III中N原子的杂化类型都是sp3
B.III中碳氧键的键能均相等
C.III中C—N—C键角小于107.3°
(4)+1价Cu的化合物CsxCuyXz(X=Cl,Br,I)晶体中阴离子存在如图所示链状结构,该结构是[CuX4]-四面体通过共用

您最近一年使用:0次
解题方法
5 . (A)在晶体中,微观粒子是有规律排布的。而实际上的晶体与理想结构或多或少会产生偏离,这种偏离称为晶体的缺陷。由于晶体缺陷,氧化铁FexO中的x常常不确定。
(1)请写出铁原子基态电子排布式______ 。
(2)Fe2+与Fe3+相比,较稳定的是_____ ,请从二者结构上加以解释__________ 。
(3)硫氰根离子和异硫氰根离子都可用SCN-表示,碳原子都处于中央,则碳原子的轨道杂化类型为_____ 。其中异硫氰根离子与CO2是等电子体,异硫氰根离子的电子式为__________ 。Fe3+与SCN―可以形成配位数1~6的配离子,若Fe3+与SCN―以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为_________________________ 。
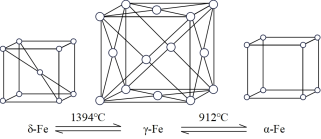
(4)如图:铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是____
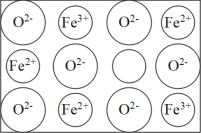
(5)FexO有NaCl结构的晶胞。今有某种FexO晶体中就存在如图所示的缺陷,其密度为5.71 g·cm-3,晶胞棱长为a=4.28×10-8cm(已知:4.283=78.4),则x=______ 。
(1)请写出铁原子基态电子排布式
(2)Fe2+与Fe3+相比,较稳定的是
(3)硫氰根离子和异硫氰根离子都可用SCN-表示,碳原子都处于中央,则碳原子的轨道杂化类型为
(4)如图:铁有δ、γ、α三种同素异形体,三种晶体在不同温度下能发生转化。下列说法不正确的是____

| A.γ-Fe晶体中,铁原子的配位数为12 |
| B.δ-Fe晶体和α-Fe晶体都是非密置在三维空间堆积而成的,堆积后非密置层都保持原来的结构不变 |
| C.三种晶体的空间利用率大小为:γ-Fe晶体>δ-Fe晶体>α-Fe晶体 |
D.三种晶胞的棱长之比为: |

您最近一年使用:0次



