名校
1 . 下列说法不正确的是
A.CO 、NO 、NO 、SO 、SO 中心原子都是sp2杂化 中心原子都是sp2杂化 |
| B.NH3、PCl3、H3O+的空间结构都是三角锥 |
| C.CO2、SO3都是由极性键构成的非极性分子 |
| D.CH2=CHCN分子中的σ键和π键的比为2∶1 |
您最近一年使用:0次
名校
解题方法
2 . 我国科学家制备了一种ZnPc/C60太阳能电池,其结构示意图如下。
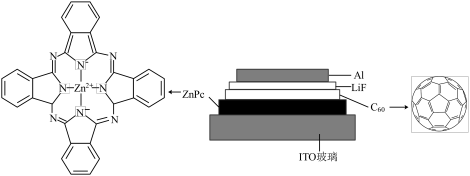
(1)铝元素属于_____________ 区(填“s”“d”“ ”或“p”)。
”或“p”)。
(2)C60分子中60个碳原子都是等价的,均以近似_____________ 杂化的方式形成3个不共平面的σ键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,π电子云分布在C60分子笼的内外层表面上。循环伏安测试表明:C60在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
(3)①ZnPc中Zn2+的价层电子排布式是_____________ 。
②ZnPc中存在配位键的原因是_____________ 。
(4)某溶剂中,ZnPc可以和C60形成分子间电荷转移复合物,反应方程式可表示为:ZnPc+C60 ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。
ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。
反应:ZnPc+C60 ZnPc-C60△H
ZnPc-C60△H_____________ 0(填“>”或“<”),ZnPc-C60中ZnPc是电子_____________ (填“给体”或“受体”)。
(5)LiF晶体结构属于氯化钠型,其晶胞结构如图所示。
①LiF的熔点和沸点比NaCl的高,请解释原因_____________ 。
②LiF晶体的密度约为2.6g/cm3,LiF晶胞的体积约为_____________ cm3(计算结果保留一位有效数字)。


(1)铝元素属于
 ”或“p”)。
”或“p”)。(2)C60分子中60个碳原子都是等价的,均以近似
(3)①ZnPc中Zn2+的价层电子排布式是
②ZnPc中存在配位键的原因是
(4)某溶剂中,ZnPc可以和C60形成分子间电荷转移复合物,反应方程式可表示为:ZnPc+C60
 ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。
ZnPc-C60,不同温度下生成电荷转移复合物的平衡常数如下表。温度 | 生成ZnPc-C60的K |
24℃ | 1.2329 |
44℃ | 0.9674 |
64℃ | 0.4923 |
 ZnPc-C60△H
ZnPc-C60△H(5)LiF晶体结构属于氯化钠型,其晶胞结构如图所示。
①LiF的熔点和沸点比NaCl的高,请解释原因
②LiF晶体的密度约为2.6g/cm3,LiF晶胞的体积约为

您最近一年使用:0次
2023-01-05更新
|
448次组卷
|
5卷引用:北京市石景山区2022-2023学年高三上学期期末考试化学试题
名校
3 . 2022年诺贝尔化学奖授予了对点击化学和生物正交化学做出贡献的三位科学家。点击化学的代表反应为铜([Cu])催化的叠氮-炔基Husigen成环反应,其反应原理如下图所示。下列说法正确的是


| A.[Cu]能降低反应的活化能 | B.基态 的价电子排布式为 的价电子排布式为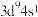 |
| C.转化过程中N的杂化方式未改变 | D.该总反应的反应类型属于取代反应 |
您最近一年使用:0次
名校
4 . 二氟卡宾(: )作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以生成
)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以生成 ,反应历程如图所示:
,反应历程如图所示:

下列叙述错误的是
 )作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以生成
)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以生成 ,反应历程如图所示:
,反应历程如图所示:
下列叙述错误的是
A. 中C原子为 中C原子为 杂化,1个 杂化,1个 分子中存在3个 分子中存在3个 键,1个 键,1个 键 键 |
B. 和 和 生成 生成 反应的 反应的 |
C.决定整个反应速率的步骤是   |
| D.上述反应历程中存在S—S的断裂和生成 |
您最近一年使用:0次
名校
5 . 下图是某种偶氮苯X和Y的结构简式,有关说法正确的是


| A.X与Y互为同分异构体 | B.Y的化学式为 |
C.X分子中C均为 杂化 杂化 | D.X与Y互为同系物 |
您最近一年使用:0次
2022-11-07更新
|
251次组卷
|
2卷引用:北京市第八十中学2022-2023学年高三上学期期末测试化学试题
名校
6 . 下列关于HCHO及构成微粒的化学用语或图示表达不正确 的是
A.O的原子结构示意图: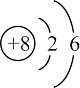 | B.基态C原子的轨道表示式: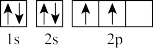 |
C.C原子杂化轨道示意图: | D.HCHO的分子结构模型: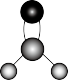 |
您最近一年使用:0次
2022-11-04更新
|
346次组卷
|
4卷引用:北京十中2022-2023学年高三上学期期末统练3化学试题
名校
解题方法
7 . 某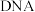 分子的片段如图所示。下列关于该片段的说法
分子的片段如图所示。下列关于该片段的说法不正确 的是

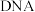 分子的片段如图所示。下列关于该片段的说法
分子的片段如图所示。下列关于该片段的说法
| A.图示片段包含1个胞嘧啶、1个鸟嘌呤 |
B.该片段中所有氮原子都采取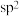 杂化 杂化 |
| C.该片段在一定条件下可发生水解反应 |
| D.若脱氧核糖中3号C所连羟基被还原为H原子,其参与形成的核苷酸将无法聚合为核酸 |
您最近一年使用:0次
2022-10-20更新
|
512次组卷
|
3卷引用:北京市第八十中学2022-2023学年高三上学期期末测试化学试题
北京市第八十中学2022-2023学年高三上学期期末测试化学试题北京市中国人民大学附属中学2022-2023学年高三上学期期中考试化学模拟试卷试题(已下线)模拟卷08-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
名校
解题方法
8 . H2O2是常用的氧化剂,其分子结构如下图所示,两个氢原子犹如在半展开的书的两面上。下列说法不正确 的是
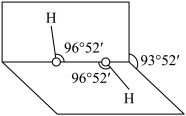
| A.在H2O2分子中只有σ键没有π键 |
| B.H2O2为非极性分子,O原子采取sp3杂化轨道成键 |
| C.H2O2能与水混溶,不溶于CCl4 |
| D.H2O2分子间作用力强于H2O分子间作用力 |
您最近一年使用:0次
2022-09-09更新
|
421次组卷
|
6卷引用:北京市石景山区2021-2022学年高二下学期期末考试化学试题
北京市石景山区2021-2022学年高二下学期期末考试化学试题湖南省株洲市第八中学2023届高三上学期第一次月考化学试题天津市红桥区2022-2023学年高二下学期期末考试化学试题(已下线)专题01 物质的结构与性质-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)湖南省攸县第一中学2022-2023学年高三第五次月考化学试题湖南省株洲市第八中学2022-2023学年高三上学期第五次月考化学试题
解题方法
9 . 碳纳米管是一种具有特殊结构的材料,具有许多异常的力学、电学和化学性能。近些年随着碳纳米管及纳米材料研究的深入,其广阔的应用前景也不断地展现出来。下列关于纳米管说法不正确 的是


| A.碳纳米管具有导电、熔点高等特点 |
| B.纳米管是一种新型有机材料 |
| C.纳米管中C原子的杂化方式为sp2 |
| D.纳米管孔径较大,可以掺杂各种金属原子,体现特殊的催化活性 |
您最近一年使用:0次
10 . 中学常见的6种有机化合物:乙烷、乙烯、1-溴丙烷、1-丙醇、乙酸、乙酸乙酯。
(1)物质结构
① 6种物质的分子中只含有σ键的是___________ 。
② 6种物质中,碳原子的杂化方式均为sp2杂化的是___________ 。
(2)物理性质
①常温下,乙醇的溶解性大于苯酚,从结构角度分析其原因:___________ 。
②从物质结构角度解释乙酸的沸点高于1-丙醇的原因:___________ 。
(3)反应类型
①1-溴丙烷生成丙烯的化学方程式为___________ ,反应类型为___________ 。
②1-溴丙烷与氨气发生取代反应的产物中,有机化合物的结构简式可能是___________ 。
(4)物质制备
乙酸乙酯广泛用于药物、染料、香料等工业。实验室用无水乙醇、冰醋酸和浓硫酸反应可制备乙酸乙酯,常用装置如下图。

①写出无水乙醇、冰醋酸和浓硫酸反应制备乙酸乙酯的化学方程式___________ 。
②试管X中的试剂为___________ 。
③为提高反应速率或限度,实验中采取的措施及对应理由不正确 的是___________ (填字母)。
a.浓硫酸可做催化剂,提高化学反应速率
b.浓硫酸可做吸水剂,促进反应向生成乙酸乙酯的反应移动
c.已知该反应为放热反应,升高温度可同时提高化学反应速率和反应限度
④ 写出3种不同物质类别的乙酸乙酯的同分异构体的结构简___________ 、___________ 、___________ 。
(1)物质结构
① 6种物质的分子中只含有σ键的是
② 6种物质中,碳原子的杂化方式均为sp2杂化的是
(2)物理性质
①常温下,乙醇的溶解性大于苯酚,从结构角度分析其原因:
②从物质结构角度解释乙酸的沸点高于1-丙醇的原因:
| 物质 | 相对分子质量 | 沸点 |
| 1-丙醇 | 60 | 97.4℃ |
| 乙酸 | 60 | 118℃ |
(3)反应类型
①1-溴丙烷生成丙烯的化学方程式为
②1-溴丙烷与氨气发生取代反应的产物中,有机化合物的结构简式可能是
(4)物质制备
乙酸乙酯广泛用于药物、染料、香料等工业。实验室用无水乙醇、冰醋酸和浓硫酸反应可制备乙酸乙酯,常用装置如下图。

①写出无水乙醇、冰醋酸和浓硫酸反应制备乙酸乙酯的化学方程式
②试管X中的试剂为
③为提高反应速率或限度,实验中采取的措施及对应理由
a.浓硫酸可做催化剂,提高化学反应速率
b.浓硫酸可做吸水剂,促进反应向生成乙酸乙酯的反应移动
c.已知该反应为放热反应,升高温度可同时提高化学反应速率和反应限度
④ 写出3种不同物质类别的乙酸乙酯的同分异构体的结构简
您最近一年使用:0次



