1 . 氮化硼晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
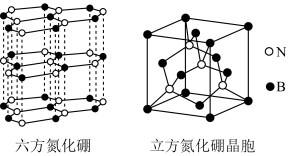
| A.六方氮化硼与立方氮化硼互为同素异形体 |
B.立方相氮化硼含有 键和 键和 键,所以硬度大 键,所以硬度大 |
C.六方、立方相氮化硼晶体的化学式均为BN,硼原子的杂化类型分别为 、 、 |
| D.两种晶体中既有极性键又有非极性键 |
您最近一年使用:0次
2 . 科研人员利用 作催化剂,在光照条件下实现了
作催化剂,在光照条件下实现了 和
和 合成甲醇
合成甲醇 ,该反应历程示意图如下。
,该反应历程示意图如下。不正确 的是
 作催化剂,在光照条件下实现了
作催化剂,在光照条件下实现了 和
和 合成甲醇
合成甲醇 ,该反应历程示意图如下。
,该反应历程示意图如下。
| A.过程Ⅱ中存在极性键的断裂与形成 |
B.过程Ⅴ中生成 时吸收能量 时吸收能量 |
C.总反应的化学方程式是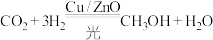 |
| D.在催化反应的过程中,C原子的杂化类型发生改变 |
您最近一年使用:0次
解题方法
3 . 将钴酞菁和三氯化铝复合嵌接在碳纳米管上,制得一种高效催化还原二氧化碳的催化剂。回答下列问题:
(1)碳的几种单质如图1所示。
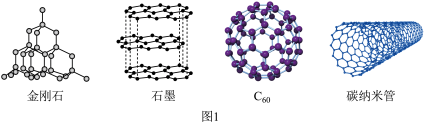
①几种碳的单质中属于共价晶体的是________ 。
② 间的作用力是
间的作用力是______ 。
③基态碳原子价层电子排布式为_________ 。
(2)钴酞菁的分子结构如图2所示。

①比较C原子和N原子的电负性大小,并从原子结构的角度说明理由________ 。
②钴酞菁分子中能形成配位键的原因是________ 。
(3)气态 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图3所示。
的形式存在,其空间结构如图3所示。 结构属立方晶系,晶胞如图4所示。
结构属立方晶系,晶胞如图4所示。

①二聚体中的 轨道杂化类型为
轨道杂化类型为________ 。
② 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的熔点192℃,原因是
的熔点192℃,原因是_________ 。
③ 晶体距离
晶体距离 最近的阳离子有
最近的阳离子有____ 个。
④ 的晶胞形状为正方体,边长为
的晶胞形状为正方体,边长为 ,该晶体密度为
,该晶体密度为_____  。(列出计算式,阿伏加德罗常数用
。(列出计算式,阿伏加德罗常数用 表示,
表示, )
)
(1)碳的几种单质如图1所示。

①几种碳的单质中属于共价晶体的是
②
 间的作用力是
间的作用力是③基态碳原子价层电子排布式为
(2)钴酞菁的分子结构如图2所示。

①比较C原子和N原子的电负性大小,并从原子结构的角度说明理由
②钴酞菁分子中能形成配位键的原因是
(3)气态
 通常以二聚体
通常以二聚体 的形式存在,其空间结构如图3所示。
的形式存在,其空间结构如图3所示。 结构属立方晶系,晶胞如图4所示。
结构属立方晶系,晶胞如图4所示。
①二聚体中的
 轨道杂化类型为
轨道杂化类型为②
 的熔点为1090℃,远高于
的熔点为1090℃,远高于 的熔点192℃,原因是
的熔点192℃,原因是③
 晶体距离
晶体距离 最近的阳离子有
最近的阳离子有④
 的晶胞形状为正方体,边长为
的晶胞形状为正方体,边长为 ,该晶体密度为
,该晶体密度为 。(列出计算式,阿伏加德罗常数用
。(列出计算式,阿伏加德罗常数用 表示,
表示, )
)
您最近一年使用:0次
名校
解题方法
4 . 我国科学家从中国特有的喜树中分离得到具有肿瘤抑制作用的喜树碱,结构如图。下列关于喜树碱的说法不正确 的是

A.分子中N原子有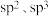 两种杂化方式 两种杂化方式 |
| B.分子中不含有手性碳原子 |
C.羟基中 的极性强于乙基中 的极性强于乙基中 的极性 的极性 |
D.带*的氮原子有孤电子对,能与含空轨道的 以配位键结合 以配位键结合 |
您最近一年使用:0次
2024-01-14更新
|
839次组卷
|
6卷引用:北京市中国人民大学附属中学2023-2024学年高三上学期期末考前化学练习
名校
解题方法
5 . 胆矾(CuSO4•5H2O)的结构示意图如图所示。下列说法不 正确的是
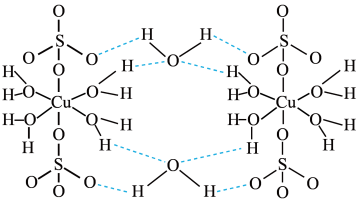
A.基态Cu2+的价层电子轨道表示式是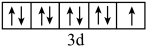 |
B.SO 中的O-S-O的键角小于H2O中的H-O-H的键角 中的O-S-O的键角小于H2O中的H-O-H的键角 |
| C.H2O中氧原子的VSEPR的价层电子对数是4 |
D.胆矾中的H2O与Cu2+、H2O与SO 的作用力分别为配位键和氢键 的作用力分别为配位键和氢键 |
您最近一年使用:0次
2023-10-22更新
|
355次组卷
|
6卷引用:北京市东城区2022-2023学年高二下学期期末检测化学试题
6 . 有下列五种物质:
① ②
② ③CH3OH④CH3COOH⑤
③CH3OH④CH3COOH⑤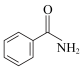
回答问题(1)~(4):
(1)①中碳原子杂化方式分别是_____ 。②中官能团名称是_____ 。
(2)写出②转化成丙烯的化学方程式_____ 。
(3)写出③与④反应的化学方程式_____ 。
(4)⑤在氢氧化钠溶液中反应的化学方程式是_____ 。
(5)下列三组物质能用酸性高锰酸钾溶液鉴别的一组物质是_____ (填字母序号)。
a.乙烯和乙炔 b.乙烯和乙烷 c.苯和环己烷
(6)普伐他汀是一种调节血脂的药物,其结构如图所示。下列关于普伐他汀的性质描述正确的是_____ (填字母序号)。
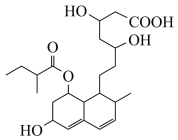
a.该物质能与Na、NaHCO3发生反应
b.能与FeCl3溶液发生显色反应
c.能发生加成、取代、消去反应
d.1mol该物质最多可与1molNaOH反应
①
 ②
② ③CH3OH④CH3COOH⑤
③CH3OH④CH3COOH⑤
回答问题(1)~(4):
(1)①中碳原子杂化方式分别是
(2)写出②转化成丙烯的化学方程式
(3)写出③与④反应的化学方程式
(4)⑤在氢氧化钠溶液中反应的化学方程式是
(5)下列三组物质能用酸性高锰酸钾溶液鉴别的一组物质是
a.乙烯和乙炔 b.乙烯和乙烷 c.苯和环己烷
(6)普伐他汀是一种调节血脂的药物,其结构如图所示。下列关于普伐他汀的性质描述正确的是

a.该物质能与Na、NaHCO3发生反应
b.能与FeCl3溶液发生显色反应
c.能发生加成、取代、消去反应
d.1mol该物质最多可与1molNaOH反应
您最近一年使用:0次
2023-07-27更新
|
165次组卷
|
2卷引用:北京市大兴区2022-2023学年高二下学期期末考试化学试题
7 . 主族元素N、Si、F、Cl、Se、Ca等的某些化合物对工农业生产意义重大。
(1) 陶瓷具有硬度大、强度高、耐高温等性质,其晶体类型为
陶瓷具有硬度大、强度高、耐高温等性质,其晶体类型为___________ 。
(2) 的熔、沸点低于
的熔、沸点低于 ,原因是
,原因是___________ 。
(3)硒元素位于元素周期表中___________ (选填s、p、d、f、ds)区,基态硒原子核外电子云轮廓图呈球形、哑铃形的能级上电子数之比为___________ 。
(4) 的中心原子杂化方式为
的中心原子杂化方式为___________ , 的空间构型是
的空间构型是___________ ,与 互为等电子体的微粒有
互为等电子体的微粒有___________ (写一种微粒即可)。
(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ ;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,将原子位置的坐标表示为晶胞棱长的分数,称作原子的分数坐标。ZnSe晶胞中部分原子的分数坐标:A点为 、B点为
、B点为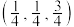 ,则C点原子的分数坐标为
,则C点原子的分数坐标为___________ 。

(6)已知: 称为羟基,无机含氧酸(
称为羟基,无机含氧酸( )分子结构中含有羟基,如果成酸元素R相同,含氧酸分子中非羟基氧个数越多,R的正电性越高,导致
)分子结构中含有羟基,如果成酸元素R相同,含氧酸分子中非羟基氧个数越多,R的正电性越高,导致 中的O的电子向R偏移,
中的O的电子向R偏移,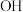 键极性增强,因而在水分子的作用下,也就越容易电离出
键极性增强,因而在水分子的作用下,也就越容易电离出 ,即酸性越强。也就是说,无机含氧酸的酸性随着分子中连接在中心原子R上的非羟基氧的个数增多而增强。
,即酸性越强。也就是说,无机含氧酸的酸性随着分子中连接在中心原子R上的非羟基氧的个数增多而增强。
亚磷酸( )为弱酸,分子结构中含有一个非羟基氧,其酸性比HClO的酸性
)为弱酸,分子结构中含有一个非羟基氧,其酸性比HClO的酸性___________ (填“强”或“弱”), 与过量NaOH溶液反应的离子方程式为
与过量NaOH溶液反应的离子方程式为___________ 。
(7)萤石( )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
)是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是___________ ,若该立方晶胞参数为acm,阴、阳离子的核间距最小为___________ cm。

(1)
 陶瓷具有硬度大、强度高、耐高温等性质,其晶体类型为
陶瓷具有硬度大、强度高、耐高温等性质,其晶体类型为(2)
 的熔、沸点低于
的熔、沸点低于 ,原因是
,原因是(3)硒元素位于元素周期表中
(4)
 的中心原子杂化方式为
的中心原子杂化方式为 的空间构型是
的空间构型是 互为等电子体的微粒有
互为等电子体的微粒有(5)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
 、B点为
、B点为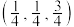 ,则C点原子的分数坐标为
,则C点原子的分数坐标为
(6)已知:
 称为羟基,无机含氧酸(
称为羟基,无机含氧酸( )分子结构中含有羟基,如果成酸元素R相同,含氧酸分子中非羟基氧个数越多,R的正电性越高,导致
)分子结构中含有羟基,如果成酸元素R相同,含氧酸分子中非羟基氧个数越多,R的正电性越高,导致 中的O的电子向R偏移,
中的O的电子向R偏移,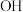 键极性增强,因而在水分子的作用下,也就越容易电离出
键极性增强,因而在水分子的作用下,也就越容易电离出 ,即酸性越强。也就是说,无机含氧酸的酸性随着分子中连接在中心原子R上的非羟基氧的个数增多而增强。
,即酸性越强。也就是说,无机含氧酸的酸性随着分子中连接在中心原子R上的非羟基氧的个数增多而增强。亚磷酸(
 )为弱酸,分子结构中含有一个非羟基氧,其酸性比HClO的酸性
)为弱酸,分子结构中含有一个非羟基氧,其酸性比HClO的酸性 与过量NaOH溶液反应的离子方程式为
与过量NaOH溶液反应的离子方程式为(7)萤石(
 )是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
)是自然界中常见的含氟矿物,其晶胞结构如图所示,X代表的离子是
您最近一年使用:0次
名校
解题方法
8 . 黄铜矿是主要的炼铜原料,其中铜元素的主要存在形式是 ,含有
,含有 和
和 。
。
(1)基态 的价层轨道表示式为
的价层轨道表示式为___________ 。
(2)在较低温度下 与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的中心原子杂化方式为___________ ,属于___________ (填“极性”或“非极性”)分子。
②X与水相比,二者中沸点较低的化合物的电子式为___________ 。
(3) 与氧气反应生成
与氧气反应生成 ,
, 中心原子的价层电子对数为
中心原子的价层电子对数为___________ ;从电子云重叠方式看, 分子中所含的共价键类型有
分子中所含的共价键类型有___________ 。
(4)用配位浸出法炼铜时,可用氨水将 中的铜元素浸出,溶液变蓝,同时生成
中的铜元素浸出,溶液变蓝,同时生成 和含有+6价硫元素的微粒,该过程中发生反应的离子方程式为
和含有+6价硫元素的微粒,该过程中发生反应的离子方程式为___________ 。
 ,含有
,含有 和
和 。
。(1)基态
 的价层轨道表示式为
的价层轨道表示式为(2)在较低温度下
 与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。①X分子的中心原子杂化方式为
②X与水相比,二者中沸点较低的化合物的电子式为
(3)
 与氧气反应生成
与氧气反应生成 ,
, 中心原子的价层电子对数为
中心原子的价层电子对数为 分子中所含的共价键类型有
分子中所含的共价键类型有(4)用配位浸出法炼铜时,可用氨水将
 中的铜元素浸出,溶液变蓝,同时生成
中的铜元素浸出,溶液变蓝,同时生成 和含有+6价硫元素的微粒,该过程中发生反应的离子方程式为
和含有+6价硫元素的微粒,该过程中发生反应的离子方程式为
您最近一年使用:0次
9 . 酒石酸(C4H6O6)是一种有机酸,其分子结构模型如图。下列说法不正确 的是
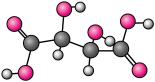

| A.酒石酸中各元素的电负性由大到小的顺序为O>C>H |
| B.酒石酸中碳原子有sp2、sp3两种杂化方式 |
| C.1 mol酒石酸最多能与2 mol 金属钠发生反应 |
| D.常温下,酒石酸钾水溶液pH>7,说明酒石酸是弱酸 |
您最近一年使用:0次
解题方法
10 . 研究发现, 低压合成甲醇的反应:
低压合成甲醇的反应: ,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。
,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。
(1) 分子和
分子和 分子中,
分子中, 原子的杂化轨道类型分别为
原子的杂化轨道类型分别为______________ 和______________ 。
(2) 和
和 中,沸点较高的是
中,沸点较高的是_____________ ,从结构角度分析,原因是______________________ 。
(3)基态锰原子的价层电子排布式为_______________ 。
(4)工业上利用甲醇空气氧化法生产甲醛(HCHO)。下列关于甲醛分子的说法正确的是____________ (填序号)。
a.碳氧双键中有一个 键,一个
键,一个 键
键
b.中心原子的孤电子对数为0
c.甲醛分子为极性分子
d.甲醛的VSEPR模型为平面三角形
 低压合成甲醇的反应:
低压合成甲醇的反应: ,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。
,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。(1)
 分子和
分子和 分子中,
分子中, 原子的杂化轨道类型分别为
原子的杂化轨道类型分别为(2)
 和
和 中,沸点较高的是
中,沸点较高的是(3)基态锰原子的价层电子排布式为
(4)工业上利用甲醇空气氧化法生产甲醛(HCHO)。下列关于甲醛分子的说法正确的是
a.碳氧双键中有一个
 键,一个
键,一个 键
键b.中心原子的孤电子对数为0
c.甲醛分子为极性分子
d.甲醛的VSEPR模型为平面三角形
您最近一年使用:0次



