名校
解题方法
1 . 乙烯是石油化学工业的重要原料,其产量可以用来衡量一个国家石油化学工业的发展水平。下列关于乙烯的说法不正确 的是
| A.含σ键、π键 | B.化学键均为非极性共价键 |
| C.碳原子均采取sp2杂化 | D.所有原子均位于同一平面 |
您最近一年使用:0次
2022-08-03更新
|
174次组卷
|
4卷引用:北京市朝阳区2020-2021学年高二下学期期末质量检测化学试题
名校
2 . 下列说法正确的是
| A.H2S、O3分子都是直线形 |
| B.BF3和NH3都是含有极性键的非极性分子 |
| C.CH3COOH分子中碳原子的杂化方式均为sp3 |
| D.CO2、HCN分子的结构式分别是:O=C=O、H-C≡N |
您最近一年使用:0次
9-10高二下·辽宁锦州·期末
名校
解题方法
3 . 如图所示,在乙烯分子中有5个σ键和一个π键,它们分别是
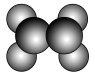
| A.sp2杂化轨道形成σ键,未杂化的2p轨道形成π键 |
| B.sp2杂化轨道形成π键,未杂化的2p轨道形成σ键 |
| C.C—H之间是sp2形成σ键,C—C之间是未参加杂化的2p轨道形成π键 |
| D.C—C之间是sp2形成σ键,C—H之间是未参加杂化的2p轨道形成π键 |
您最近一年使用:0次
2021-12-25更新
|
1585次组卷
|
65卷引用:北京交通大学附属中学2020-2021学年高二下学期期末考试化学试题
北京交通大学附属中学2020-2021学年高二下学期期末考试化学试题(已下线)09—10年锦州市高二下学期期末考试化学卷(已下线)09~10年银川一中高二下学期期末考试化学卷(已下线)2012-2013学年宁夏银川一中高二下学期期末考试化学试卷2014-2015江苏省南通中学高二上学期期末化学(理)试卷2014-2015学年吉林省吉林市第一中学高二下期末化学试卷内蒙古包头市第三十三中学2016-2017学年高二下学期期末考试化学试题甘肃省庆阳市镇原中学2019-2020学年高二下学期期末考试化学试题安徽省蚌埠第三中学2019-2020学年高二下学期期末考试化学试题(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构高二选择性必修3(人教版2019)第一章 有机化合物的结构特点与研究方法 第一节 有机化合物的结构特点 课时2 有机化合物中的共价键(鲁科版2019)选择性必修2 第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构(人教版2019)选择性必修2 第二章 分子结构与性质 第二节 分子的空间结构 课时2 杂化轨道理论鲁科版2019选择性必修2第2章 微粒间相互作用与物质性质 第2节 共价键与分子的空间结构 第1课时 分子空间结构的理论分析高二选择性必修2(人教版2019)第二章 分子结构与性质 第二节 分子的空间结构 课时2 杂化轨道理论(已下线)2.2.1 分子空间结构的理论分析-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题河南省开封市五县2020-2021学年高二下学期月考化学试题(已下线)2.2.2 杂化轨道理论简介-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)四川省宜宾市南溪区第二中学校2021-2022学年高二上学期12月月考化学试题(已下线)2010-2011学年山东省兖州市高二下学期期中考试化学试卷(已下线)2011-2012学年陕西省师大附中高二下学期期中考试化学试卷(已下线)2012--2013学年新疆乌鲁木齐市一中高二下学期期中考试化学试卷(平行班)(已下线)2014年高二鲁科版选修3化学规范训练2.2.1典型分子空间构型练习卷(已下线)2013届新疆乌鲁木齐市一中高二第二学期期中考试化学试卷(已下线)2015届西藏拉萨中学高三第一次月考化学试卷2015届西藏拉萨中学高三第一次月考化学试卷22014-2015学年辽宁实验分校高二下6月阶段测试化学试卷2015-2016学年西藏日喀则一中高二10月月考化学试卷2015-2016学年吉林省吉林五十五中高二下3月月考化学试卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年广东汕头金山中学高二下第十二周练化学卷2015-2016学年山西省右玉一中高二5月月考化学试卷2015-2016学年河南省三门峡市灵宝一中高二下第一次月考化学试卷2015-2016学年山西省朔州市右玉一中高二下5月月考化学试卷河北省蠡县中学2016-2017学年高二6月月考化学试题河南省焦作市博爱一中2016-2017学年高二下学期第一次月考化学试题河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:2.2 第2课时人教版2017-2018学年高二化学选修三同步训练:2.2 分子的立体构型(第2课时)河北省石家庄市鹿泉一中2017-2018学年高二3月月考化学试题山东省单县五中2017-2018学年高二下学期第一次月考化学试题【全国百强校】宁夏吴忠中学2017-2018学年高二6月月考化学试题新疆兵团八师一四三团一中2018-2019学年高二下学期期中考试化学试题(已下线)2019年11月26日《每日一题》2020年高考化学一轮复习—— 共价键的分类与判断2020届高三化学二轮物质结构题型专攻——分子结构与性质【选择基础专练】河南省林州市第一中学2019-2020学年高二3月线上调研考试化学试题山东省泰安市新泰市第二中学2019-2020学年高二下期中考试化学试题宁夏育才中学2019-2020学年高二下学期开学检测化学试题山西省太原市实验中学校2019-2020学年高二下学期期中考试化学试题河北省邯郸市大名县第一中学2019-2020学年高二下学期第四次半月考化学试题(清北班)天津市和平区2020届高三一模化学试题四川省自贡市田家炳中学2020-2021学年高二上学期开学考试化学试题内蒙古赤峰第二实验中学2021届高三模拟考试(一)化学试题新疆哈密市第八中学2019-2020学年高二下学期期中考试化学试题河南省汤阴县五一中学2019-2020学年高二下学期期中考试化学试题(已下线)2.2.2 杂化轨道理论(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)2.2.2 杂化轨道理论-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)课中-1.1.2 有机化合物中的共价键和有机化合物的同分异构现象-人教2019选择性必修3云南省楚雄彝族自治州民族中学2021-2022学年高二下学期3月月考化学试题陕西省宝鸡市长岭中学2021-2022学年高二下学期期中考试化学试题(已下线)第39练 共价键-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第40练 分子的空间结构-2023年高考化学一轮复习小题多维练(全国通用)安徽省滁州市定远县育才学校2021-2022学年高二分层班下学期期中考试化学试题山东省菏泽市单县二中2021-2022学年高二下学期开学考试 化学试题2.2.2 杂化轨道理论-随堂练习
解题方法
4 . 完成下列填空
(1)下列常见物质的空间结构呈直线形的是___________ ,呈平面三角形的是___________ 。中心原子轨道采取sp3杂化的是___________ ,采取sp2杂化的是___________ 。
①BF3 ②CO2 ③NH3 ④CCl4 ⑤HC≡CH
(2)NF3是微电子工业中种优良的等离子蚀刻气体,利用杂化轨道理论解释其空间结构是三角锥形:___________ 。
(3)某小组进行如下操作,观察到下列现象:
步骤1:向AgNO3溶液中逐滴滴加氨水,产生白色沉淀;
步骤2:继续滴加,沉淀消失,溶液变澄清。
①澄清溶液中含[Ag(NH3)2]+,其中含有的化学键类型有___________ 。
a.σ键 b.配位键 c.氢键
②已知:Ag++NH3•H2O AgOH↓+NH
AgOH↓+NH ,利用平衡移动原理解释步骤2的现象
,利用平衡移动原理解释步骤2的现象___________ 。
(1)下列常见物质的空间结构呈直线形的是
①BF3 ②CO2 ③NH3 ④CCl4 ⑤HC≡CH
(2)NF3是微电子工业中种优良的等离子蚀刻气体,利用杂化轨道理论解释其空间结构是三角锥形:
(3)某小组进行如下操作,观察到下列现象:
步骤1:向AgNO3溶液中逐滴滴加氨水,产生白色沉淀;
步骤2:继续滴加,沉淀消失,溶液变澄清。
①澄清溶液中含[Ag(NH3)2]+,其中含有的化学键类型有
a.σ键 b.配位键 c.氢键
②已知:Ag++NH3•H2O
 AgOH↓+NH
AgOH↓+NH ,利用平衡移动原理解释步骤2的现象
,利用平衡移动原理解释步骤2的现象
您最近一年使用:0次
5 . 下图是三种有机物的结构,请回答下列问题。

(1)维生素C的分子式是____ ,该分子中碳碳双键中的碳原子的杂化轨道类型是____ 。
(2)写出葡萄糖分子中含有的官能团的名称是_______ 。
(3)依据σ键、π键的成键特点,分析阿司匹林分子中至少有_______ 个原子共平面。
(4)下列说法正确的是_______ 。
a.维生素C和葡萄糖均有还原性
b.葡萄糖是人类能量的主要来源之一
c.阿司匹林属于芳香烃
(5)观察三种物质的分子结构,推测常温下三种物质在水中溶解度由大到小的顺序是_ (填序号)。
(6)写出阿司匹林与足量NaOH溶液混合加热,反应的化学方程式_______ 。

(1)维生素C的分子式是
(2)写出葡萄糖分子中含有的官能团的名称是
(3)依据σ键、π键的成键特点,分析阿司匹林分子中至少有
(4)下列说法正确的是
a.维生素C和葡萄糖均有还原性
b.葡萄糖是人类能量的主要来源之一
c.阿司匹林属于芳香烃
(5)观察三种物质的分子结构,推测常温下三种物质在水中溶解度由大到小的顺序是
(6)写出阿司匹林与足量NaOH溶液混合加热,反应的化学方程式
您最近一年使用:0次
名校
解题方法
6 . A、B、C、D 4种短周期元素,原子序数依次增大。其元素相关信息如下表。
(1)元素A、B、C中,电负性最大的是_______ (填元素符号)。
(2)A与B形成共价化合物 ,其分子的空间结构呈
,其分子的空间结构呈_______ 形。
(3) 易溶于
易溶于 中的原因是
中的原因是_______ 。
(4) 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ ; 的空间结构为
的空间结构为_______ 。
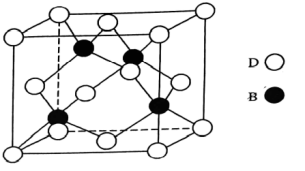
(5)B和D两种元素组成的化合物是共价晶体,其晶胞如下图所示,则表示该化合物的化学式为_______ (请用元素符号表示)。
| 元素 | 信息 |
| A | 元素原子的核外电子只有一种运动状态 |
| B | 价电子层中的未成对电子有3个 |
| C | 最外层电子数为其内层电子数的3倍 |
| D | 离子半径在同周期金属元素中最小 |
(1)元素A、B、C中,电负性最大的是
(2)A与B形成共价化合物
 ,其分子的空间结构呈
,其分子的空间结构呈(3)
 易溶于
易溶于 中的原因是
中的原因是(4)
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间结构为
的空间结构为(5)B和D两种元素组成的化合物是共价晶体,其晶胞如下图所示,则表示该化合物的化学式为

您最近一年使用:0次
2021-07-20更新
|
215次组卷
|
2卷引用:北京市密云区2020-2021学年高二下学期期末考试化学试题
7 . 碳元素的单质有多种形式,下图依次是 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:

回答下列问题:
(1)碳元素基态原子的最外层电子排布式为_______ 。
(2) 所属的晶体类型为
所属的晶体类型为_______ 晶体。
(3)在石墨晶体中,碳原子数与化学键数之比为_______ 。
(4)金刚石中碳原子的杂化轨道类型是_______ 。
(5)上述三种单质互称为_______ 。
a.同系物 b.同素异形体 c.同分异构体
 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:
回答下列问题:
(1)碳元素基态原子的最外层电子排布式为
(2)
 所属的晶体类型为
所属的晶体类型为(3)在石墨晶体中,碳原子数与化学键数之比为
(4)金刚石中碳原子的杂化轨道类型是
(5)上述三种单质互称为
a.同系物 b.同素异形体 c.同分异构体
您最近一年使用:0次
2021-07-20更新
|
350次组卷
|
3卷引用:北京市密云区2020-2021学年高二下学期期末考试化学试题
北京市密云区2020-2021学年高二下学期期末考试化学试题3.2.2 共价晶体-2021-2022学年高二化学课后培优练(人教版2019选择性必修2)(已下线)第三章 晶体结构与性质 章节过关检测-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)
名校
8 . 下列关于丙烯(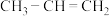 )分子的说法中,
)分子的说法中,不正确 的是
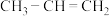 )分子的说法中,
)分子的说法中,| A.有1个π键 | B.有1个碳原子是sp3杂化 |
| C.存在非极性键 | D.3个碳原子在同一直线上 |
您最近一年使用:0次
2021-07-20更新
|
188次组卷
|
2卷引用:北京市密云区2020-2021学年高二下学期期末考试化学试题
9 . ECH(环氧氯丙烷,结构为 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。
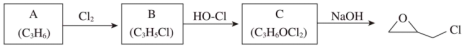
已知:
(1)A为丙烯,其分子中含有的官能团是_______ 。
(2)已知 为加成反应,
为加成反应, 的反应类型是
的反应类型是_______ 反应。
(3) 的反应中,B与次氯酸加成得到的C,有两种结构。
的反应中,B与次氯酸加成得到的C,有两种结构。
①C结构简式是ⅰ: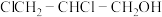 和ⅱ:
和ⅱ:_______ 。
②由分子中化学键的极性分析:ⅰ为 的主要产物。该分析过程是
的主要产物。该分析过程是_______ 。
(4)对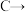 环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中
环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中 和物质C的比例增大,环氧氯丙烷的产率如图所示:
和物质C的比例增大,环氧氯丙烷的产率如图所示:
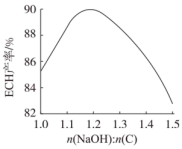
根据该反应中各物质的性质,分析随 的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):
的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):_______ 。
(5)原料中的丙烯可由石油裂解得到。在裂解分离得到的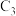 馏分中,除丙烯外,杂质气体中含有2种分子式均为
馏分中,除丙烯外,杂质气体中含有2种分子式均为 的链烃。
的链烃。
①杂质的其中一种分子内含有 杂化的碳原子,则该分子名称是
杂化的碳原子,则该分子名称是_______ 。
②杂质的另一种分子内,无 杂化的碳原子,则该分子内碳原子的杂化类型是
杂化的碳原子,则该分子内碳原子的杂化类型是_______ ;已知该分子中,4个氢原子不在同一个平面内,由分子中碳原子的杂化解释其原因:_______ 。
 )是生产环氧树脂的中间体,工业上可由如图路线合成。
)是生产环氧树脂的中间体,工业上可由如图路线合成。
已知:

(1)A为丙烯,其分子中含有的官能团是
(2)已知
 为加成反应,
为加成反应, 的反应类型是
的反应类型是(3)
 的反应中,B与次氯酸加成得到的C,有两种结构。
的反应中,B与次氯酸加成得到的C,有两种结构。①C结构简式是ⅰ:
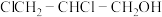 和ⅱ:
和ⅱ:②由分子中化学键的极性分析:ⅰ为
 的主要产物。该分析过程是
的主要产物。该分析过程是(4)对
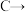 环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中
环氧氯丙烷的反应研究表明,当保持其他条件(反应温度、反应时间等)不变时,随起始反应物中 和物质C的比例增大,环氧氯丙烷的产率如图所示:
和物质C的比例增大,环氧氯丙烷的产率如图所示:
根据该反应中各物质的性质,分析随
 的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):
的值增大,环氧氯丙烷产率下降的原因(结合化学方程式表示):(5)原料中的丙烯可由石油裂解得到。在裂解分离得到的
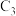 馏分中,除丙烯外,杂质气体中含有2种分子式均为
馏分中,除丙烯外,杂质气体中含有2种分子式均为 的链烃。
的链烃。①杂质的其中一种分子内含有
 杂化的碳原子,则该分子名称是
杂化的碳原子,则该分子名称是②杂质的另一种分子内,无
 杂化的碳原子,则该分子内碳原子的杂化类型是
杂化的碳原子,则该分子内碳原子的杂化类型是
您最近一年使用:0次
10 . 硼及其化合物在新材料、工农业生产等方面用途广泛。
(1)氮化硼存在不同的变体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,则六方氮化硼的晶体类型属于_______ 。
②高温高压下,六方氮化硼可转化为立方氮化硼,立方氮化硼的结构与金刚石类似,每个立方氮化硼晶胞中硼原子和氮原子的个数比为_______ 。
(2)氨硼烷( )是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)
)是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)

①氨硼烷分子为_______ (填“极性”或“非极性”)分子。
②氨硼烷分子中,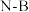 键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:
键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:_______ 。
③氨硼烷常温下为固态,它的熔点比乙烷的熔点高近300℃,是由于其分子间除了分子间作用力,还存在正电性H和负电性H的相互作用,这种作用称为“双氢键”。仿照氢键的表示方法:“ ”,上述双氢键可表示为
”,上述双氢键可表示为_______ (式中用“ ”及“
”及“ ”表示氢的带电情况)。
”表示氢的带电情况)。
④氨硼烷常温下稳定,加热到90℃左右分解产生 ,若该反应中只有氢元素的化合价发生变化,则每产生
,若该反应中只有氢元素的化合价发生变化,则每产生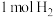 ,反应转移的电子的物质的量是
,反应转移的电子的物质的量是_______  。
。
⑤由氨硼:烷的组成或性质分析,氨硼烷作为储氢材料的优势有_______ 。
(1)氮化硼存在不同的变体,如六方氮化硼、立方氮化硼等,其结构如图。

①六方氮化硼的晶体结构类似石墨,则六方氮化硼的晶体类型属于
②高温高压下,六方氮化硼可转化为立方氮化硼,立方氮化硼的结构与金刚石类似,每个立方氮化硼晶胞中硼原子和氮原子的个数比为
(2)氨硼烷(
 )是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)
)是极具潜力的高性能储氢材料,其晶体结构之一如图。(已知电负性:H 2.1,B 2.0,N 3.0)
①氨硼烷分子为
②氨硼烷分子中,
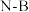 键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:
键为配位键,由原子的价层电子排布特点分析该配位键的形成过程:③氨硼烷常温下为固态,它的熔点比乙烷的熔点高近300℃,是由于其分子间除了分子间作用力,还存在正电性H和负电性H的相互作用,这种作用称为“双氢键”。仿照氢键的表示方法:“
 ”,上述双氢键可表示为
”,上述双氢键可表示为 ”及“
”及“ ”表示氢的带电情况)。
”表示氢的带电情况)。④氨硼烷常温下稳定,加热到90℃左右分解产生
 ,若该反应中只有氢元素的化合价发生变化,则每产生
,若该反应中只有氢元素的化合价发生变化,则每产生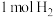 ,反应转移的电子的物质的量是
,反应转移的电子的物质的量是 。
。⑤由氨硼:烷的组成或性质分析,氨硼烷作为储氢材料的优势有
您最近一年使用:0次
2021-07-12更新
|
283次组卷
|
2卷引用:北京市东城区2020-2021学年高二下学期期末考试化学试题



