名校
解题方法
1 . 有两种有机化合物,用李比希法测得这两种有机物所含氢和碳的质量分数都分别为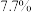 和
和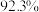 ,用质谱仪测得两种有机物具有相同的最大分子离子峰,将
,用质谱仪测得两种有机物具有相同的最大分子离子峰,将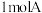 在氧气中充分燃烧产生
在氧气中充分燃烧产生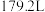 二氧化碳(标准状况),A含有苯环,所有碳原子均为
二氧化碳(标准状况),A含有苯环,所有碳原子均为 杂化;B分子中碳原子的化学环境完全相同且碳原子的杂化方式都为
杂化;B分子中碳原子的化学环境完全相同且碳原子的杂化方式都为 杂化。
杂化。
(1)A的分子式为_________________ 。
(2)B的键线式为__________________ 。
(3)化合物A与溴水反应可生成化合物C。
①该反应的方程式为___________________________ ;反应类型为__________________ 。
②与C互为同分异构体且核磁共振氢谱有两组峰,峰面积比为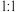 的有机物结构简式为
的有机物结构简式为__________________ 。
(4)A的一种同分异构体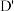 的结构中也含有苯环,A和
的结构中也含有苯环,A和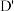 在下列仪器中显示的信号(或数据)完全相同,该仪器是
在下列仪器中显示的信号(或数据)完全相同,该仪器是_________ 。
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪 e.X-射线晶体衍射仪
(5)化合物B的六氯代物有_________ 种。
 和
和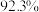 ,用质谱仪测得两种有机物具有相同的最大分子离子峰,将
,用质谱仪测得两种有机物具有相同的最大分子离子峰,将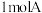 在氧气中充分燃烧产生
在氧气中充分燃烧产生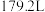 二氧化碳(标准状况),A含有苯环,所有碳原子均为
二氧化碳(标准状况),A含有苯环,所有碳原子均为 杂化;B分子中碳原子的化学环境完全相同且碳原子的杂化方式都为
杂化;B分子中碳原子的化学环境完全相同且碳原子的杂化方式都为 杂化。
杂化。(1)A的分子式为
(2)B的键线式为
(3)化合物A与溴水反应可生成化合物C。
①该反应的方程式为
②与C互为同分异构体且核磁共振氢谱有两组峰,峰面积比为
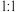 的有机物结构简式为
的有机物结构简式为(4)A的一种同分异构体
 的结构中也含有苯环,A和
的结构中也含有苯环,A和 在下列仪器中显示的信号(或数据)完全相同,该仪器是
在下列仪器中显示的信号(或数据)完全相同,该仪器是a.质谱仪 b.红外光谱仪 c.元素分析仪 d.核磁共振仪 e.X-射线晶体衍射仪
(5)化合物B的六氯代物有
您最近一年使用:0次
名校
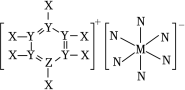
2 . 短周期主族元素X、Y、Z、M、N的原子序数依次增大,其中基态Y原子s能级电子数是P能级电于数的两倍,Z和M位于同一主族,其结构如图所示,下列说法不正确的是

| A.原子半径:Y>Z>X |
| B.非金属性:N>M>Y |
| C.YX4和MN3的中心原子杂化方式不同 |
| D.同周期中第一电离能小于Z的元素有五种 |
您最近一年使用:0次
名校
3 . 价层电子对互斥理论可以预测某些微粒的空间结构。下列说法不正确的是
| A.SO2和SO3的VSEPR模型均为平面三角形 |
| B.PCl3、NCl3的空间构型都是三角锥形 |
| C.BF3和NF3均为sp2杂化 |
D.CO2与 的键角相等 的键角相等 |
您最近一年使用:0次
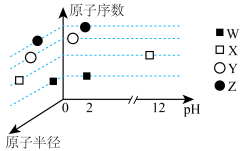
4 . 已知: 为短周期主族元素。常温下,它们的原子半径、原子序数、pH[元素最高价氧化物对应水化物的溶液(浓度均为
为短周期主族元素。常温下,它们的原子半径、原子序数、pH[元素最高价氧化物对应水化物的溶液(浓度均为 )的pH]的关系如图所示。下列说法正确的是
)的pH]的关系如图所示。下列说法正确的是
 为短周期主族元素。常温下,它们的原子半径、原子序数、pH[元素最高价氧化物对应水化物的溶液(浓度均为
为短周期主族元素。常温下,它们的原子半径、原子序数、pH[元素最高价氧化物对应水化物的溶液(浓度均为 )的pH]的关系如图所示。下列说法正确的是
)的pH]的关系如图所示。下列说法正确的是
A. 晶体的晶胞中 晶体的晶胞中 原子的配位数为6 原子的配位数为6 |
B.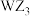 分子的中心原子为 分子的中心原子为 杂化 杂化 |
C.第一电离能: |
D.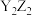 分子为含有极性共价键的平面结构分子 分子为含有极性共价键的平面结构分子 |
您最近一年使用:0次
名校
5 . 利用Sonogashira反应机理合成苯乙炔的基本过程如图,其中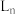 为2个三苯基膦配体(
为2个三苯基膦配体( ,Ph表示苯基),下列说法中正确的是
,Ph表示苯基),下列说法中正确的是

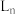 为2个三苯基膦配体(
为2个三苯基膦配体( ,Ph表示苯基),下列说法中正确的是
,Ph表示苯基),下列说法中正确的是
| A.催化循环过程中,Pd的配位数不变 | B.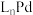 和CuI可提高碘苯的平衡转化率 和CuI可提高碘苯的平衡转化率 |
C. 中的磷和碳均为 中的磷和碳均为 杂化 杂化 | D.该反应过程中涉及3个中间产物 |
您最近一年使用:0次
名校
解题方法
6 . 亚铁氰化钾( )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。
(1)O元素位于___________ 区,基态O原子核外电子的空间运动状态有___________ 种。
(2)Fe在元素周期表中的位置___________ ,基态Fe原子的价电子轨道表示式为___________ 。
(3)黄血盐( )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是___________ , 该原子能量最高的电子所在能级符号为___________ 。
(4)亚铁氰化钾( )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为___________ 。
(5)普鲁士蓝( )中C的杂化方式为
)中C的杂化方式为___________ 。
 )是一种常见的食盐抗结剂,其三水合物(
)是一种常见的食盐抗结剂,其三水合物( )是黄色晶体,俗称黄血盐,遇
)是黄色晶体,俗称黄血盐,遇 立即产生深蓝色沉淀(
立即产生深蓝色沉淀( )。回答下列问题。
)。回答下列问题。(1)O元素位于
(2)Fe在元素周期表中的位置
(3)黄血盐(
 )中四种非金属元素的第一电离能最大的是
)中四种非金属元素的第一电离能最大的是(4)亚铁氰化钾(
 )中四种元素的电负性由大到小的顺序为
)中四种元素的电负性由大到小的顺序为(5)普鲁士蓝(
 )中C的杂化方式为
)中C的杂化方式为
您最近一年使用:0次
名校
解题方法
7 . 下列推测合理的是
A. 和 和 都是正四面体形分子且键角都为 都是正四面体形分子且键角都为 |
| B.NH3、CH4和H2O的中心原子杂化类型相同 |
| C.相同条件下,邻羟基苯甲酸的沸点高于对羟基苯甲酸 |
D.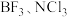 分子中各原子的最外层电子都满足8电子稳定结构 分子中各原子的最外层电子都满足8电子稳定结构 |
您最近一年使用:0次
2023-10-04更新
|
92次组卷
|
2卷引用:吉林省长春外国语学校2022-2023学年高二下学期开学考试化学试题
名校
解题方法
8 . 铁和硒(Se)都是人体所必需的微量元素,且在医药、催化、材料等领域有广泛应用,回答下列问题:
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①基态Se原子的核外电子排布式为[Ar]___________ ;
②该新药分子中有___________ 种不同化学环境的C原子;
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:

①富马酸分子中σ键与π键的数目比为___________ ;
②富马酸亚铁中各元素的电负性由大到小的顺序为___________ 。
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为NH ,反应过程如图所示:
,反应过程如图所示:

①产物中N原子的杂化轨道类型为___________ ;
② 的空间构型为
的空间构型为___________ 。
(1)乙烷硒啉(Ethaselen)是一种抗癌新药,其结构式如下:

①基态Se原子的核外电子排布式为[Ar]
②该新药分子中有
(2)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示:

①富马酸分子中σ键与π键的数目比为
②富马酸亚铁中各元素的电负性由大到小的顺序为
(3)科学家近期合成了一种固氮酶模型配合物,该物质可以在温和条件下直接活化H2,将N3-转化为NH
 ,反应过程如图所示:
,反应过程如图所示:
①产物中N原子的杂化轨道类型为
②
 的空间构型为
的空间构型为
您最近一年使用:0次
名校
9 . 布洛芬是一种用于小儿发热的经典解热镇痛药,异丁基苯是合成它的一种原料,二者的结构简式如图。下列说法正确的是


| A.异丁基苯属于芳香烃,与对二乙苯互为同分异构体 |
| B.异丁基苯和布洛芬中碳原子均有sp和sp3杂化 |
C.1mol布洛芬与足量的 溶液反应生成 溶液反应生成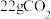 |
| D.两者均能与NaOH溶液反应 |
您最近一年使用:0次
10 . 由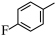 经两步反应合成
经两步反应合成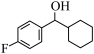 的步骤如下:
的步骤如下:
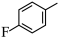
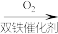
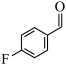
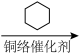
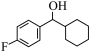
完成下列问题:
(1)上述有机物涉及的3种第二周期元素,其电负性由小到大排序依次是___________ 。
(2)用“*”标记出下图分子中的手性碳原子________ 。
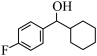
(3)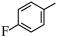 的分子式是
的分子式是___________ ,其中碳原子的杂化类型是___________ ,分子中有___________ 个原子参与形成离域键。
(4)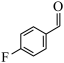 转化为
转化为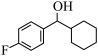 的过程中,C=O键中的
的过程中,C=O键中的___________ (填“σ”或“π”)键断裂,所属的有机反应基本类型是___________ 反应。
 经两步反应合成
经两步反应合成 的步骤如下:
的步骤如下:
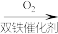



完成下列问题:
(1)上述有机物涉及的3种第二周期元素,其电负性由小到大排序依次是
(2)用“*”标记出下图分子中的手性碳原子

(3)
 的分子式是
的分子式是(4)
 转化为
转化为 的过程中,C=O键中的
的过程中,C=O键中的
您最近一年使用:0次
2023-09-10更新
|
256次组卷
|
2卷引用:吉林省长春外国语学校2023-2024学年高三上学期11月期中考试化学试题



