1 . 固体化合物 由4种元素组成,某学习小组开展如图探究实验:
由4种元素组成,某学习小组开展如图探究实验:
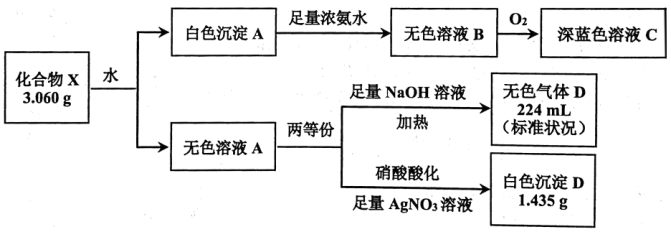
已知:白色沉淀 仅含两种元素。溶液
仅含两种元素。溶液 和溶液
和溶液 中阳离子由相同元素组成,且完全转化时,消耗标准状况下
中阳离子由相同元素组成,且完全转化时,消耗标准状况下 ,同时消耗
,同时消耗 。
。
请回答:
(1)无色气体 的电子式是
的电子式是_______ 。
(2)化合物 中的金属元素是
中的金属元素是_______ (填写元素符号),化学式是_______ 。
(3)写出无色溶液 转化为深蓝色溶液
转化为深蓝色溶液 的离子方程式
的离子方程式_______ 。
(4)白色沉淀 加水煮沸得到绿色溶液(溶质的元素组成与沉淀
加水煮沸得到绿色溶液(溶质的元素组成与沉淀 相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。
相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。
①写出上述反应的化学方程式_______ 。
②设计实验方案证明红色固体是混合物_______ 。
 由4种元素组成,某学习小组开展如图探究实验:
由4种元素组成,某学习小组开展如图探究实验:
已知:白色沉淀
 仅含两种元素。溶液
仅含两种元素。溶液 和溶液
和溶液 中阳离子由相同元素组成,且完全转化时,消耗标准状况下
中阳离子由相同元素组成,且完全转化时,消耗标准状况下 ,同时消耗
,同时消耗 。
。请回答:
(1)无色气体
 的电子式是
的电子式是(2)化合物
 中的金属元素是
中的金属元素是(3)写出无色溶液
 转化为深蓝色溶液
转化为深蓝色溶液 的离子方程式
的离子方程式(4)白色沉淀
 加水煮沸得到绿色溶液(溶质的元素组成与沉淀
加水煮沸得到绿色溶液(溶质的元素组成与沉淀 相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。
相同),并转化为红色固体,该红色固体由一种单质和一种氧化物组成。①写出上述反应的化学方程式
②设计实验方案证明红色固体是混合物
您最近一年使用:0次
2021-09-02更新
|
897次组卷
|
2卷引用:浙江省“七彩阳光”2022届新高考研究联盟返校考试化学试题
2 . 氮、磷、砷、铁、钛等元素及其化合物在现代农业、科技和国防建设中有着许多独特的用途。
I.如LiFePO4是新型锂离子电池的电极材料,可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。
(1)Fe2+核外电子排布式为___________ ,NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是___________ (填元素符号)。
(2)苯胺(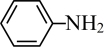 )和NH4H2PO4中的N原子杂化方式分别为
)和NH4H2PO4中的N原子杂化方式分别为___________ 。
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是___________ 。
II.(4)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiC136H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________ 。
(5)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。
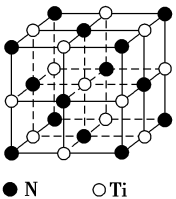
①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则与该Ti原子最邻近的Ti的数目为___________ 。Ti 原子与跟它次邻近的N原子之间的距离为___________ 。
②已知在氮化钛晶体中Ti原子的半径为apm,N原子的半径为bpm,它们在晶体中是紧密接触的,则在氮化钛晶体中原子的空间利用率为___________ 。(用a、b表示)
III.(6)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的晶胞如图所示,该磷钇矿的化学式为___________ 。
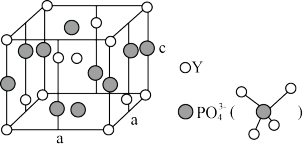
(7)已知晶胞参数为anm和cnm,阿伏加德罗常数的值为NA,则该磷钇矿的ρ为___________ 。g·cm-3 (列出计算式,用a、c表示)
I.如LiFePO4是新型锂离子电池的电极材料,可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。
(1)Fe2+核外电子排布式为
(2)苯胺(
 )和NH4H2PO4中的N原子杂化方式分别为
)和NH4H2PO4中的N原子杂化方式分别为(3)苯胺和甲苯相对分子质量接近,但苯胺熔点比甲苯的高,原因是
II.(4)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiC136H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为
(5)氮化钛熔点高,硬度大,具有典型的NaCl型晶体结构,其晶胞结构如图所示。

①设氮化钛晶体中Ti原子与跟它最邻近的N原子之间的距离为r,则与该Ti原子最邻近的Ti的数目为
②已知在氮化钛晶体中Ti原子的半径为apm,N原子的半径为bpm,它们在晶体中是紧密接触的,则在氮化钛晶体中原子的空间利用率为
III.(6)从磷钇矿中可提取稀土元素钇(Y),某磷钇矿的晶胞如图所示,该磷钇矿的化学式为

(7)已知晶胞参数为anm和cnm,阿伏加德罗常数的值为NA,则该磷钇矿的ρ为
您最近一年使用:0次
名校
3 . 胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:

下列有关胆矾的说法正确的是

下列有关胆矾的说法正确的是
| A.Cu2+的价电子排布式为3d84s1 |
| B.所有氧原子都采取sp3杂化 |
| C.氧原子参与形成离子键、配位键和氢键三种化学键 |
| D.胆矾中的水在不同温度下会分步失去 |
您最近一年使用:0次
2019-04-29更新
|
1100次组卷
|
4卷引用:鲁科版2019选择性必修2第2章综合检测卷



