1 . C、N化合物对人类生存环境有重要影响。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为_________ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序为_________ 。
(3)键角:NH3__________ (填“>“<”或“=”)H2O;NH3的VSEPR模型为_________ 。
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为_________ 。
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为_________ (填元素符号),原因是_________ 。
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。_________ 。
②2号原子的坐标为_________ 。
③该晶体的密度为__________ g/cm3。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为
(2)C、N、O三种元素的第一电离能由小到大的顺序为
(3)键角:NH3
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。
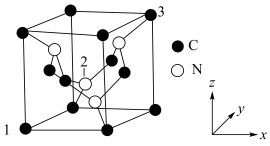
②2号原子的坐标为
③该晶体的密度为
您最近一年使用:0次
2024-03-27更新
|
315次组卷
|
4卷引用:2024届青海省海东市高三下学期二模理科综合试卷-高中化学
2024届青海省海东市高三下学期二模理科综合试卷-高中化学青海省西宁市湟中区2024届高三下学期一模理综化学试题2024届陕西省榆林市高三下学期第二次模拟检测理科综合试题-高中化学(已下线)化学(北京卷01)-2024年高考押题预测卷
名校
解题方法
2 . 五羰基铁[Fe(CO)5]催化化工生产中某反应的机理如下图所示,下列说法错误 的是
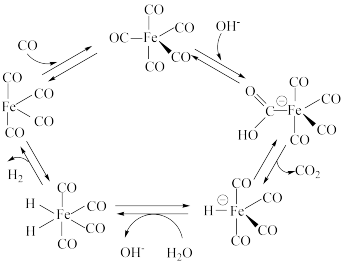

| A.Fe(CO)4是该反应的中间体 |
| B.OH-参与了该催化循环 |
| C.反应过程中Fe的成键数目保持不变 |
| D.该催化反应为CO+H2O⇌CO2+H2 |
您最近一年使用:0次
2022-08-03更新
|
409次组卷
|
3卷引用:青海省海东市第一中学2022届高三第一次模拟考试理科综合化学试题
青海省海东市第一中学2022届高三第一次模拟考试理科综合化学试题(已下线)易错点20 化学反应机理-备战2023年高考化学考试易错题广东省广州市华南师范大学附属中学2022-2023学年高三上学期11月月考化学试题
解题方法
3 . 铁、铬、锰、镍及化合物在生产生活中应用广泛。
(1)铁元素在元素周期表中位置为____ 。KSCN和K4[Fe(CN)6]常用于检验Fe3+,SCN-的立体构型为____ 。
(2)Ni原子基态原子价层电子排布式为____ ,区分晶体Ni和非晶体Ni最可靠的科学方法为_____ 。
(3)六羰基铬[Cr(CO)6]用于制造高纯度铬粉,它的沸点为220℃,Cr(CO)6的晶体类型为____ ,Cr(CO)6中键和π键的个数之比____ 。
(4)P、S的第二电离能(I2)的大小关系为I2(P)____ I2(S),原因是_____ 。β—MnSe的结构中Se为面心立方最密堆积,晶胞结构如图所示。
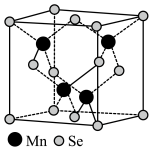
①β—MnSe中Mn的配位数为____ 。
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为NA。则距离最近的两个锰原子之间的距离为____ pm。
(1)铁元素在元素周期表中位置为
(2)Ni原子基态原子价层电子排布式为
(3)六羰基铬[Cr(CO)6]用于制造高纯度铬粉,它的沸点为220℃,Cr(CO)6的晶体类型为
(4)P、S的第二电离能(I2)的大小关系为I2(P)

①β—MnSe中Mn的配位数为
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为NA。则距离最近的两个锰原子之间的距离为
您最近一年使用:0次
名校
解题方法
4 . 硒化物(如KCu4Se8)可用于太阳能电池、光传感器、热电发电与制冷等。回答下列问题:
(1)基态Se原子核外电子排布式为[Ar]___________ 。
(2)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为___________ 。
(3)O、S、Se均位于元素周期表第VIA族,它们的氢化物H2O、H2S、H2Se分子的键角从大到小顺序为___________ 。
(4)配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为___________ ,配合离子中与Cu(Ⅱ)形成配位键的原子是___________ ,配体中碳原子的杂化方式是___________ 。
(5)TMTSF(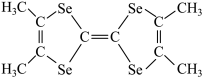 )中共价键的类型是
)中共价键的类型是___________ ,每个分子中含___________ 个σ键。
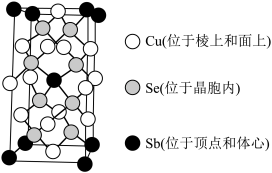
(6)Cu、Sb、Se组成的热电材料,其晶胞结构如图所示,a=b=566pm,c=1128pm,该晶体的密度为___________ (列出计算表达式)g·cm-3。
(1)基态Se原子核外电子排布式为[Ar]
(2)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为
(3)O、S、Se均位于元素周期表第VIA族,它们的氢化物H2O、H2S、H2Se分子的键角从大到小顺序为
(4)配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为
(5)TMTSF(
 )中共价键的类型是
)中共价键的类型是(6)Cu、Sb、Se组成的热电材料,其晶胞结构如图所示,a=b=566pm,c=1128pm,该晶体的密度为

您最近一年使用:0次
2021-02-26更新
|
406次组卷
|
4卷引用:青海省海东市2021届高三第二次模拟考试理科综合化学试题
青海省海东市2021届高三第二次模拟考试理科综合化学试题广东省佛山市顺德区均安中学2021届高三下学期第三次教学质量检测化学试题(已下线)大题08 物质结构与性质(一)(选修)-【考前抓大题】备战2021年高考化学(全国通用)(已下线)第4周 周测卷-备战2022年高考化学周测与晚练(新高考专用)
5 . 物质结构决定物质性质,回答下列涉及物质结构和性质的问题。
(1)第二周期中,元素的第一电离能处于B与N之间的元素有______ 种。
(2)某元素位于第四周期VII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为___________ 。
(3)AlC13是有机合成和石油化工的催化剂,已知AlCl3可以通过配位键形成具有桥式结构的双聚分子Al2Cl6,Al2Cl6分子的结构式为_________ 。
(4)KCN可被H2O2氧化为KOCN。KOCN可作为制药材料,其晶体类型是________ ,碳原子采取sp杂化,1mol该物质中含有的π键数目为______ ;H2O2常温下是液体,沸点较高(150℃),其主要原因是____________ 。
(5)氮化硼(BN)和磷化硼(BP)都是受到高度关注的耐磨涂料,它们结构相似,但是氮化硼晶体的熔点要比磷化硼晶体高,其原因是________ 。
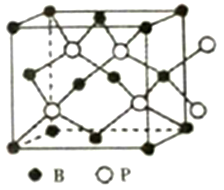
(6)磷化硼晶体的晶胞结构如图所示,在BP晶胞中B原子的堆积方式为______ ,若图中立方体的边长为a pm,则磷化硼中硼原子和磷原子之间的最近距离为__________ 。
(1)第二周期中,元素的第一电离能处于B与N之间的元素有
(2)某元素位于第四周期VII族,其基态原子的未成对电子数与基态碳原子的未成对电子数相同,则其基态原子的价层电子排布式为
(3)AlC13是有机合成和石油化工的催化剂,已知AlCl3可以通过配位键形成具有桥式结构的双聚分子Al2Cl6,Al2Cl6分子的结构式为
(4)KCN可被H2O2氧化为KOCN。KOCN可作为制药材料,其晶体类型是
(5)氮化硼(BN)和磷化硼(BP)都是受到高度关注的耐磨涂料,它们结构相似,但是氮化硼晶体的熔点要比磷化硼晶体高,其原因是
(6)磷化硼晶体的晶胞结构如图所示,在BP晶胞中B原子的堆积方式为
您最近一年使用:0次



