名校
1 . 已知:①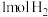 分子中化学键断裂时需要吸收436kJ的能量,②
分子中化学键断裂时需要吸收436kJ的能量,② 蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成
蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成 分子时释放299kJ的能量。下列判断不正确的是
分子时释放299kJ的能量。下列判断不正确的是
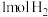 分子中化学键断裂时需要吸收436kJ的能量,②
分子中化学键断裂时需要吸收436kJ的能量,② 蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成
蒸气中化学键断裂时需要吸收151kJ的能量,③由H原子和I原子形成 分子时释放299kJ的能量。下列判断不正确的是
分子时释放299kJ的能量。下列判断不正确的是A. 蒸气比 蒸气比 分子稳定 分子稳定 |
B. 发生分解生成 发生分解生成 蒸气和 蒸气和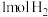 吸收11kJ热量 吸收11kJ热量 |
| C.HI溶液与NaOH溶液反应属于放热反应 |
| D.上述HI的生成过程中有非极性键的断裂和极性键的生成 |
您最近一年使用:0次
名校
解题方法
2 . 氮可形成多种化合物,其中三氯化氮NCl3)常温下是一种淡黄色液体,其分子星三角锥形,关于NCl3的叙述不正确的是
| A.NCl3晶体为共价晶体 | B.分子中N-Cl键是极性共价键 |
| C.NCl3晶体融化时破坏共价键 | D.NCl3中的原子都满足8电子的稳定结构 |
您最近一年使用:0次
名校
解题方法
3 . 高铁酸钠(Na2FeO4)具有很强的氧化性,是一种新型的绿色净水消毒剂,只在碱性环境中稳定存在。工业上可以通过次氯酸钠氧化法制备高铁酸钠,生产过程如下:
(1)氢氧化钠固体中存在的化学键类型有___________ 。
(2)经过步骤①后,加入NaOH固体的原因是___________ 。
(3)H2O2的电子式为___________ ,是___________ 分子(填“极性”或“非极性”),步骤②反应的离子方程式是___________ 。
(4)从溶液Ⅰ中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为___________ 。
(5)已知用Na2FeO4消毒时,其产物为Fe(OH)3;通过计算可知Na2FeO4的消毒效率(以单位质量得到的电子数表示)比氯气的___________ (填“高”或“低”),用高铁酸钠代替氯气作净水消毒剂的优点是___________ (答出一点即可)。

(1)氢氧化钠固体中存在的化学键类型有
(2)经过步骤①后,加入NaOH固体的原因是
(3)H2O2的电子式为
(4)从溶液Ⅰ中分离出Na2FeO4后,还有副产品Na2SO4、NaCl,则步骤③中反应的离子方程式为
(5)已知用Na2FeO4消毒时,其产物为Fe(OH)3;通过计算可知Na2FeO4的消毒效率(以单位质量得到的电子数表示)比氯气的
您最近一年使用:0次
名校
4 . 下列物质的结构与性质或性质与用途具有对应关系的是
A. 分子间存在氢键, 分子间存在氢键, 易溶于水 易溶于水 |
B. 熔点低,可用作超导体 熔点低,可用作超导体 |
| C.液氨汽化时吸收大量的热,可用作制冷剂 |
D. 是极性分子,可用于漂白纸浆 是极性分子,可用于漂白纸浆 |
您最近一年使用:0次
名校
5 . 如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:__________ 种不同空间运动状态。⑨号元素在周期表中的位置是__________ ,基态时其最高能层的电子占据的原子轨道电子云轮廓为__________ 形。第二周期所有元素中第一电离能介于①②之间的有__________ 种。基态⑩原子的简化电子排布式__________ ,该元素位于__________ 区。
(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式__________ ,该分子为__________ (填“极性”或“非极性”)分子。
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。

(2)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(3)下列有关性质的比较正确且能用元素周期律解释的是__________(填标号)。
| A.非金属性:②>③ |
| B.气态最简单氢化物的稳定性:③>⑦ |
| C.最高价氧化物对应的水化物的碱性:④>⑤ |
| D.最简单氢化物的沸点:③>⑦ |
您最近一年使用:0次
名校
解题方法
6 . 以下实验目的、方法和相关解释都正确的是
| 选项 | 实验目的 | 实验方法 | 相关解释 |
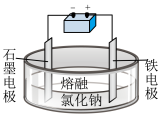
| A | 电解熔融氯化钠 |
| 该装置阳极反应为2Cl--2e-=Cl2 |
| B | 金属防腐 |
| 该图采用的是外加电流法对铁管道进行保护 |
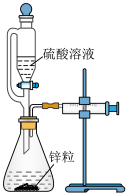
| C | 测量锌粒和不同浓度的硫酸溶液反应速率的快慢 |
| 该实验用到的实验仪器有恒压滴液漏斗、锥形瓶、双孔塞、注射器 |
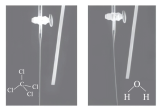
| D | 验证分子极性 |
| 该实验是用毛皮摩擦过的橡胶棒靠近 和 和 ,由图中现象可知 ,由图中现象可知 为非极性分子, 为非极性分子, 为极性分子 为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-05更新
|
271次组卷
|
4卷引用:河北省保定市保定部分2023-2024学年高一下学期4月(1+3)期中考试化学试题
名校
7 . 无机物可根据其组成和性质进行分类。现有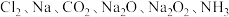 六种物质,完成下列填空:
六种物质,完成下列填空:
(1)由分子构成的单质是
(2)既有离子键又有共价键的物质的电子式为
(3)上述化合物中组成元素的原子半径由大到小的顺序是
(4)
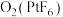 是离子化合物,其中
是离子化合物,其中 为
为 价。正确判断是___________。
价。正确判断是___________。| A.常温下为固体 | B.不存在共价键 | C.属于极性分子 | D.由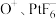 构成 构成 |
您最近一年使用:0次
8 . 化合物可分为离子化合物和共价化合物,其分类的依据就是看化合物中是否存在着阴、阳离子。共价化合物又可分为极性化合物和非极性化合物,若分子结构对称,则为非极性分子;反之,则为极性分子。在氮氧化物中, 是一种比较有趣的化合物。它在低温下呈固态,在温度稍高(如在夏天)就变成气态,同时发生部分分解,生成氮的低价氧化物和氧气。
是一种比较有趣的化合物。它在低温下呈固态,在温度稍高(如在夏天)就变成气态,同时发生部分分解,生成氮的低价氧化物和氧气。
(1)
 是
是 和
和 的化学方程式为
的化学方程式为(2)已知
 分子的经典结构为
分子的经典结构为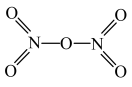 ,则气态时
,则气态时 是
是(3)
 在固态时,能发生如下电离:
在固态时,能发生如下电离: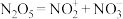 。因此,固态时的
。因此,固态时的 属于
属于(4)
 能和许多物质发生化学反应。与金属Na发生反应的化学方程式为
能和许多物质发生化学反应。与金属Na发生反应的化学方程式为
您最近一年使用:0次
名校
9 . 关于 的下列叙述中不正确的是
的下列叙述中不正确的是
 的下列叙述中不正确的是
的下列叙述中不正确的是A. 是极性分子 是极性分子 | B.同时含有离子键和非极性共价键 |
| C.同时含有极性键和非极性键 | D.1mol 完全分解,转移1mol电子 完全分解,转移1mol电子 |
您最近一年使用:0次
10 . 设NA为阿伏伽德罗常数的值,下列说法正确的是
| A.25℃时,100mLpH=13的NaOH溶液中滴加醋酸溶液至中性,溶液中醋酸根离子和钠离子的总数为0.02NA |
| B.电解精炼铜,当精炼初始的10分钟内阳极共减重16g,则该10分钟内电路中通过的电子数为0.5NA |
| C.标准状况下,22.4LO3中含有的非极性共价键的数量为2NA |
| D.0.1mol·L-1的Na2SO3溶液中,含S微粒的总数为0.1NA |
您最近一年使用:0次