名校
解题方法
1 . 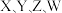 为原子序数依次增大的主族元素。基态
为原子序数依次增大的主族元素。基态 原子中含有两种形状的电子云,且有一个单电子;基态
原子中含有两种形状的电子云,且有一个单电子;基态 原子的最高能级轨道中均有电子,且自旋方向相同;基态
原子的最高能级轨道中均有电子,且自旋方向相同;基态 原子的价层电子排布式为
原子的价层电子排布式为 是地壳中含量最多的金属元素。下列说法错误的是
是地壳中含量最多的金属元素。下列说法错误的是
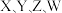 为原子序数依次增大的主族元素。基态
为原子序数依次增大的主族元素。基态 原子中含有两种形状的电子云,且有一个单电子;基态
原子中含有两种形状的电子云,且有一个单电子;基态 原子的最高能级轨道中均有电子,且自旋方向相同;基态
原子的最高能级轨道中均有电子,且自旋方向相同;基态 原子的价层电子排布式为
原子的价层电子排布式为 是地壳中含量最多的金属元素。下列说法错误的是
是地壳中含量最多的金属元素。下列说法错误的是A.电负性 | B.简单氢化物的沸点: |
C. 的第一电离能高于同周期相邻元素 的第一电离能高于同周期相邻元素 | D. 的合金餐具不宜长时间存放酸性或碱性食物 的合金餐具不宜长时间存放酸性或碱性食物 |
您最近一年使用:0次
2 . 二氧化碳利用技术已成为当今世界研究热点。回答下列问题:
(1)空气中CO2含量过高造成的环境问题是___________ 。
(2)氢气还原二氧化碳是处理二氧化碳的方法之一,常见反应原理有
H2(g)+CO2(g) H2O(g)+CO(g) △H2=+41.2kJ∙mol-1
H2O(g)+CO(g) △H2=+41.2kJ∙mol-1
3H2(g)+3CO(g) CH3OCH3(g)+CO2(g) △H2=-245.5kJ∙mol-1
CH3OCH3(g)+CO2(g) △H2=-245.5kJ∙mol-1
①6H2(g)+2CO2(g) CH3OCH3(g)+3H2O(g) △H3=
CH3OCH3(g)+3H2O(g) △H3=___________ kJ∙mol-1
②在上述反应涉及的分子中,属于非极性分子的是___________ 。甲醇的沸点(64.7℃)高于二甲醚的沸点(-29.5℃),原因是___________ 。
(3)在恒压密闭容器中通入CO2和H2的混合气体,制备甲醇:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-94.3kJ∙mol-1,反应过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
CH3OH(g)+H2O(g) △H=-94.3kJ∙mol-1,反应过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:___________ ℃。
②随着温度升高,反应速率加快,甲醇的时空收率增大。继续升高温度,甲醇的时空收率反而降低的原因可能是___________ 。
(4)一种Li/CO2电池模拟装置如图所示。___________ (填“阴”或“阳”)离子交换膜。
②充电时阳极的电极反应式为___________ 。
(1)空气中CO2含量过高造成的环境问题是
(2)氢气还原二氧化碳是处理二氧化碳的方法之一,常见反应原理有
H2(g)+CO2(g)
 H2O(g)+CO(g) △H2=+41.2kJ∙mol-1
H2O(g)+CO(g) △H2=+41.2kJ∙mol-13H2(g)+3CO(g)
 CH3OCH3(g)+CO2(g) △H2=-245.5kJ∙mol-1
CH3OCH3(g)+CO2(g) △H2=-245.5kJ∙mol-1①6H2(g)+2CO2(g)
 CH3OCH3(g)+3H2O(g) △H3=
CH3OCH3(g)+3H2O(g) △H3=②在上述反应涉及的分子中,属于非极性分子的是
(3)在恒压密闭容器中通入CO2和H2的混合气体,制备甲醇:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H=-94.3kJ∙mol-1,反应过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表:
CH3OH(g)+H2O(g) △H=-94.3kJ∙mol-1,反应过程中测得甲醇的时空收率(STY)(表示单位物质的量催化剂表面甲醇的平均生成速率)随温度(T)变化如下表: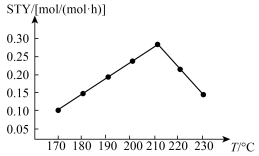
②随着温度升高,反应速率加快,甲醇的时空收率增大。继续升高温度,甲醇的时空收率反而降低的原因可能是
(4)一种Li/CO2电池模拟装置如图所示。
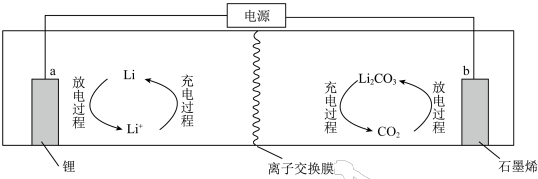
②充电时阳极的电极反应式为
您最近一年使用:0次
21-22高二上·四川达州·阶段练习
名校
解题方法
3 . R、T、W、X、Y、Z都是短周期元素,且W、X、Y、Z的核电荷数依次增大。下表列出它们的性质和结构:
(1)Z原子的外围电子轨道表达式为___________ ,T、X、Z的第一电离能由大到小的顺序为___________ (用化学符号填空)。
(2)常温下,RW3是一种刺激性气味、易液化的气体。RW3极易溶于水的主要原因是___________ (至少答两点)。
(3)在浓的QCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为QCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配离子的化学式为___________ ,1mol的QCl3·6H2O的绿色晶体溶于水再加入足量AgNO3溶液,得到的沉淀的物质的量为___________ 。
(4)分析R、T、X、Z简单氢化物的沸点高低并解释原因___________
| 元素编号 | 元素性质或原子结构 |
| R | 原子价电子排布式为nsnnpn+1 |
| T | 基态原子核外3个能级上有电子,且各能级上的电子数相等 |
| W | 宇宙中含量最多的元素 |
| X | 核外s能级上的电子总数与P能级上的电子总数相等 |
| Z | 原子核外P能级上的电子总数比s能级上的电子总数多2 |
| Q | 有“生物金属”之称,Q4+和氩原子的核外电子排布相同 |
(1)Z原子的外围电子轨道表达式为
(2)常温下,RW3是一种刺激性气味、易液化的气体。RW3极易溶于水的主要原因是
(3)在浓的QCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6,组成为QCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配离子的化学式为
(4)分析R、T、X、Z简单氢化物的沸点高低并解释原因
您最近一年使用:0次
2021-10-08更新
|
180次组卷
|
3卷引用:2020年天津卷化学高考真题变式题1-12



