名校
1 . 下列关于共价晶体、分子晶体的叙述中,不正确的是
A.在 晶体中,1个硅原子和4个氧原子形成4个共价键 晶体中,1个硅原子和4个氧原子形成4个共价键 |
| B.混合晶体石墨的熔点高于金刚石 |
C. 的相对分子质量大于 的相对分子质量大于 ,所以 ,所以 的沸点高于 的沸点高于 |
| D.金刚石为网状结构,由共价键形成的碳原子环中,最小环上最多4个碳原子共面 |
您最近一年使用:0次
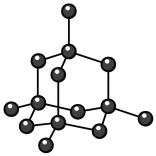
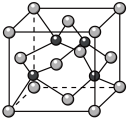
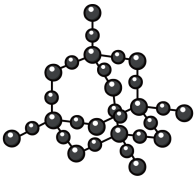
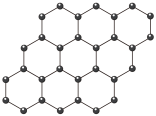
2 . 观察下列模型,判断下列说法错误的是
金刚石 | 碳化硅 | 二氧化硅 | 石墨烯 |
|
|
|
|
|
|
A. 晶体堆积属于分子密堆积 晶体堆积属于分子密堆积 |
B. 晶体中Si和Si-O键个数比为1:4 晶体中Si和Si-O键个数比为1:4 |
| C.石墨烯中碳原子和六元环个数比为2:1 |
| D.原子数相同的金刚石和碳化硅,共价键个数之比为1:2 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
3 . 冰晶胞中水分子的空间排列方式与金刚石晶胞类似。每个冰晶胞平均占有8个水分子,冰晶胞与金刚石晶胞排列方式相同的原因是___________ 。
您最近一年使用:0次
2023高三·全国·专题练习
4 . 原子晶体不能形成最密堆积结构的原因是______________________ 。
您最近一年使用:0次
5 . SiO2为何是原子晶体,原因是___________ 。
您最近一年使用:0次
名校
解题方法
6 . 下列有关阿伏加德罗常数说法不正确的是
| A.1molNH3中所含孤电子对数目为NA |
| B.1mol冰晶体中最多可含氢键2NA |
| C.46gC2H6O分子中含极性键数目一定是7NA |
| D.1mol金刚石晶体中有C-C键2NA |
您最近一年使用:0次
7 . 下列有关晶体的说法正确的是
| A.石英是共价晶体,每个硅原子与4个氧原子形成正四面体结构 |
| B.在晶体中只要有阳离子就一定有阴离子 |
| C.石墨晶体中存在大π键,因而石墨层间可以滑动,质地较软 |
| D.晶体溶于水后,可电离出自由移动的离子,该晶体一定是离子晶体 |
您最近一年使用:0次
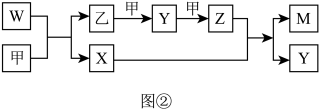
8 . A、B、D、E四种元素均为短周期元素,原子序数逐渐增大。A元素原子的核外电子数、电子层数和最外层电子数均相等。B、D、E三种元素在周期表中的相对位置如表①所示,只有E元素的单质能与水反应生成两种酸,甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素:W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质;X分子含有10个电子。它们之间的转化关系如图②所示。
表①
请回答下列问题:
(1)Z的化学式为___________ ;X分子的空间构型为___________ 。
(2)E的单质与水反应的离子方程式为___________ 。 D、E元素可分别与硅(Si)、钛(Ti)元素形成化合物,其中SiD2的熔点为1723℃,沸点2230℃,TiE4的熔点为-24.1℃,沸点为136.4℃,两者熔沸点差别很大的原因是___________ 。
(3)W-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。W-空气燃料电池放电时负极反应式为___________ 。
(4)将一定量的A2、B2的混合气体放入1L恒容密闭容器中,在200℃下达到平衡。测得平衡气体的总物质的量为0.4mol,其中A2为0.1mol,B2为0.1mol。则该条件下A2的平衡转化率为___________ ,该温度下的平衡常数为___________ 。
表①
| B | D | |
| E |

请回答下列问题:
(1)Z的化学式为
(2)E的单质与水反应的离子方程式为
(3)W-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。W-空气燃料电池放电时负极反应式为
(4)将一定量的A2、B2的混合气体放入1L恒容密闭容器中,在200℃下达到平衡。测得平衡气体的总物质的量为0.4mol,其中A2为0.1mol,B2为0.1mol。则该条件下A2的平衡转化率为
您最近一年使用:0次
解题方法
9 . 短周期元素X、Y、Z、W中,X元素的原子最外层电子排布为ns1,Y元素的原子价电子排布为ns2np2,Z元素的最外层电子数是其电子层数的3倍,W元素原子的M电子层的p能级中有3个未成对电子。
(1)Z原子的电子排布式为___________ ,若X为非金属元素,则按原子轨道的重叠方式,X与Z形成的化合物中的共价键属于___________ 键(填“σ”或“π”)。
(2)当n=2时,Y在元素周期表的位置为___________ ,YZ2属于___________ 分子(填“极性”或“非极性”)。
(3)当n=3时,YZ2晶体属于___________ 晶体;YZ2晶体中Y原子与Y-Z键的数目之比为___________ 。
(4)若X元素的原子最外层电子排布为2s1,Y元素的原子价电子排布为3s23p2,X、Y、Z、W四种元素的第一电离能由大到小的顺序是___________ (用元素符号表示)。
(1)Z原子的电子排布式为
(2)当n=2时,Y在元素周期表的位置为
(3)当n=3时,YZ2晶体属于
(4)若X元素的原子最外层电子排布为2s1,Y元素的原子价电子排布为3s23p2,X、Y、Z、W四种元素的第一电离能由大到小的顺序是
您最近一年使用:0次
解题方法
10 . 物质结构决定物质的性质。下列物质结构与性质不具有对应关系的是
| 选项 | 物质结构 | 性质 |
| A | 碳原子以共价键结合成立体网状结构 | 金刚石质地坚硬 |
| B | 石墨层与层之间以分子间作用力结合 | 石墨层与层之间可以滑动 |
| C | N2中氮氮三键键能大 | N2在常温下难以发生化学反应 |
| D | 乙醇分子中含有羟基 | 乙醇易燃烧 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次