1 . 干冰和冰是两种常见的分子晶体,关于两种晶体的比较中正确的是
| A.晶体的密度:干冰>冰 |
| B.晶体的熔点:干冰>冰 |
| C.晶体中的空间利用率:干冰>冰 |
| D.晶体中分子间相互作用力类型相同 |
您最近一年使用:0次
2 . 美国加州Livermore国家实验室物理学家Choong—Shik和他的同事们,在40Gpa的高压容器中,用Nd:YbLiF4激光器将液态二氧化碳加热到1800K,二氧化碳转化为与石英具有相似结构的晶体。估计该晶体可能具有的结构或性质是
| A.该晶体属于共价晶体 | B.硬度与金刚石相近 |
| C.熔点较低 | D.硬度较小 |
您最近一年使用:0次
2021-04-12更新
|
159次组卷
|
4卷引用:海南省海南鑫源高级中学2020-2021学年高二下学期第一次月考化学试题
海南省海南鑫源高级中学2020-2021学年高二下学期第一次月考化学试题(已下线)3.2 分子晶体与共价晶体(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)3.2.2共价晶体与分子晶体(课中)-鲁科版选择性必修2(已下线)3.2.2 共价晶体课堂例题
3 . 下列有关晶体结构或性质的描述中正确的是
A.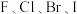 与金属 与金属 形成的卤化物,离子键键能越小,还原性越强 形成的卤化物,离子键键能越小,还原性越强 |
| B.冰中存在非极性共价键、分子间作用力和氢键 |
C.金属性 ,但金属钾的熔点低于金属钠 ,但金属钾的熔点低于金属钠 |
D.物质的量均为 的金刚石与石墨晶体所含的 的金刚石与石墨晶体所含的 键的数目相同 键的数目相同 |
您最近一年使用:0次
4 . 石墨烯是单层碳原子排列成的蜂窝状六角平面晶体,具有重要的应用前景。可利用碳化硅制备高品质石墨烯材料。下列说法正确的是
| A.24 g石墨烯约含1 mol六元碳环 |
| B.碳化硅晶胞与金刚石晶胞结构相似 |
| C.石墨烯的熔点低于碳化硅 |
| D.利用碳化硅制备石墨烯的过程属于物理剥离 |
您最近一年使用:0次
解题方法
5 . 下列关于物质熔、沸点的比较不正确的是( )
| A.Si、SiC、金刚石的熔点依次降低 |
| B.SiCl4、MgBr2、氮化硼的熔点依次升高 |
| C.F2、Cl2、Br2、I2的沸点依次升高 |
| D.AsH3、PH3、NH3的沸点依次升高 |
您最近一年使用:0次
2020-05-14更新
|
135次组卷
|
2卷引用:山东省泰安市新泰市第二中学2019-2020学年高二下期中考试化学试题
解题方法
6 . 下表是某些原子晶体的熔点和硬度。
分析表中的数据,判断下列叙述正确的是( )
| 原子晶体 | 金刚石 | 氮化硼 | 碳化硅 | 硅 | 锗 |
| 熔点/℃ | 3350 | 3000 | 2600 | 1415 | 938.4 |
| 硬度 | 10 | 9.5 | 9.0 | 7.0 | 6.0 |
分析表中的数据,判断下列叙述正确的是( )
| A.构成原子晶体的原子种类越多,晶体的熔点越高 |
| B.构成原子晶体的原子间的共价键键能越大,晶体的熔点越高 |
| C.构成原子晶体的原子的半径越大,晶体的硬度越大 |
| D.构成原子晶体的原子的半径越大,晶体的硬度越小 |
您最近一年使用:0次
2020-04-11更新
|
272次组卷
|
2卷引用:课时1 原子晶体——A学习区 夯实基础(鲁科版选修3)
名校
7 . 如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法正确的是


| A.X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| B.由X、Y和氢三种元素可以形成离子化合物 |
| C.物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 |
| D.T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
您最近一年使用:0次
8 . 下列对一些实验事实及其理论解释都正确的是
选项 | 实验事实 | 理论解释 |
A | Be原子的第一电离能小于B原子 | 同周期元素原子的电离能随原子序数增大而增大 |
B | CH4为正四面体形分子 | CH4分子中C为sp3杂化,键角为109°28′ |
C | 金刚石的熔点高于石墨 | 金刚石是原子晶体,石墨是分子晶体 |
D | HF的沸点高于HCl | HF分子间能形成氢键,HCl不能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 据报导用激光将置于铁室中的石墨靶上的碳原子“炸松”,与此同时再用一个射频电火花喷射出氮气,此时碳、氮原子结合成碳氮化合物的薄膜,该膜的硬度可比金刚石更坚硬,其原因可能是
| A.碳、氮原子构成网状的原子晶体 |
| B.膜中的C—N键长比金刚石的C—C键长短 |
| C.碳、氮都是非金属,化合时放出大量热 |
| D.相邻主族非金属的化合物比单质硬度大 |
您最近一年使用:0次
2016-12-09更新
|
250次组卷
|
2卷引用:2014-2015江苏省南通中学高二上学期期末化学(理)试卷



