解题方法
1 . 图1为某 晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。
晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。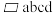 为所取晶胞的下底面,为锐角等于
为所取晶胞的下底面,为锐角等于 的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
 晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。
晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。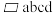 为所取晶胞的下底面,为锐角等于
为所取晶胞的下底面,为锐角等于 的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
| A.befc | B.kecb | C.jkba | D.dchg |
您最近一年使用:0次
名校
解题方法
2 . 下表为长式周期表的一部分,其中的序号代表对应的元素。
(1)写出上表中元素⑨的三价离子的结构示意图_______ 。
(2)元素⑩的晶体中原子堆积方式是_______ ,晶体中原子的空间利用率是_______
(3)元素②的第二电离能_______ Na(填写“>”“=”或“<”)的第二电离能;元素⑨的氧化物MXO晶体晶胞结构为NaCl型,由于晶体缺陷,x值为0.88,若晶体中的M分别为M2﹢、M3﹢,此晶体中M2﹢与M3﹢的最简整数比为_______
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______ 。
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为_______ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ |
(2)元素⑩的晶体中原子堆积方式是
(3)元素②的第二电离能
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是
(5)用惰性电极电解足量的由元素⑦与元素⑧形成的化合物的水溶液,写出电解反应的离子方程式为
您最近一年使用:0次
3 . 金是一种贵重金属,抗腐蚀,是延展性最好的金属之一。负载型金纳米材料在催化动态催化理论、光学、电子学等方面有重要作用。
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为_______ 。
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是_______ 。
Ⅱ.金的提取
硫脲(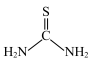 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是_______ 。
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:
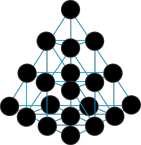
(4)该金团簇的化学式为_______ (填字母)。
a.Au b.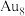 c.
c.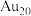
(5)该金团簇中有_______ 种不同化学环境的金原子。
Ⅰ.金的结构
(1)金元素位于元素周期表第6周期ⅠB族,金的价电子排布式为
(2)金晶体的晶胞为面心立方晶胞,Au在晶胞中的配位数是
Ⅱ.金的提取
硫脲(
 )液相提金原理:
)液相提金原理:
(3)硫脲易溶于水,原因是
Ⅲ.金的应用
一种最稳定的负载型纳米金团簇,具有最完美的对称性,其结构如图所示:

(4)该金团簇的化学式为
a.Au b.
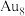 c.
c.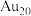
(5)该金团簇中有
您最近一年使用:0次
4 . 某纳米钛铝合金晶胞结构如图甲(Al、Ti各有1个原子在晶胞内部),金属铬的晶胞如图乙所示,已知铬的密度为ρg•cm-3,阿伏加德罗常数为NA。下列说法中正确的是


| A.甲中Al与Ti原子个数比为11∶5 |
| B.1个基态Ti原子中含有4个未成对电子 |
| C.乙中与铬原子距离最近的铬原子共有12个 |
D.铬原子的半径r= × ×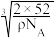 ×1010pm ×1010pm |
您最近一年使用:0次
5 . 下列有关说法不正确 的是
 氢原子的电子云 |  金属Cu的晶胞结构 | 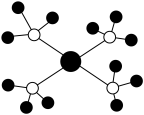 四氨合铜离子 |  CaF2晶胞结构 |
| A.电子云密度大的区域电子数目多 | B.晶胞中每个Cu原子周围有12个紧邻的原子 | C.铜离子与氨分子中的氮原子形成4个配位键 | D.每个CaF2晶胞平均占有4个Ca2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
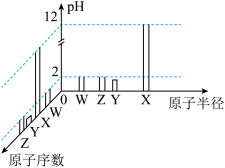
6 . 已知W、X、Y、Z为短周期元素,R外围电子的电子排布式为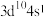 。常温下,W、X、Y、Z的最高价氧化物对应的水化物溶液(浓度均为
。常温下,W、X、Y、Z的最高价氧化物对应的水化物溶液(浓度均为 )的pH和原子半径、原子序数的关系如图所示。回答下列问题。
)的pH和原子半径、原子序数的关系如图所示。回答下列问题。
(1)R位于元素周期表中第_______ 周期第_______ 族。
(2)写出化合物 的电子式
的电子式_______ 。
(3)基态Z原子中存在未成对电子的能级,画出Z原子该能级的轨道表示式_______ 。
(4)XZ晶体中,其化学键的牢固程度可用_______ 衡量。
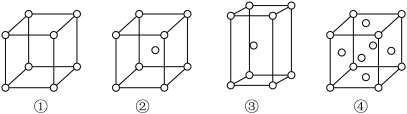
(5)有四种不同堆积方式的金属晶体的晶胞如下图所示,单质R晶体的堆积方式是_______ (填序号),其二维空间的排列方式为_______ (填“非密置层”或“密置层”)。
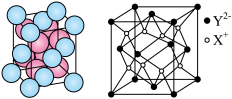
(6) 的晶胞如下图所示,设
的晶胞如下图所示,设 的半径为
的半径为 ,
, 的半径为
的半径为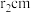 。该晶体中每个
。该晶体中每个 周围与它最接近且距离相等的
周围与它最接近且距离相等的 共有
共有_______ 个, 的配位数为
的配位数为_______ 。 晶体的密度为
晶体的密度为_______  。(阿伏加德罗常数的值用
。(阿伏加德罗常数的值用 表示,写表达式,不化简)。
表示,写表达式,不化简)。
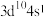 。常温下,W、X、Y、Z的最高价氧化物对应的水化物溶液(浓度均为
。常温下,W、X、Y、Z的最高价氧化物对应的水化物溶液(浓度均为 )的pH和原子半径、原子序数的关系如图所示。回答下列问题。
)的pH和原子半径、原子序数的关系如图所示。回答下列问题。
(1)R位于元素周期表中第
(2)写出化合物
 的电子式
的电子式(3)基态Z原子中存在未成对电子的能级,画出Z原子该能级的轨道表示式
(4)XZ晶体中,其化学键的牢固程度可用
(5)有四种不同堆积方式的金属晶体的晶胞如下图所示,单质R晶体的堆积方式是

(6)
 的晶胞如下图所示,设
的晶胞如下图所示,设 的半径为
的半径为 ,
, 的半径为
的半径为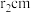 。该晶体中每个
。该晶体中每个 周围与它最接近且距离相等的
周围与它最接近且距离相等的 共有
共有 的配位数为
的配位数为 晶体的密度为
晶体的密度为 。(阿伏加德罗常数的值用
。(阿伏加德罗常数的值用 表示,写表达式,不化简)。
表示,写表达式,不化简)。
您最近一年使用:0次
解题方法
7 . 金的晶胞结构如图所示(假设晶胞参数为anm),下列说法错误的是
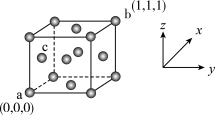

| A.金原子在晶胞中的空间利用率约为74% |
B.c原子的坐标为 ( ,0, ,0, ) ) |
C.该晶体的密度为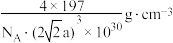 |
D.金晶胞沿z轴方向的投影图为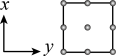 |
您最近一年使用:0次
2023-04-24更新
|
729次组卷
|
4卷引用:河南省创新发展联盟2022-2023学年高二下学期第二次联考(期中)化学试题
河南省创新发展联盟2022-2023学年高二下学期第二次联考(期中)化学试题河南省新乡市2022-2023学年高二下学期4月期中考试化学试题(已下线)专题11 根据投影推断晶胞结构(已下线)微题型02 晶体结构及相关计算-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
解题方法
8 . 下列有关晶体堆积模型和晶胞的说法错误的是


| A.图①、图②和图③都是最密堆积,图④的空间占有率是图中最小的 |
| B.从左至右的配位数依次为12、12、12、6、8 |
| C.图①可以表示氯化钠晶胞中氯离子的堆积方式 |
| D.铜晶体、碳化硅晶体中的硅原子、硫化锌晶体中的硫离子都采用图③中的最密堆积 |
您最近一年使用:0次
21-22高二下·全国·单元测试
解题方法
9 . 金属晶体
(1)在金属晶体中,原子间以_____________ 相结合。
(2)金属晶体的性质:优良的_____________ 、_____________ 和_____________ 。
(1)在金属晶体中,原子间以
(2)金属晶体的性质:优良的
您最近一年使用:0次
名校
10 . 铜及其化合物在工农业生产中有广泛的应用。
Ⅰ.金属铜的原子堆积模型如图-1所示,
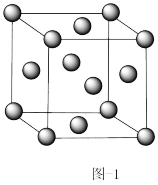
(1)该晶胞中每个Cu原子周围最近距离的Cu原子数目为_______ 。
Ⅱ. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(2)向 溶液中加入过量NaOH溶液可生成
溶液中加入过量NaOH溶液可生成 。
。 中除了配位键外,还存在的化学键类型有_______(填字母)。
中除了配位键外,还存在的化学键类型有_______(填字母)。
(3)将CuO投入 、
、 的混合溶液中进行“氨浸”,控制温度为50~55℃,pH约为9.5,CuO转化为
的混合溶液中进行“氨浸”,控制温度为50~55℃,pH约为9.5,CuO转化为 溶液。
溶液。
①CuO被浸取的离子方程式为_______ 。
② 结构中,若用两个
结构中,若用两个 分子代替两个
分子代替两个 分子,可以得到两种不同结构的化合物,由此推测
分子,可以得到两种不同结构的化合物,由此推测 的空间构型为
的空间构型为_______ 。
(4) 可以与乙二胺(
可以与乙二胺(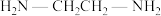 )形成配离子,如题图-2所示:
)形成配离子,如题图-2所示:
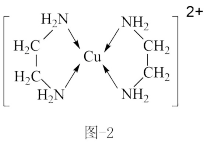
③H、O、N三种元素的电负性从大到小的顺序为_______ 。
④乙二胺分子中N原子成键时采取的杂化类型是_______ 。乙二胺和三甲胺 均属于胺,但乙二胺比三甲胺的沸点高很多,原因是
均属于胺,但乙二胺比三甲胺的沸点高很多,原因是_______ 。
Ⅲ.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,
(5)下列物质中,属于顺磁性物质的是_______ (填标号)。
A. B.
B. C.
C.
Ⅰ.金属铜的原子堆积模型如图-1所示,

(1)该晶胞中每个Cu原子周围最近距离的Cu原子数目为
Ⅱ.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(2)向
 溶液中加入过量NaOH溶液可生成
溶液中加入过量NaOH溶液可生成 。
。 中除了配位键外,还存在的化学键类型有_______(填字母)。
中除了配位键外,还存在的化学键类型有_______(填字母)。| A.离子键 | B.金属键 | C.极性共价键 | D.非极性共价键 |
 、
、 的混合溶液中进行“氨浸”,控制温度为50~55℃,pH约为9.5,CuO转化为
的混合溶液中进行“氨浸”,控制温度为50~55℃,pH约为9.5,CuO转化为 溶液。
溶液。①CuO被浸取的离子方程式为
②
 结构中,若用两个
结构中,若用两个 分子代替两个
分子代替两个 分子,可以得到两种不同结构的化合物,由此推测
分子,可以得到两种不同结构的化合物,由此推测 的空间构型为
的空间构型为(4)
 可以与乙二胺(
可以与乙二胺(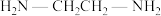 )形成配离子,如题图-2所示:
)形成配离子,如题图-2所示: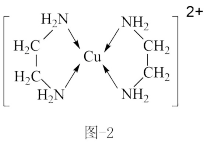
③H、O、N三种元素的电负性从大到小的顺序为
④乙二胺分子中N原子成键时采取的杂化类型是
 均属于胺,但乙二胺比三甲胺的沸点高很多,原因是
均属于胺,但乙二胺比三甲胺的沸点高很多,原因是Ⅲ.将含有未成对电子的物质置于外磁场中,会使磁场强度增大,称其为顺磁性物质,
(5)下列物质中,属于顺磁性物质的是
A.
 B.
B. C.
C.
您最近一年使用:0次
2022-11-11更新
|
1508次组卷
|
4卷引用:江苏省苏州市2022-2023学年高二上学期期中调研化学试卷



