名校
1 . 化工产品中,含氯物质众多,其用途广泛。回答下列问题:
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为_______ (填化学式)。

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为_______ mol/L。
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为_______ 、_______ 。
②“转化”发生反应的离子方程式为_______ 。
(1)如图为氯及其化合物的“价-类”二维图。缺失的物质B为

(2)次氯酸钠是一种含氯物质,取含次氯酸钠14.9g/L的“84”消毒液1mL,加水稀释至100mL,则稀释后的溶液中次氯酸钠的物质的量浓度为
(3)电石渣[主要成分为Ca(OH)2]是氯碱工业中的废料,某同学在实验室以电石渣为原料制取KClO3的工艺流程如图所示:

已知:Ca(ClO3)2易溶于水。
①“一系列操作”为
②“转化”发生反应的离子方程式为
您最近一年使用:0次
名校
2 . 溶液在日常生活、工农业生产和科学研究中具有广泛用途。
(1)60℃时,KNO3的溶解度为_______ 。
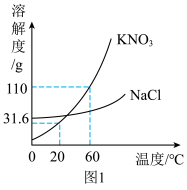
(2)20℃时,将20gKNO3加入到50g水中,充分溶解后所得溶液的质量为_______ g。
(3)除去KNO3溶液中混有的少量的NaCl,提纯的方法是_______ 。
(4)60℃,将KNO3和NaCl两种物质的饱和溶液降温至20℃,质量分数的大小关系为_______ 。
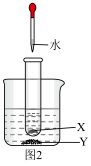
(5)探究温度对溶解度的影响,如图2所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体则余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合有_______ 。
(1)60℃时,KNO3的溶解度为

(2)20℃时,将20gKNO3加入到50g水中,充分溶解后所得溶液的质量为
(3)除去KNO3溶液中混有的少量的NaCl,提纯的方法是
(4)60℃,将KNO3和NaCl两种物质的饱和溶液降温至20℃,质量分数的大小关系为
(5)探究温度对溶解度的影响,如图2所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体则余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合有

您最近一年使用:0次
3 . 海水是一种丰富的资源,工业上可从海水中提取多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。

回答下列问题:
(1)流程图中操作a的名称为________ 。(填序号)
A、蒸发结晶 B、降温结晶
(2)生产生石灰的方程式__________________________ 。从离子反应的角度思考,往海水中加入石灰乳的作用是____________________ 。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是_____________ 。
②操作b是在________ 氛围中进行,若在空气中加热,则会生成Mg(OH)2,
写出有关反应的化学方程式:________________________________________ 。
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为__________ ,从考虑成本和废物循环利用的角度,副产物氯气可以用于_______________ 。

回答下列问题:
(1)流程图中操作a的名称为
A、蒸发结晶 B、降温结晶
(2)生产生石灰的方程式
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是
②操作b是在
写出有关反应的化学方程式:
(4)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
您最近一年使用:0次
2019-01-19更新
|
465次组卷
|
2卷引用:河南省南阳市内乡县菊潭高级中学2022届高三入学考试化学试题
解题方法
4 . 钼酸钠(Na2MoO4)具有广泛的用途.可做新型水处理荆、优良的金属缓蚀剂及可用于局部过热的循环水系统;Al(OH)3工业和医药上都具有重要用途.现从某废钼催化剂(主要成分MoO3、Al2O3、Fe2O3等)中回收Na2MoO4和Al(OH)3,其工艺如图:
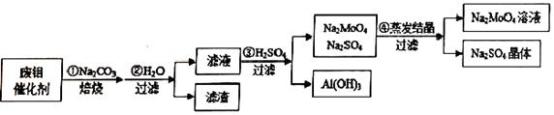
回答下列问题:
(1)已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应,试写出MoO3与Na2CO3反应的化学方程式:__________________ 。
(2)第②步操作所后的滤液中,溶质有Na2MoO4、_________ 和过量的Na2CO3;检验第②步操作所得滤渣中含有三价铁的方法是___________________ 。
(3)第③步操作H2SO4需要适量,通常是通过_________ 来调控H2SO4的用量;与Na2SO4相比,Na2MoO4的溶解度受温度的影响变化__________ (填“较大”或“较小”)。
(4)利用铝热反应可回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3。写出MoO3发生铝热反应的化学方程式:_________________ 。
(5)取废钼催化剂5.00g,加入5.30gNa2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39gNa2SO4晶体,则废钼催化剂中Al2O3、MoO3的物质的量的比值为_______ 。

回答下列问题:
(1)已知MoO3、Al2O3与SiO2相似,均能在高温下跟Na2CO3发生类似反应,试写出MoO3与Na2CO3反应的化学方程式:
(2)第②步操作所后的滤液中,溶质有Na2MoO4、
(3)第③步操作H2SO4需要适量,通常是通过
(4)利用铝热反应可回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得MoO3。写出MoO3发生铝热反应的化学方程式:
(5)取废钼催化剂5.00g,加入5.30gNa2CO3(足量),经上述实验操作后,最终得到2.34g Al(OH)3和6.39gNa2SO4晶体,则废钼催化剂中Al2O3、MoO3的物质的量的比值为
您最近一年使用:0次



