2024·重庆·模拟预测
1 . 叠氮化钠(NaN3)在防腐、有机合成和汽车行业有着广泛的用途。用氨基钠(NaNH2)制取叠氮化钠的方程式为: 实验室用下列装置制取叠氮化钠。
实验室用下列装置制取叠氮化钠。
(1)仪器a的名称是_______ 。
(2)装置B、D的主要作用分别是_______ 。
(3)检查装置A的气密性的操作是_______ 。
(4)装置A中反应除生成装置C中需要的物质外,还生成SnCl4等。其反应的化学方程式为_______ 。
(5)装置C处充分反应后,应先停止加热,再关闭分液漏斗活塞,原因是_______ 。
(6)取mg反应后装置C中所得固体,用下图所示装置测定产品的纯度(原理为:加入ClO将N1氧化成N2,测定N2的体积,从而计算产品纯度)。_______ 。
②若G的初始读数为V1mL、末读数为V2mL,本实验条件下气体摩尔体积为VL·mol-1,则产品中NaN3的质量分数为_______ 。
 实验室用下列装置制取叠氮化钠。
实验室用下列装置制取叠氮化钠。
(1)仪器a的名称是
(2)装置B、D的主要作用分别是
(3)检查装置A的气密性的操作是
(4)装置A中反应除生成装置C中需要的物质外,还生成SnCl4等。其反应的化学方程式为
(5)装置C处充分反应后,应先停止加热,再关闭分液漏斗活塞,原因是
(6)取mg反应后装置C中所得固体,用下图所示装置测定产品的纯度(原理为:加入ClO将N1氧化成N2,测定N2的体积,从而计算产品纯度)。
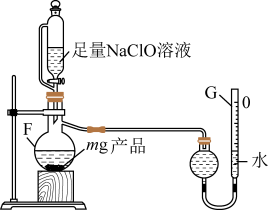
②若G的初始读数为V1mL、末读数为V2mL,本实验条件下气体摩尔体积为VL·mol-1,则产品中NaN3的质量分数为
您最近半年使用:0次
2024高三·全国·专题练习
解题方法
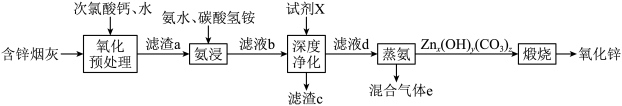
2 . 氧化锌在橡胶、油漆涂料、化工、医疗及食品等行业有着广泛应用。一种以含锌烟灰(含有ZnO、CuO、PbO、FeO、Fe2O3、MnO、MnO2、CdO等)为原料制备氧化锌的工艺流程如图所示:
②25℃时相关物质的Ksp如下表:
③ Zn(OH)2和ZnCO3的分解温度分别为125℃、300℃。
请回答下列问题:
(1)“氧化预处理”阶段得到的氧化产物有FeOOH、MnO2,写出生成FeOOH的离子方程式:___________ ;“氧化预处理”的目的是___________ 。
(2)若“氨浸”阶段溶解ZnO时消耗的n(NH3·H2O)∶n(NH4HCO3)=2∶1,写出该反应的离子方程式:___________ 。
(3)实验室模拟蒸氨装置如图所示。蒸氨时控制温度为95℃左右,在装置b中[Zn(NH3)4]2+转化为碱式碳酸锌沉淀。___________ (填字母)。
A.液面上方但不接触液面 B.略伸入液面下 C.伸入溶液底部
②在不改变水蒸气的温度、浸出液用量和蒸氨时间的条件下,为提高蒸氨效率和锌的沉淀率,可采取的措施是___________ (写出一种)。
③混合气体e可返回至“___________ ”阶段循环利用。
(4)研究发现Znx(OH)y(CO3)z热分解得到ZnO的过程可分为两步。
某实验小组取11.2 g Znx(OH)y(CO3)z固体进行热重分析,两步反应的固体失重率( ×100%)依次为8.0%、19.6%,则Znx(OH)y(CO3)z的化学式为
×100%)依次为8.0%、19.6%,则Znx(OH)y(CO3)z的化学式为___________ 。
②25℃时相关物质的Ksp如下表:
| 物质 | MnS | FeS | ZnS | PbS | CdS | CuS |
| Ksp | 2.5×10-13 | 6.3×10-18 | 1.6×10-24 | 8.0×10-28 | 3.6×10-29 | 5.0×10-36 |
请回答下列问题:
(1)“氧化预处理”阶段得到的氧化产物有FeOOH、MnO2,写出生成FeOOH的离子方程式:
(2)若“氨浸”阶段溶解ZnO时消耗的n(NH3·H2O)∶n(NH4HCO3)=2∶1,写出该反应的离子方程式:
(3)实验室模拟蒸氨装置如图所示。蒸氨时控制温度为95℃左右,在装置b中[Zn(NH3)4]2+转化为碱式碳酸锌沉淀。
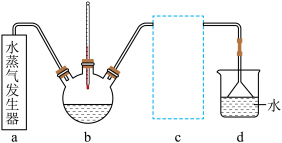
A.液面上方但不接触液面 B.略伸入液面下 C.伸入溶液底部
②在不改变水蒸气的温度、浸出液用量和蒸氨时间的条件下,为提高蒸氨效率和锌的沉淀率,可采取的措施是
③混合气体e可返回至“
(4)研究发现Znx(OH)y(CO3)z热分解得到ZnO的过程可分为两步。
某实验小组取11.2 g Znx(OH)y(CO3)z固体进行热重分析,两步反应的固体失重率(
 ×100%)依次为8.0%、19.6%,则Znx(OH)y(CO3)z的化学式为
×100%)依次为8.0%、19.6%,则Znx(OH)y(CO3)z的化学式为
您最近半年使用:0次
名校
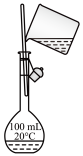
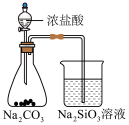
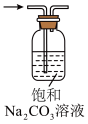
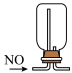
3 . 下列实验装置或操作能够达到实验目的的是
| A | B | C | D |
|
|
|
|
| 转移溶液 | 验证碳酸酸性强于硅酸 | 除去 中混有的少量HCl 中混有的少量HCl | 收集NO |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7日内更新
|
549次组卷
|
4卷引用:四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题
四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题(已下线)押题卷02(15+4题型) -2024高考化学考点必杀300题(新高考通用)广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题
4 . 无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。___________ 。
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。已知:氯化亚砜(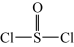 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。

您最近半年使用:0次
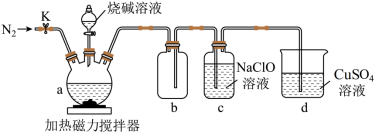
5 . 某兴趣小组设计如图实验装置制备次磷酸钠( )。
)。
已知:①白磷( )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。
② 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。_______ ,检查装置气密性后,应先打开K通入 一段时间,目的是
一段时间,目的是_______ 。
 )。
)。已知:①白磷(
 )在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成
)在空气中可自燃,与过量烧碱溶液混合,80~90℃时反应生成 和
和 。
。②
 是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成
是一种有强还原性的有毒气体,空气中可自燃,可与NaClO溶液反应生成 。
。
 一段时间,目的是
一段时间,目的是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
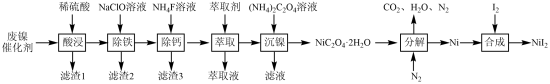
6 . 《自然》杂志公布最新科学研究成果:碘化镍(NiI2)在二维形式上具有多铁性。某小组以废镍催化剂(主要成分是Ni,含少量Zn、Fe、CaO、SiO2等杂质)为原料制备碘化镍的流程如下:
(1)滤渣1的成分是CaSO4、___________ (填化学式)。滤渣2经过洗涤、干燥、___________ (填操作名称)可制铁红。
(2)“萃取"中,萃取剂的密度小于1 g·cm-3,若在实验室中分离萃取液,操作是___________ (填操作名称)。
(1)滤渣1的成分是CaSO4、
(2)“萃取"中,萃取剂的密度小于1 g·cm-3,若在实验室中分离萃取液,操作是
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
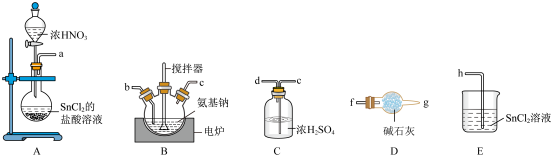
7 . 叠氮化钠(NaN3)可用作汽车安全气囊的气体发生剂。某小组对叠氮化钠的制备和产品纯度测定进行相关探究。
查阅资料:①叠氮化钠可以由氨基钠(NaNH2)和N2O为原料加热制得,其中N2O的制备反应为 。
。
②氨基钠易氧化、易潮解;NaN3能与强酸反应生成HN3,HN3不稳定,易爆炸。
③N2O有强氧化性,不与酸、碱反应。
回答下列问题:
Ⅰ.制备NaN3_______ →h。
查阅资料:①叠氮化钠可以由氨基钠(NaNH2)和N2O为原料加热制得,其中N2O的制备反应为
 。
。②氨基钠易氧化、易潮解;NaN3能与强酸反应生成HN3,HN3不稳定,易爆炸。
③N2O有强氧化性,不与酸、碱反应。
回答下列问题:
Ⅰ.制备NaN3
您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
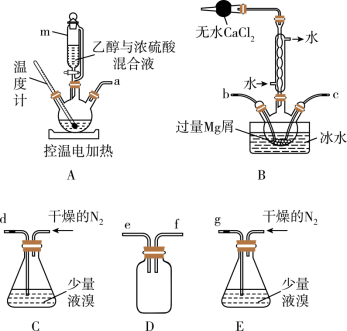
8 . 无水溴化镁常常做催化剂。选用如图所示装置(夹持装置略)采用镁屑与液溴为原料制备无水MgBr2。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是_______ 。
(2)装置A中使用仪器m的优点是_______ 。
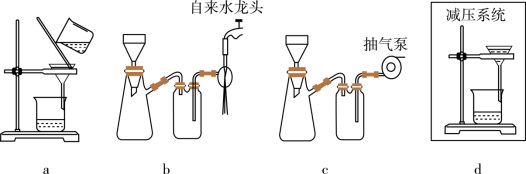
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是_______ (填序号)。_______ 。
①乙醚的熔点为34.6℃,沸点为132℃。
②Mg和Br2剧烈反应,放出大量的热;MgBr2具有强吸水性;MgBr2能与乙醚发生反应MgBr2+3C2H5OC2H5→MgBr2•3C2H5OC2H5。
实验主要步骤如下:
Ⅰ.选用上述部分装置,正确连接,检查装置的气密性。向装置中加入药品。
Ⅱ.加热装置A,迅速升温至140℃,并保持140℃加热一段时间,停止加热。
Ⅲ.通入干燥的氮气,让液溴缓慢进入装置B中,直至完全加入。
IV.装置B中反应完毕后恢复至室温,过滤反应物,将得到的滤液转移至干燥的烧瓶中,在冰水中冷却,析出晶体,再过滤得三乙醚合溴化镁粗产品。
V.用苯洗涤粗产品,减压过滤,得三乙醚合溴化镁,将其加热至160℃分解得无水MgBr2。回答下列问题:
(1)装置D的作用是
(2)装置A中使用仪器m的优点是
(3)步骤V采用减压过滤(使容器内压强降低,以达到固液快速分离)。下列装置可用作减压过滤的是
您最近半年使用:0次
9 . “单原子催化”已经成为催化领域的研究前沿。一种Ru单原子催化剂用于生物质基醛/酮的还原胺化反应如图:RCHO RCH2NH2。实验装置如图所示:
RCH2NH2。实验装置如图所示:_______ ,使用前,检查仪器甲气密性的操作是:_______ 。
(2)以上各仪器接口的连接顺序是______→gh←________。________
(3)装置E中反应温度为100℃,加热方式不宜使用水浴加热,原因是_______ 。加热E装置前,须先通入一段时间的H2,目的是_______ 。
 RCH2NH2。实验装置如图所示:
RCH2NH2。实验装置如图所示: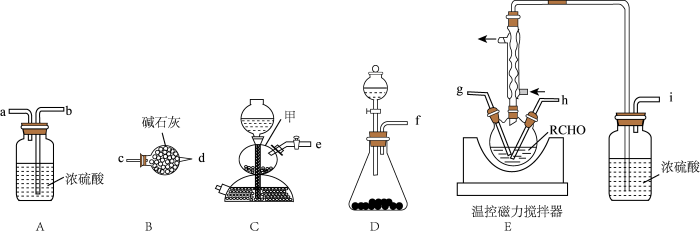
(2)以上各仪器接口的连接顺序是______→gh←________。
(3)装置E中反应温度为100℃,加热方式不宜使用水浴加热,原因是
您最近半年使用:0次
10 . 连二亚硫酸钠(Na2S2O4),也称为保险粉,Na2S2O4)易溶于水,难溶于甲醇,具有极强的还原性,易被空气氧化,在碱性介质中稳定。工业上常用制备Na2S2O4的方法有I.锌粉法、II.甲酸钠法。
I.实验室模拟锌粉法的装置如图(加热等辅助仪器略去)
Zn+2SO2=ZnS2O4
ZnS2O4+2NaOH=Zn(OH)2↓+Na2S2O4
(1)①装置A中分液漏斗中的试剂是_______ 。
A.稀硫酸B.98%的硫酸C.70%的硫酸
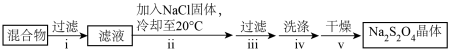
②装置B中反应结束后,取出混合物进行以下操作,得到Na2S2O4晶体。_______ 。
I.实验室模拟锌粉法的装置如图(加热等辅助仪器略去)

Zn+2SO2=ZnS2O4
ZnS2O4+2NaOH=Zn(OH)2↓+Na2S2O4
(1)①装置A中分液漏斗中的试剂是
A.稀硫酸B.98%的硫酸C.70%的硫酸
②装置B中反应结束后,取出混合物进行以下操作,得到Na2S2O4晶体。
您最近半年使用:0次