名校
1 . Ⅰ.某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
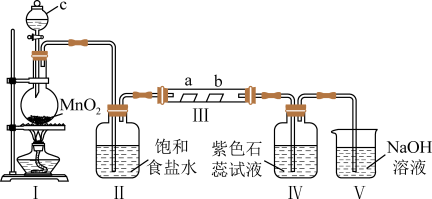
(1)装置Ⅰ中仪器c的名称是_______ ,写出装置Ⅰ中制备Cl2的化学方程式为_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的_______ 装置(填序号)。

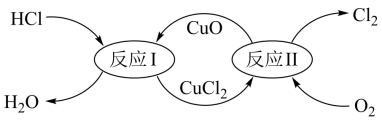
(4)“地康法”制取Cl2的反应原理如图所示,在450℃条件下,反应Ⅱ的化学方程式为_______ 。
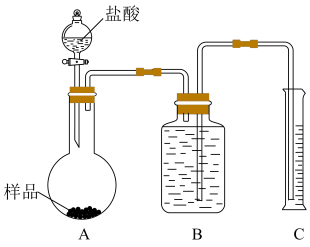
Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组设计了如下实验方案。
(5)把一定质量的样品与足量盐酸反应后,用如图所示装置测定产生CO2气体的体积,为了使测量结果准确,B中溶液选用_______ ,但选用该溶液后实验结果仍然不够准确,可能的原因是_______ 。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

(4)“地康法”制取Cl2的反应原理如图所示,在450℃条件下,反应Ⅱ的化学方程式为

Ⅱ.工业上碳酸钠大多采用侯氏制碱法制取,所得碳酸钠样品中往往含有少量的NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组设计了如下实验方案。
(5)把一定质量的样品与足量盐酸反应后,用如图所示装置测定产生CO2气体的体积,为了使测量结果准确,B中溶液选用

您最近一年使用:0次
2023-01-19更新
|
339次组卷
|
2卷引用: 湖北省武汉市新洲区第一中学2022--2023学年高一上学期阶段检测化学试题
2 . I. 某中学研究性学习小组为探究碳酸钠和碳酸氢钠两种物质的某些性质、进行了如下实验,如图Ⅰ~Ⅳ所示:
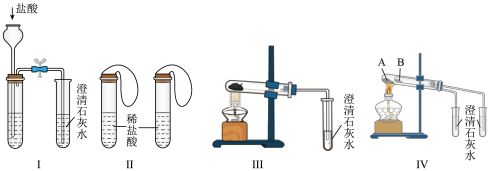
(1)若用实验Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是__________ ,现象是___________________ 。
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号)_____________ 。
(3)为测定Na2CO3和NaHCO3混合物中Na2CO3质量分数,采用实验Ⅲ进行实验,取a克混合物充分加热,最后减重b克,则碳酸钠的质量分数为___________ (用含有a、b的数学式表示)。
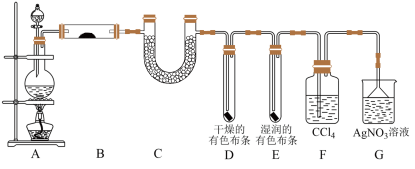
II.该研究性学习小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。
已知:Cl2易溶于CCl4而HCl不溶于CCl4
按要求回答问题:
(4)写出装置A制取Cl2的化学方程式_________________________ 。
(5)装置B中的试剂是_______________ ,现象是________________ 。
(6)装置D和E中出现的不同现象说明的问题是_________________ 。
(7)装置F的作用是______________________ 。
(8)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在F和D之间再连接一个洗气瓶装置,则装置中应放入_______________________ (填写试剂或用品名称),改正后证明有HCl挥发出来的现象是_______________________ 。

(1)若用实验Ⅳ来验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是
(2)若用实验来鉴别碳酸钠和碳酸氢钠两种固体,能达到实验目的的是(填装置序号)
(3)为测定Na2CO3和NaHCO3混合物中Na2CO3质量分数,采用实验Ⅲ进行实验,取a克混合物充分加热,最后减重b克,则碳酸钠的质量分数为
II.该研究性学习小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略)。
已知:Cl2易溶于CCl4而HCl不溶于CCl4

按要求回答问题:
(4)写出装置A制取Cl2的化学方程式
(5)装置B中的试剂是
(6)装置D和E中出现的不同现象说明的问题是
(7)装置F的作用是
(8)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在F和D之间再连接一个洗气瓶装置,则装置中应放入
您最近一年使用:0次
3 . 实验目的:为研究铁质材料与热浓硫酸的反应
(1)称取铁钉(碳素钢 ) 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。
①甲同学认为 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为___________ (选填序号)
A. 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液
②乙同学取 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为___________ 。(保留三位有效数字)。
(2)分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是___________ 。

(3)装置A中试剂的作用是___________ ,反应的离子方程式___________ 。
(4)简述确认气体Y中含有 的实验现象
的实验现象___________ 。
(5)如果气体Y中含有 ,预计实验现象应是
,预计实验现象应是___________ 。
(1)称取铁钉(
 放入
放入 浓硫酸中,加热,充分反应后得到溶液
浓硫酸中,加热,充分反应后得到溶液 并收集到气体
并收集到气体 。
。①甲同学认为
 中除
中除 外还可能含有
外还可能含有 。若要确认其中是否含有
。若要确认其中是否含有 ,应选择加入的试剂为
,应选择加入的试剂为A.
 溶液和氯水 B.铁粉和
溶液和氯水 B.铁粉和 溶液 C.浓氨水 D.酸性
溶液 C.浓氨水 D.酸性 溶液
溶液②乙同学取
 (标准状况)气体
(标准状况)气体 通入足量溴水中,然后加入足量
通入足量溴水中,然后加入足量 溶液,经适当操作后得到干燥固体
溶液,经适当操作后得到干燥固体 。据此推知气体
。据此推知气体 中
中 的体积分数为
的体积分数为(2)分析上述实验中
 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和
和 气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有
气体。为此设计了下列探究实验装置(图中夹持仪器省略)。气体Y中还有 的原因是
的原因是
(3)装置A中试剂的作用是
(4)简述确认气体Y中含有
 的实验现象
的实验现象(5)如果气体Y中含有
 ,预计实验现象应是
,预计实验现象应是
您最近一年使用:0次
2021-10-10更新
|
285次组卷
|
5卷引用:2014-2015江西省临川市第一中学高一上学期期末化学试卷
名校
解题方法
4 . 回答下列问题:
(1)已知白磷的着火点为40℃,下列实验能达到实验目的的是_______ 。
(2)气体制备、收集是初中化学的重要知识。请结合如图所示装置回答有关问题。

(ⅰ)实验室常用醋酸钠和碱石灰两种固体混合物加热制得甲烷气体,甲烷不溶于水。制取甲烷的发生装置可选用_______ (填字母,下同),用D装置采用排水法收集甲烷,水从_______ (填“①”或“②”)端排入量筒。
(ⅱ)实验室制氨气是利用氯化铵和氢氧化钙的固体混合物加热的方法,写出制氨气的反应方程式_______ 。
(ⅲ)用装置C代替装置B制取二氧化碳的优点是_______ ;用D装置收集二氧化碳,则气体应从_______ (填“①”或“②”)端进入。
(1)已知白磷的着火点为40℃,下列实验能达到实验目的的是
| A | B | C | D |
 | 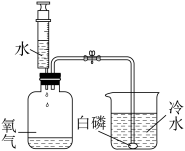 |  |  |
实验室制取 | 白磷在水中燃烧 | 防止铁丝生锈 | 测定空气里氧气含量 |

(ⅰ)实验室常用醋酸钠和碱石灰两种固体混合物加热制得甲烷气体,甲烷不溶于水。制取甲烷的发生装置可选用
(ⅱ)实验室制氨气是利用氯化铵和氢氧化钙的固体混合物加热的方法,写出制氨气的反应方程式
(ⅲ)用装置C代替装置B制取二氧化碳的优点是
您最近一年使用:0次
名校
5 . 化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图:
,实验流程如图:

(1)生成 的总反应的化学方程式为
的总反应的化学方程式为___________ 。
(2)从下图A~E中选择合适的仪器制备 ,正确的连接顺序是
,正确的连接顺序是___________ (按气流方向,用小写字母表示),B中使用雾化装置的优点是___________ 。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)反应完成后,将B中U形管内的混合物处理得到固体 和滤液:
和滤液:
灼烧 发生化学反应为:
发生化学反应为:___________ 。若灼烧前后固体质量减少1.24g,则生成的 的质量为
的质量为___________ g。
(4)工业纯碱中可能混有少量NaCl,同学们对工业纯碱样品展开探究。
探究一:确定纯碱样品中是否含有NaCl
有同学认为该实验方案有错误,正确方案应选用___________ (填字母)代替稀盐酸。
a. 溶液 b.稀硝酸 c.
溶液 b.稀硝酸 c. 溶液
溶液
探究二:测定纯碱样品中 的质量分数
的质量分数
【方案1】称取mg样品溶解,加入过量 溶液,搅拌至反应完全。过滤、洗涤、干燥,称量沉淀的质量为ng,则样品中
溶液,搅拌至反应完全。过滤、洗涤、干燥,称量沉淀的质量为ng,则样品中 的质量分数为
的质量分数为___________ 。
【方案2】如图所示,取样品于锥形瓶中,加入足量稀盐酸。反应结束后,根据干燥管增重计算 的质量分数。若结果大于100%,可能的原因是
的质量分数。若结果大于100%,可能的原因是___________ 。

 ,进一步处理得到产品
,进一步处理得到产品 和
和 ,实验流程如图:
,实验流程如图:
(1)生成
 的总反应的化学方程式为
的总反应的化学方程式为(2)从下图A~E中选择合适的仪器制备
 ,正确的连接顺序是
,正确的连接顺序是A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)反应完成后,将B中U形管内的混合物处理得到固体
 和滤液:
和滤液:灼烧
 发生化学反应为:
发生化学反应为: 的质量为
的质量为(4)工业纯碱中可能混有少量NaCl,同学们对工业纯碱样品展开探究。
探究一:确定纯碱样品中是否含有NaCl
| 实验操作 | 现象 | 结论 |
| 取样品加水溶解,加入过量稀盐酸至反应完全 | 有气泡产生 | 样品中有NaCl |
向上述溶液中继续滴加适量 溶液 溶液 | 有白色沉淀产生 |
a.
 溶液 b.稀硝酸 c.
溶液 b.稀硝酸 c. 溶液
溶液探究二:测定纯碱样品中
 的质量分数
的质量分数【方案1】称取mg样品溶解,加入过量
 溶液,搅拌至反应完全。过滤、洗涤、干燥,称量沉淀的质量为ng,则样品中
溶液,搅拌至反应完全。过滤、洗涤、干燥,称量沉淀的质量为ng,则样品中 的质量分数为
的质量分数为【方案2】如图所示,取样品于锥形瓶中,加入足量稀盐酸。反应结束后,根据干燥管增重计算
 的质量分数。若结果大于100%,可能的原因是
的质量分数。若结果大于100%,可能的原因是
您最近一年使用:0次
名校
解题方法
6 .  常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集
常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集 。
。

已知:① 固体在潮湿空气中容易变质,且易升华;
固体在潮湿空气中容易变质,且易升华;
②向含 的溶液中滴加
的溶液中滴加 溶液,生成深蓝色沉淀。
溶液,生成深蓝色沉淀。
请回答下列问题:
(1)仪器a的名称是___________ 。
(2)装置A圆底烧瓶中的固体为 ,请写出装置A中发生反应的离子方程式:
,请写出装置A中发生反应的离子方程式:___________ 。
(3)装置C中的试剂c的作用是___________ ,装置F中加入试剂d的作用是___________ 。
(4)实验时,应先点燃___________ (填“A”或“D”)处酒精灯,理由是___________ 。
(5)该兴趣小组想要对反应后装置D中剩余物质的成分进行检验,设计了如下的实验方案:
甲同学认为,实验Ⅲ中的现象无法说明反应后装置D中剩余物质中含有 ,原因是④
,原因是④___________ (用化学方程式 表示)。
 常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集
常用于污水处理、金属蚀刻等领域,某兴趣小组利用如图所示的实验装置制备并收集 。
。
已知:①
 固体在潮湿空气中容易变质,且易升华;
固体在潮湿空气中容易变质,且易升华;②向含
 的溶液中滴加
的溶液中滴加 溶液,生成深蓝色沉淀。
溶液,生成深蓝色沉淀。请回答下列问题:
(1)仪器a的名称是
(2)装置A圆底烧瓶中的固体为
 ,请写出装置A中发生反应的离子方程式:
,请写出装置A中发生反应的离子方程式:(3)装置C中的试剂c的作用是
(4)实验时,应先点燃
(5)该兴趣小组想要对反应后装置D中剩余物质的成分进行检验,设计了如下的实验方案:
| 实验序号 | 实验操作 | 预期现象 | 实验结论 |
| Ⅰ | 取少量D中的固体物质,用磁铁吸引 | 磁铁上吸引了黑色物质 | ① |
| Ⅱ | 另取少量固体于试管中,加入适量水溶解,向试管中滴加少量② | 固体物质完全溶解,③ | 固体中含有 |
| Ⅲ | 再取少量固体于试管中,加入适量水溶解,向试管中滴加 溶液 溶液 | 固体物质完全溶解,有深蓝色沉淀生成 | 固体中含有 |
 ,原因是④
,原因是④
您最近一年使用:0次
名校
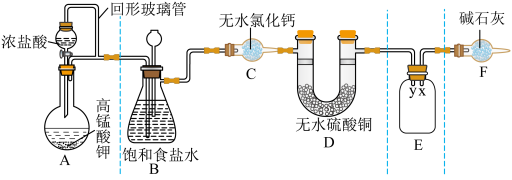
7 . 某同学用 与浓盐酸反应制备纯净的
与浓盐酸反应制备纯净的 的装置如图所示。回答下列问题:
的装置如图所示。回答下列问题:
已知: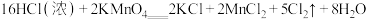
(1)装置A中盛放浓盐酸的仪器名称是
(2)E装置中导管(填“x”或“y”)
(3)装置F的作用有两个:一是
请写出氯气与碱石灰反应的化学方程式
(4)
 、HClO和
、HClO和 三种微粒的物质的量分数随pH(即
三种微粒的物质的量分数随pH(即 )变化的关系如图所示。
)变化的关系如图所示。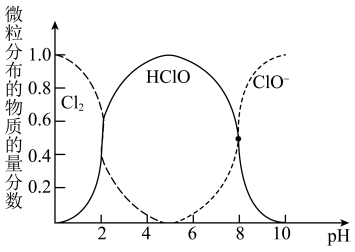
回答问题:①使用84消毒液时为增强消毒效果常调节4<pH<6,原因是
②通常购买的84消毒液pH在12左右,为增强消毒效果可向其中滴加
A.可口可乐 B.稀 C.食醋 D.浓盐酸
C.食醋 D.浓盐酸
(5)实验室将
 通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为
通入质量分数40%的NaOH溶液中来制备84消毒液。当NaOH消耗一半时转移电子数为 ,计算此时所得溶液中NaClO的质量分数为
,计算此时所得溶液中NaClO的质量分数为
您最近一年使用:0次
名校
8 . 回答下列问题。
Ⅰ.为测定金属钠样品(表面有Na2O )中钠单质的质量分数,设计了如下实验(反应装置如图所示,U形管中的无水CaCl2用作干燥剂)

①称量A、B装置的总质量
②称取一定质量的钠样品
③将钠样品投入锥形瓶中,迅速塞紧带U形干燥管的橡皮塞有关数据:A、B装置反应前总质量为ag,称取的金属钠样品质量为bg,反应后A、B总质量为cg。
请根据题意回答下列问题:
(1)钠与水反应的化学方程式为___________ 。
(2)用a、b、c表示的钠单质的质量分数为___________ 。
(3)没有B装置对测定结果有何影响?___________ (填“偏大”“偏小”或“不影响”)。
Ⅱ.现用金属钠和空气制备纯度较高的Na2O2,装置如图所示。

请回答下列问题:
(4)为完成实验应将装置丁接在装置___________ 之间(填“甲乙”或“乙丙”),且装置丁中盛放的试剂是___________ 。
(5)装置丙的作用是___________ 。
(6)为制得更纯的Na2O2,应先___________ ,后___________ 。
(7)点燃酒精灯后,观察到装置乙中的现象为:钠先熔化成闪亮的小球,后剧烈燃烧___________ (请把乙中现象补充完整)
Ⅰ.为测定金属钠样品(表面有Na2O )中钠单质的质量分数,设计了如下实验(反应装置如图所示,U形管中的无水CaCl2用作干燥剂)

①称量A、B装置的总质量
②称取一定质量的钠样品
③将钠样品投入锥形瓶中,迅速塞紧带U形干燥管的橡皮塞有关数据:A、B装置反应前总质量为ag,称取的金属钠样品质量为bg,反应后A、B总质量为cg。
请根据题意回答下列问题:
(1)钠与水反应的化学方程式为
(2)用a、b、c表示的钠单质的质量分数为
(3)没有B装置对测定结果有何影响?
Ⅱ.现用金属钠和空气制备纯度较高的Na2O2,装置如图所示。

请回答下列问题:
(4)为完成实验应将装置丁接在装置
(5)装置丙的作用是
(6)为制得更纯的Na2O2,应先
(7)点燃酒精灯后,观察到装置乙中的现象为:钠先熔化成闪亮的小球,后剧烈燃烧
您最近一年使用:0次
名校
9 . Na2O2是实验室中的常用试剂,工业上可用作氧化剂、防腐剂、除臭剂、杀菌剂、漂白剂等,该物质保存不当时易变质。某化学学习小组成员以实验室中标有“过氧化钠”的试剂为对象进行实验。回答下列问题:
Ⅰ.对该“试剂”的组成进行探究:
实验小组成员取出该标有“过氧化钠”的试剂瓶中的试剂,观察其外部特征:主要为块状、白色,用研钵捣碎块状物,可观察到内部呈淡黄色。
(1)上述淡黄色物质为Na2O2,猜想块状物外层白色物质的组成
猜想1:只有NaOH
猜想2:只有Na2CO3
猜想3:___________
(2)设计实验并得出结论:
可选用试剂:BaCl2溶液、NaCl溶液、Ba(OH)2溶液
Ⅱ.该学习小组成员继续采用下图装置,测定一块质量为m克的上述“试剂”中过氧化钠的质量分数。

(3)可用石灰石和稀盐酸制备CO2,该过程的离子反应方程式为:___________ 。
(4)装置乙的作用是___________ 。
(5)装置丁中液面与装置丙中液面高度相同时,测得量筒中水的体积折算成氧气的质量为a克,则混合物中过氧化钠的质量分数为___________ 。
Ⅰ.对该“试剂”的组成进行探究:
实验小组成员取出该标有“过氧化钠”的试剂瓶中的试剂,观察其外部特征:主要为块状、白色,用研钵捣碎块状物,可观察到内部呈淡黄色。
(1)上述淡黄色物质为Na2O2,猜想块状物外层白色物质的组成
猜想1:只有NaOH
猜想2:只有Na2CO3
猜想3:
(2)设计实验并得出结论:
可选用试剂:BaCl2溶液、NaCl溶液、Ba(OH)2溶液
| 序号 | 实验步骤 | 实验现象 | 结论后解析 |
| 1 | ①取少量上述白色物质,加入到盛有稀盐酸的试管 | “猜想1”不成立 | |
| 2 | ②取少量上述白色物质溶于水,向其中加入过量的 | 产生白色沉淀 | 所涉及的离子方程式: |
| ③过滤②所得混合物,向滤液中滴加几滴酚酞 | 溶液不变红 |
Ⅱ.该学习小组成员继续采用下图装置,测定一块质量为m克的上述“试剂”中过氧化钠的质量分数。

(3)可用石灰石和稀盐酸制备CO2,该过程的离子反应方程式为:
(4)装置乙的作用是
(5)装置丁中液面与装置丙中液面高度相同时,测得量筒中水的体积折算成氧气的质量为a克,则混合物中过氧化钠的质量分数为
您最近一年使用:0次
名校
10 . 某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
I.制备纯碱:先以 和水等为原料,用下图所示装置制取
和水等为原料,用下图所示装置制取 ,然后再将
,然后再将 制备成
制备成 。
。
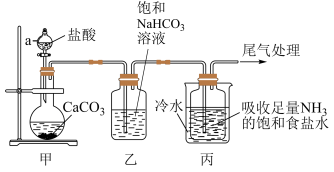
(1)仪器a的名称是___________ ,装置乙的作用是___________ 。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是 。装置丙中可得两种产物,分别是
。装置丙中可得两种产物,分别是 和另一种盐,装置丙中反应的化学方程式为
和另一种盐,装置丙中反应的化学方程式为___________ 。
(3)用装置丙中产生的 制取
制取 时,需要进行的实验操作有过滤、洗涤、
时,需要进行的实验操作有过滤、洗涤、_________ ,最后一步发生反应的化学方程式为___________ 。
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有 ,请选择下列装置设计实验,并完成下表:
,请选择下列装置设计实验,并完成下表:
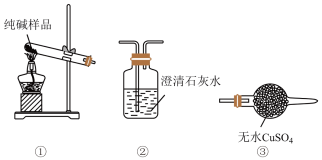
(5)测定该纯碱样品的纯度:称取ag样品,置于小烧杯中,加水溶解,滴加足量 溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为bg。则该纯碱样品的纯度为
溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为bg。则该纯碱样品的纯度为___________ (用含有a、b的式子表示)。
I.制备纯碱:先以
 和水等为原料,用下图所示装置制取
和水等为原料,用下图所示装置制取 ,然后再将
,然后再将 制备成
制备成 。
。
(1)仪器a的名称是
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是
 。装置丙中可得两种产物,分别是
。装置丙中可得两种产物,分别是 和另一种盐,装置丙中反应的化学方程式为
和另一种盐,装置丙中反应的化学方程式为(3)用装置丙中产生的
 制取
制取 时,需要进行的实验操作有过滤、洗涤、
时,需要进行的实验操作有过滤、洗涤、II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有
 ,请选择下列装置设计实验,并完成下表:
,请选择下列装置设计实验,并完成下表:
| 选择的装置连接顺序(填编号) | 实验现象 | 实验结论 |
样品中含 |
(5)测定该纯碱样品的纯度:称取ag样品,置于小烧杯中,加水溶解,滴加足量
 溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为bg。则该纯碱样品的纯度为
溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为bg。则该纯碱样品的纯度为
您最近一年使用:0次



