名校
解题方法
1 . 滴定是一种定量分析的手段,也是一种重要的化学实验操作。
I.酸碱中和滴定是最基本的滴定方法。现用0.1000mol·L-1NaOH标准溶液来测定某盐酸的浓度。有以下实验操作:
①向润洗过的碱式滴定管中加入0.1000mol·L-1的NaOH标准溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”刻度或“0”刻度以下的某刻度,并记录读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液;
⑤用NaOH标准溶液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2~3次。
请回答下列问题:
(1)在使用滴定管前首先要进行的操作是_______ ,滴定管盛装好NaOH溶液后排气泡,图1中排气泡正确的操作是_______ (填序号)。

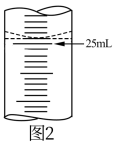
(2)①若甲学生在实验过程中,记录滴定前碱式滴定管内液面读数为4.80mL,滴定后液面如图2,则此时消耗标准溶液的体积为_______ 。
②乙学生做了三组平行实验,滴定并记录V(NaOH)的初、终读数,数据记录如表所示:
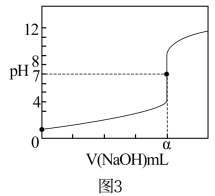
利用手持技术测得滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如图3所示,则a_______ (填“>”、“<”或“=”)20.02。
II.氧化还原滴定实验(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)与酸碱中和滴定类似。测血钙的含量时,进行如下实验:
①将2.00mL血液用蒸馏水稀释后,向其中加入足量草酸铵[(NH4)2C2O4]晶体,反应生成CaC2O4沉淀,过滤后,将沉淀用足量稀硫酸处理得H2C2O4溶液;
②将①得到的H2C2O4溶液装入锥形瓶内,再用1.0×10-4mol·L-1酸性KMnO4溶液滴定,达到终点时用去KMnO4溶液的体积为20.00mL。
(3)用酸性KMnO4溶液滴定H2C2O4的反应的离子方程式为_______ 。
(4)实验中选用的滴定方式合理的是_______ (填字母序号)。(夹持部分略去)
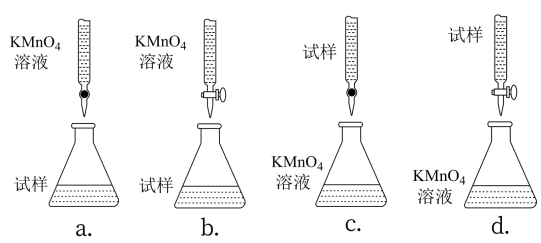
(5)用酸性KMnO4溶液滴定所得H2C2O4溶液,是否需要加入指示剂?_______ (填“是”或“否”),若是,请说明理由;若否请说明判断滴定终点的方法:_______ 。
(6)通过计算可得,该血液中钙的含量为_______ mg·mL-1。
I.酸碱中和滴定是最基本的滴定方法。现用0.1000mol·L-1NaOH标准溶液来测定某盐酸的浓度。有以下实验操作:
①向润洗过的碱式滴定管中加入0.1000mol·L-1的NaOH标准溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”刻度或“0”刻度以下的某刻度,并记录读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入2滴酚酞试液;
⑤用NaOH标准溶液滴定至终点,记下滴定管液面读数;
⑥重复以上滴定操作2~3次。
请回答下列问题:
(1)在使用滴定管前首先要进行的操作是



(2)①若甲学生在实验过程中,记录滴定前碱式滴定管内液面读数为4.80mL,滴定后液面如图2,则此时消耗标准溶液的体积为
②乙学生做了三组平行实验,滴定并记录V(NaOH)的初、终读数,数据记录如表所示:
| 滴定次数 | 1 | 2 | 3 |
| V(HCl)/mL | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.22 |
II.氧化还原滴定实验(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)与酸碱中和滴定类似。测血钙的含量时,进行如下实验:
①将2.00mL血液用蒸馏水稀释后,向其中加入足量草酸铵[(NH4)2C2O4]晶体,反应生成CaC2O4沉淀,过滤后,将沉淀用足量稀硫酸处理得H2C2O4溶液;
②将①得到的H2C2O4溶液装入锥形瓶内,再用1.0×10-4mol·L-1酸性KMnO4溶液滴定,达到终点时用去KMnO4溶液的体积为20.00mL。
(3)用酸性KMnO4溶液滴定H2C2O4的反应的离子方程式为
(4)实验中选用的滴定方式合理的是

(5)用酸性KMnO4溶液滴定所得H2C2O4溶液,是否需要加入指示剂?
(6)通过计算可得,该血液中钙的含量为
您最近一年使用:0次
2022-01-15更新
|
172次组卷
|
2卷引用:内蒙古兴安盟乌兰浩特市第一中学2022-2023学年高二上学期期中考试化学试题



