名校
1 . 亚硝酰氯NOCl常用于合成洗涤剂、触媒及用作中间体,是一种红褐色液体或黄色气体,其熔点-64.5℃,沸点-5.5℃,遇水易水解。某学习小组在实验室用Cl2与NO制备NOCl并测定其纯度,进行如图实验(夹持装置略去)。
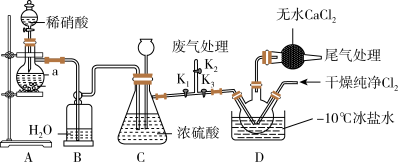
(1)实验室制取Cl2的离子方程式为____ 。
(2)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为____ 。
(3)实验过程中,若学习小组同学用酒精灯大火加热制取NO,对本实验造成的不利影响是____ 。
(4)装置C中长颈漏斗的作用是____ 。
(5)一段时间后,两种气体在D中反应的现象为____ 。
(6)若不用装置D中的干燥管对实验有何影响____ (用化学方程式表示)。
(7)亚硝酰氯NOCl纯度的测定。取D中所得液体100g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,以K2CrO4溶液为指示剂,用cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL(已知Ag2CrO4为砖红色固体)。
①滴定终点的现象:当滴入最后一滴AgNO3标准溶液后,____ 。
②则亚硝酰氯(NOCl)的质量分数为____ 。

(1)实验室制取Cl2的离子方程式为
(2)NOCl分子中各原子均满足8电子稳定结构,则NOCl的电子式为
(3)实验过程中,若学习小组同学用酒精灯大火加热制取NO,对本实验造成的不利影响是
(4)装置C中长颈漏斗的作用是
(5)一段时间后,两种气体在D中反应的现象为
(6)若不用装置D中的干燥管对实验有何影响
(7)亚硝酰氯NOCl纯度的测定。取D中所得液体100g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL样品溶于锥形瓶中,以K2CrO4溶液为指示剂,用cmol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL(已知Ag2CrO4为砖红色固体)。
①滴定终点的现象:当滴入最后一滴AgNO3标准溶液后,
②则亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
2022-04-17更新
|
790次组卷
|
4卷引用:青海省西宁市2022届高三下学期第一次模拟考试 化学试题
青海省西宁市2022届高三下学期第一次模拟考试 化学试题(已下线)秘籍19 综合实验装置分析与实验操作及实验现象描述-备战2022年高考化学抢分秘籍(全国通用)(已下线)化学-2022年高考考前押题密卷(湖北卷)湖南省岳阳市第一中学2023届高三下学期第五次月考化学试题
名校
2 . 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol/L的HCl标准溶液进行中和滴定(用甲基橙作指示剂)。 请回答下列问题:
(1)滴定前,用移液管量取待测NaOH溶液于_____ 中( 填仪器名称),并加入2~3滴指示剂;
(2)盛装标准盐酸的仪器名称为_____ ;
(3)如何判断滴定终点(需写出颜色变化)__________ ;
某学生做了三组平行实验,数据记录如下:
(4)选取下述合理数据,算出待测NaOH溶液的物质的量浓度为___________ ;(保留四位有效数字)
(5)下列哪些操作会使测定结果偏低____________ 。
a.反应容器用蒸馏水洗净后,未用待测液润洗
b.滴定前,平视读数;滴定后,仰视读数
c.滴定前,尖嘴无气泡;滴定后,尖嘴出现气泡
(1)滴定前,用移液管量取待测NaOH溶液于
(2)盛装标准盐酸的仪器名称为
(3)如何判断滴定终点(需写出颜色变化)
某学生做了三组平行实验,数据记录如下:
(4)选取下述合理数据,算出待测NaOH溶液的物质的量浓度为
| 实验序号 | 待测NaOH溶液的体积/ mL | 0.1000mol.L-1HCl溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
a.反应容器用蒸馏水洗净后,未用待测液润洗
b.滴定前,平视读数;滴定后,仰视读数
c.滴定前,尖嘴无气泡;滴定后,尖嘴出现气泡
您最近一年使用:0次
名校
3 . 碘对动植物的生命是极其重要的,海水里的碘化物和碘酸盐参与大多数海生物的新陈代谢。在高级哺乳动物中,碘以碘化氨基酸的形式集中在甲状腺内,缺乏碘会引起甲状腺肿大。
I.现要从工业含碘废液中回收碘单质(废液中含有H2O、油脂、I2、I)。设计如图一所示的实验过程:

(1)为了将含碘废液中的I2完全转化为I—而进入水层,向含碘废液中加入了稍过量的A溶液,则A应该具有___________ 性。
(2)将在三颈烧瓶中反应完全后的溶液经过操作②获得碘单质,操作②包含多步操作,操作名称分别为萃取、_____ 、_____ ,在操作②中必须用到下列所示的部分仪器或装置,这些仪器和装置是________________ (填标号)。

(3)将操作①所得溶液放入图二所示的三颈烧瓶中,并用盐酸调至pH约为2,再缓慢通入适量Cl2,使其在30~40℃反应。写出其中发生反应的离子方程式________________ ;Cl2不能过量,因为过量的Cl2将I2氧化为IO3-,写出该反应的离子方程式__________ 。
II.油脂的不饱和度可通过油脂与碘的加成反应测定,通常称为油脂的碘值。碘值越大,油脂的不饱和程度越高。碘值是指100g油脂所能吸收的I2的克数。称取xg某油脂,加入含ymol I2的韦氏溶液( 韦氏溶液是碘值测定时使用的特殊试剂,含有CH3COOH),充分振荡;过量的I2用cmol/L Na2S2O3标准溶液滴定(淀粉作指示剂),消耗Na2S2O3溶液V mL(滴定反应为:2Na2S2O3+I2=Na2S4O6+2NaI)。回答下列问题:
(1)下列有关滴定的说法不正确的是________ (填标号)。
A.标准Na2S2O3溶液应盛装在碱式滴定管中
B.滴定时眼睛只要注视滴定管中溶液体积的变化
C. 滴定终点时,俯视读数,导致测定结果偏低
D.滴定到溶液由无色变蓝色时应该立即停止滴定
(2)用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是_______________________________________________ 。
(3)该油脂的碘值为_____ g(列式表示)。
I.现要从工业含碘废液中回收碘单质(废液中含有H2O、油脂、I2、I)。设计如图一所示的实验过程:

(1)为了将含碘废液中的I2完全转化为I—而进入水层,向含碘废液中加入了稍过量的A溶液,则A应该具有
(2)将在三颈烧瓶中反应完全后的溶液经过操作②获得碘单质,操作②包含多步操作,操作名称分别为萃取、

(3)将操作①所得溶液放入图二所示的三颈烧瓶中,并用盐酸调至pH约为2,再缓慢通入适量Cl2,使其在30~40℃反应。写出其中发生反应的离子方程式
II.油脂的不饱和度可通过油脂与碘的加成反应测定,通常称为油脂的碘值。碘值越大,油脂的不饱和程度越高。碘值是指100g油脂所能吸收的I2的克数。称取xg某油脂,加入含ymol I2的韦氏溶液( 韦氏溶液是碘值测定时使用的特殊试剂,含有CH3COOH),充分振荡;过量的I2用cmol/L Na2S2O3标准溶液滴定(淀粉作指示剂),消耗Na2S2O3溶液V mL(滴定反应为:2Na2S2O3+I2=Na2S4O6+2NaI)。回答下列问题:
(1)下列有关滴定的说法不正确的是
A.标准Na2S2O3溶液应盛装在碱式滴定管中
B.滴定时眼睛只要注视滴定管中溶液体积的变化
C. 滴定终点时,俯视读数,导致测定结果偏低
D.滴定到溶液由无色变蓝色时应该立即停止滴定
(2)用该测定方法测定的碘值需要用相关的实验校正,因为所测得的碘值总比实际碘值低,原因是
(3)该油脂的碘值为
您最近一年使用:0次
2018-05-04更新
|
364次组卷
|
3卷引用:【全国校级联考】青海省西宁市第四高级中学、第五中学、第十四中学三校2018届高三4月联考理综化学试题
2013·江苏·一模
名校
解题方法
4 . 过氧化钙晶体[CaO2·8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
★过氧化钙晶体的制备
工业上生产CaO2·8H2O的主要流程如下:

(1)用上述方法制取CaO2·8H2O的化学方程式是___________________ 。
(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
①___________________ ;②___________________ 。
★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1H2SO4,用0.0200 mol·L—1KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5 H2O2+6H+ =2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为__________ 。
(4)根据表1数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)________
表1. KMnO4标准溶液滴定数据
★过氧化钙晶体的制备
工业上生产CaO2·8H2O的主要流程如下:

(1)用上述方法制取CaO2·8H2O的化学方程式是
(2)沉淀时常用冰水控制温度在10℃以下和通入过量的NH3,其可能原因分别是
①
★过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol·L-1H2SO4,用0.0200 mol·L—1KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5 H2O2+6H+ =2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为
(4)根据表1数据,计算产品中CaO2·8H2O的质量分数(写出计算过程)
| 滴定次数 | 样品的质量/g | KMnO4溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 0.3000 | 1.02 | 24.04 |
| 2 | 0.3000 | 2.00 | 25.03 |
| 3 | 0.3000 | 0.20 | 23.24 |
表1. KMnO4标准溶液滴定数据
您最近一年使用:0次
解题方法
5 . 无水MgBr2可用作催化剂。实验室采用镁屑与液溴为原料制备无水MgBr2,装置如右图(夹持仪器略去),主要步骤如下:
步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入适量的液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至室温,过滤,将滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MsBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5 MgBr2•3C2H5OC2H5
MgBr2•3C2H5OC2H5
请回答:
(1)仪器A的名称是_______ ,它在实验中的作用是_________ 。
(2)步骤2中,可以将B装置中的溴完全导入三颈瓶中的原因是_______ ;该实验如果将所用的液溴一次性全部加入三颈瓶中,其后果是____________ 。
(3)步骤3中,第一次过滤得到的固体的物质是_______ ;根据步骤3、4,总结三乙醚合溴化镁所具有的物理性质:_________________________ 。
(4)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++Y4-==Mg Y2-
①滴定前润洗滴定管的操作方法是_______________________ 。
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol•L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液25. 50 mL,则测得无水MgBr2产品的纯度是________ (以质量分数表示)。

步骤1 三颈瓶中装入10 g镁屑和150 mL无水乙醚;装置B中加入适量的液溴。
步骤2 缓慢通入干燥的氮气,直至溴完全导入三颈瓶中。
步骤3 反应完毕后恢复至室温,过滤,将滤液转移至另一干燥的烧瓶中,冷却至0℃,析出晶体,再过滤得三乙醚合溴化镁粗品。
步骤4 常温下用苯溶解粗品,冷却至0℃,析出晶体,过滤,洗涤得三乙醚合溴化镁,加热至160℃分解得无水MsBr2产品。
已知:①Mg和Br2反应剧烈放热;MgBr2具有强吸水性
②MgBr2+3C2H5OC2H5
 MgBr2•3C2H5OC2H5
MgBr2•3C2H5OC2H5请回答:
(1)仪器A的名称是
(2)步骤2中,可以将B装置中的溴完全导入三颈瓶中的原因是
(3)步骤3中,第一次过滤得到的固体的物质是
(4)为测定产品的纯度,可用EDTA(简写为Y4-)标准溶液滴定,反应的离子方程式:
Mg2++Y4-==Mg Y2-
①滴定前润洗滴定管的操作方法是
②测定前,先称取0.2500g无水MgBr2产品,溶解后,用0.0500 mol•L-1的EDTA标准溶液滴定至终点,消耗EDTA标准溶液25. 50 mL,则测得无水MgBr2产品的纯度是
您最近一年使用:0次



