名校
1 .  代表阿伏加德罗常数的值,下列叙述正确的是
代表阿伏加德罗常数的值,下列叙述正确的是
 代表阿伏加德罗常数的值,下列叙述正确的是
代表阿伏加德罗常数的值,下列叙述正确的是A.62g白磷( 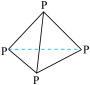 )中含有 )中含有 个非极性键 个非极性键 |
| B.30g乙烷中含有6NA个σ键 |
| C.标况下,22.4L的二氧化碳含2NA个σ键 |
D.0.5 mol雄黄( ,结构为 ,结构为 )含有 )含有 个 个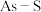 键 键 |
您最近一年使用:0次
名校
2 . 下列说法正确的是
A.Cr原子结构示意图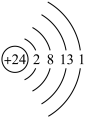 |
B.铍原子最外层的电子云图为 |
C.基态Cu原子的价层电子轨道表示式为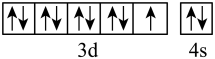 |
D.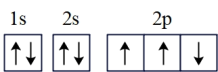 ,该轨道表示式违背了泡利不相容原理 ,该轨道表示式违背了泡利不相容原理 |
您最近一年使用:0次
名校
解题方法
3 . 按要求填空。
(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第2周期部分元素的E1变化趋势如下图所示。___________ 。氮元素能量最高的电子为___________ 轨道上的电子,其轨道呈___________ 形。
(2)B原子价层电子的轨道表达式为___________ 。
(3)Co基态原子核外电子排布式为___________ 。
(1)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第2周期部分元素的E1变化趋势如下图所示。

(2)B原子价层电子的轨道表达式为
(3)Co基态原子核外电子排布式为
您最近一年使用:0次
名校
解题方法
4 . 科学研究发现甲醇(CH3OH)和羰基硫(OCS)是火星上存在的有机物。回答下列问题:
(1)CH3OH中O的杂化类型为___________ ,16 g CH3OH中含有___________ mol σ键。
(2) 常用于酯交换等有机合成,下列各种Li原子电子排布图(轨道表示式)表示的状态中能量最高的为___________ (填字母)。
常用于酯交换等有机合成,下列各种Li原子电子排布图(轨道表示式)表示的状态中能量最高的为___________ (填字母)。
(3) 分子属于
分子属于___________ (填“极性”或“非极性”)分子;OCS分子中C=S,键能:C=O___________ C=S(填“>”或“<”)。
(1)CH3OH中O的杂化类型为
(2)
 常用于酯交换等有机合成,下列各种Li原子电子排布图(轨道表示式)表示的状态中能量最高的为___________ (填字母)。
常用于酯交换等有机合成,下列各种Li原子电子排布图(轨道表示式)表示的状态中能量最高的为___________ (填字母)。A.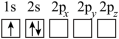 | B.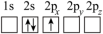 |
C.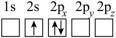 | D. |
 分子属于
分子属于
您最近一年使用:0次
名校
5 . 下列事实能用键能解释的是
| A.稀有气体一般很难发生化学反应 | B.浓硝酸易挥发而浓硫酸难挥发 |
| C.氮气的化学性质比氧气的稳定 | D.常温常压下,溴为液体,碘为固体 |
您最近一年使用:0次
名校
6 . 用价层电子对互斥理论(VSEPR)可以预测许多分子或离子的空间构型,有时也能用来推测键角大小,下列判断正确的是
| A.AB2型分子的键角均为180° | B.BeF2的键角大于SF2的键角 |
| C.BF3的键角为60° | D.PCl3是平面三角形分子 |
您最近一年使用:0次
名校
7 . X、Y、Z、W是元素周期表前四周期中的常见元素,其原子序数依次增大。X元素的一种核素的质量数为12,中子数为6;Y元素是动植物生长不可缺少的、组成蛋白质的重要元素;Z的基态原子核外9个原子轨道上都填充了电子且有2个未成对电子;W是一种常见元素,可以形成3种氧化物,其中一种氧化物是具有磁性的黑色晶体。
(1) 分子中存在的σ键和π键个数之比为
分子中存在的σ键和π键个数之比为___________ 。
(2)X的第一电离能比Y的___________ (填“大”或“小”)。
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液加热会反应会生成可以使品红溶液褪色的物质,写出化学方程式:___________ 。
(4)W的基态原子的价层电子排布式为___________ 。
(5)X、Y的最简单氢化物的VSEPR模型分别为___________ 、___________ 。
(1)
 分子中存在的σ键和π键个数之比为
分子中存在的σ键和π键个数之比为(2)X的第一电离能比Y的
(3)写出X的单质与Z的最高价氧化物对应水化物的浓溶液加热会反应会生成可以使品红溶液褪色的物质,写出化学方程式:
(4)W的基态原子的价层电子排布式为
(5)X、Y的最简单氢化物的VSEPR模型分别为
您最近一年使用:0次
名校
8 . 第三周期元素的单质及其化合物具有重要用途。例如,在熔融状态下,可用金属钠制备金属钾;MgCl2可制备多种镁产品:铝-空气电池具有较高的比能量,在碱性电解液中总反应式为4Al+3O2+4OH-+6H2O=4[Al(OH)4]-,高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氟硅烷(SiHCl3),再经氢气还原得到高纯硅。下列说法正确的是
| A.钠燃烧时火焰呈黄色与电子跃迁有关,焰色反应是化学变化 |
| B.Mg2+基态核外电子排布式为1s22s22p63s2 |
| C.1mol[Al(OH)4]-中含有4molσ键 |
| D.Si-Si键的键能小于Si-O键的键能 |
您最近一年使用:0次
名校
9 . 用 粒子轰击
粒子轰击 可得到一个中子和一种放射性核素
可得到一个中子和一种放射性核素 ,即
,即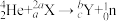 。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是
。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是
 粒子轰击
粒子轰击 可得到一个中子和一种放射性核素
可得到一个中子和一种放射性核素 ,即
,即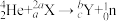 。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是
。已知基态X原子中s能级电子总数是p能级电子总数的4倍。下列说法错误的是| A.b=13 | B.最高价含氧酸的酸性:X<Y |
| C.XF3与YF3中X与Y的杂化方式相同 | D.Y的某种氢化物中含非极性键 |
您最近一年使用:0次
10 . 下列关于原子结构的说法不正确的是
A.电子由3d能级跃迁至4p能级,其光谱为吸收光谱 |
| B.s电子云是在空间各个方向上伸展程度相同的对称形状 |
| C.元素周期表每一周期原子的最外层电子排布均是从ns1过渡到ns2np6 |
| D.日常生活中的焰火、LED灯都与原子核外电子跃迁释放能量有关 |
您最近一年使用:0次



