1 . 氨在人类的生产和生活中有着广泛的应用。某化学兴趣小组为了制取并探究氨气的性质,用下列装置(部分夹持装置已略去)进行实验。 装置,则该反应的化学方程式为
装置,则该反应的化学方程式为___________ 。
(2)B装置中的干燥剂可选用___________ (填名称)。
(3)气体通过C、D装置时,试纸颜色会发生变化的是___________ (填“C”或“D”)装置。
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ ,发生该反应的化学方程式为___________ 。
(5)F装置中倒置漏斗的作用是___________ ,与F有相同作用的装置为___________ (填序号)。
(6)氨的用途很广,如:①用氨处理二氧化氮: ,该反应中氨体现
,该反应中氨体现___________ (填“氧化性”或“还原性”);②工业上用氨气制硝酸,首先将氨气催化氧化,写出氨气催化氧化的化学方程式___________ 。
(7)氨气极易溶于水,会形成喷泉实验,实验装置如图所示。下列可以产生类似现象的组合为___________ 。

 装置,则该反应的化学方程式为
装置,则该反应的化学方程式为(2)B装置中的干燥剂可选用
(3)气体通过C、D装置时,试纸颜色会发生变化的是
(4)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)F装置中倒置漏斗的作用是
|
|
|
| Ⅰ | Ⅱ | Ⅲ |
(6)氨的用途很广,如:①用氨处理二氧化氮:
 ,该反应中氨体现
,该反应中氨体现(7)氨气极易溶于水,会形成喷泉实验,实验装置如图所示。下列可以产生类似现象的组合为

| 圆底烧瓶(干燥气体) | 烧杯及胶头滴管(液体) | |
| A | NO | 水 |
| B |  | 4mol/L NaOH溶液 |
| C |  | 饱和NaCl溶液 |
| D |  | 1mol/L盐酸 |
您最近一年使用:0次
名校
解题方法
2 . 研究化学能与热能、电能的转化具有重要价值。回答下列问题:
(1)下列化学反应过程中的能量变化符合图示的是___________ (填序号)。
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥ 与
与 反应
反应 的反应过程如图所示:
的反应过程如图所示: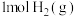 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收___________ kJ能量,生成物中新键形成共放出___________ kJ能量,该反应为___________ (填“吸热”或“放热”)反应。
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是___________ (填“A”或“B”)。
(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:___________ 。
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:___________ 。
(5)若利用反应 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料:___________ ;正极材料:___________ ;电解质溶液:___________ 。
__________________ ___________ 。
(1)下列化学反应过程中的能量变化符合图示的是
①酸碱中和反应 ②碳酸钙分解 ③金属钠与水反应 ④酒精燃烧 ⑤灼热的碳与二氧化碳反应 ⑥
 与
与 反应
反应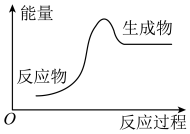
 的反应过程如图所示:
的反应过程如图所示: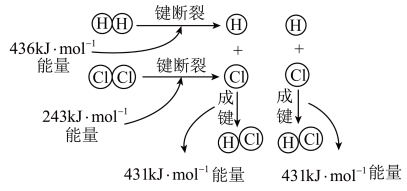
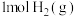 和
和 充分反应,则反应物中旧键断裂共吸收
充分反应,则反应物中旧键断裂共吸收原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(3)现有如下两个反应:A
 ;B.
;B.  ,判断上述两个反应中能设计成原电池的是
,判断上述两个反应中能设计成原电池的是(4)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
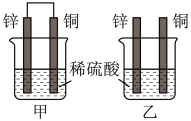
A 甲、乙均为化学能转变为电能的装置 B. 乙中铜片上没有明显变化
C. 甲中铜片质量减少、乙中锌片质量减少 D. 两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
(5)若利用反应
 设计一个原电池,请完善实验装置,负极材料:
设计一个原电池,请完善实验装置,负极材料: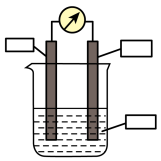
您最近一年使用:0次
3 . Ⅰ.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。___________ ,C的化学式是___________ 。
(4)加入过量A的目的是___________ 。
(5)加入过量B的目的是___________ 。
(6)加热煮沸的目的是___________ 。
(7)操作Ⅰ的名称是___________ 。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是
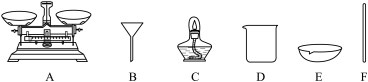

(4)加入过量A的目的是
(5)加入过量B的目的是
(6)加热煮沸的目的是
(7)操作Ⅰ的名称是
您最近一年使用:0次
解题方法
4 . 工业上,常用水蒸气通过炽热的焦炭制得水煤气(主要成分为 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:
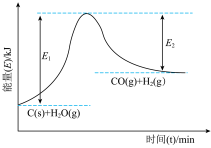
(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是___________。
(3)在体积均为 的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和水蒸气,在不同温度下反应的过程如图所示:
的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和水蒸气,在不同温度下反应的过程如图所示: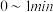 内的平均反应速率
内的平均反应速率
___________
②甲容器中,A点正反应速率___________ B点的逆反应速率(填“ ”“
”“ ”或“
”或“ ”)。
”)。
③反应过程中,两个容器温度:甲___________ 乙(填“ ”“
”“ ”或“
”或“ ”)
”)
 和
和 ),其反应的化学方程式为
),其反应的化学方程式为 ,请回答下列问题:
,请回答下列问题:(1)上述反应的能量变化图像如图所示。下列反应的能量变化与上述反应相同的是___________。
| A.碳酸氢钠与盐酸 | B.氯化铵与  的反应 的反应 |
| C.锌片与稀硫酸的反应 | D.钠与冷水的反应 |
(2)一定条件下,焦炭和水蒸气在体积一定的密闭容器中进行反应,下列有关说法正确的是___________。
A.充入 使容器压强增大,提高反应速率 使容器压强增大,提高反应速率 |
B. ,说明反应达到平衡状态 ,说明反应达到平衡状态 |
| C.容器中焦炭的质量不再变化,说明反应达到平衡状态 |
D.容器中水蒸气与氢气的体积比为 时,说明反应达到平衡状态 时,说明反应达到平衡状态 |
(3)在体积均为
 的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和水蒸气,在不同温度下反应的过程如图所示:
的甲、乙两个恒容密闭容器中,分别加入相同质量的一定量炭粉和水蒸气,在不同温度下反应的过程如图所示: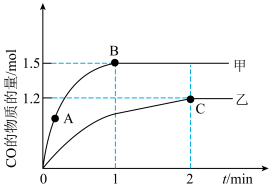
 内的平均反应速率
内的平均反应速率
②甲容器中,A点正反应速率
 ”“
”“ ”或“
”或“ ”)。
”)。③反应过程中,两个容器温度:甲
 ”“
”“ ”或“
”或“ ”)
”)
您最近一年使用:0次
5 . 完成下列问题。
如图所示,某兴趣小组研究铜与浓硫酸的反应。___________ ,这一过程中浓硫酸体现___________ 。
(2)若试管②中盛放品红试液,可以验证的 性质是
性质是___________ 。
(3)若要验证 的还原性,试管②中应盛放
的还原性,试管②中应盛放 ___________ 溶液。
(4)试管③的作用是___________ 发生的离子反应方程式为___________ 。
(5)浓硫酸具有: 脱水性;
脱水性;  酸性;
酸性;  强氧化性;
强氧化性;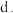 吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加___________ 。
②浓硫酸与铜共热,浓硫酸表现的性质是___________ 。
③浓硫酸与红热木炭反应,浓硫酸表现的性质是___________ 。
④蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是___________ 。
如图所示,某兴趣小组研究铜与浓硫酸的反应。

(2)若试管②中盛放品红试液,可以验证的
 性质是
性质是(3)若要验证
 的还原性,试管②中应盛放
的还原性,试管②中应盛放 (4)试管③的作用是
(5)浓硫酸具有:
 脱水性;
脱水性;  酸性;
酸性;  强氧化性;
强氧化性;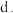 吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加
②浓硫酸与铜共热,浓硫酸表现的性质是
③浓硫酸与红热木炭反应,浓硫酸表现的性质是
④蔗糖中倒入浓硫酸,蔗糖变黑,体积膨胀,且有刺激性气味的气体产生,浓硫酸表现的性质是
您最近一年使用:0次
6 . Ⅰ:某化学兴趣小组为探究 的性质,按如图所示装置进行实验。(已知:
的性质,按如图所示装置进行实验。(已知: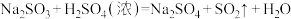 )
)
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是___________ 、___________ 。
(2)反应后,装置B中产生的现象是___________ ,发生反应的离子方程式为___________ 。
(3)装置C中的现象是___________ ,表现了 的
的___________ ,装置D中的现象是___________ ,发生反应的化学方程式为___________ 。
(4)F装置的作用是___________ ,倒扣漏斗的作用是___________ 。
Ⅱ:除了该方法制取 外也可以用铜与浓硫酸制备,用如图所示装置进行有关实验。将Cu片和浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的
外也可以用铜与浓硫酸制备,用如图所示装置进行有关实验。将Cu片和浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的 和Cu剩余。
和Cu剩余。
(5)写出Cu与浓硫酸反应的化学方程式:___________ 。
(6)烧瓶中有一定量的余酸,但未能使Cu完全溶解,你认为原因是___________ 。
(7)下列足量药品能够用来证明反应结束后的烧瓶中确有余酸的是___________(填字母)。
 的性质,按如图所示装置进行实验。(已知:
的性质,按如图所示装置进行实验。(已知: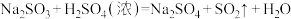 )
)
(1)装置A中盛放浓硫酸和亚硫酸钠的仪器名称分别是
(2)反应后,装置B中产生的现象是
(3)装置C中的现象是
 的
的(4)F装置的作用是
Ⅱ:除了该方法制取
 外也可以用铜与浓硫酸制备,用如图所示装置进行有关实验。将Cu片和浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的
外也可以用铜与浓硫酸制备,用如图所示装置进行有关实验。将Cu片和浓硫酸放入圆底烧瓶中加热,直到反应完毕,最后发现烧瓶中还有一定量的 和Cu剩余。
和Cu剩余。
(5)写出Cu与浓硫酸反应的化学方程式:
(6)烧瓶中有一定量的余酸,但未能使Cu完全溶解,你认为原因是
(7)下列足量药品能够用来证明反应结束后的烧瓶中确有余酸的是___________(填字母)。
| A.Fe粉 | B. 溶液 溶液 | C.Ag | D. 溶液 溶液 |
您最近一年使用:0次
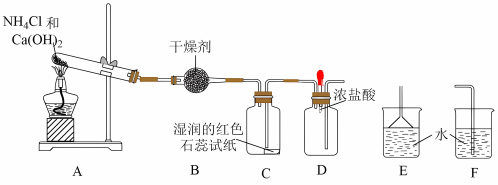
7 . 某实验小组利用以下装置制取氨气并探究氨气的性质:___________ 。
(2)装置B中的干燥剂是___________ (填名称)。
(3)装置C中的现象是___________ 。
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是___________ ,发生反应的化学方程式为___________ 。
(5)验满方法
①把湿润的红色石蕊试纸置于试管口,试纸变___________ 。
②将蘸有浓盐酸的玻璃棒置于试管口,有___________ 产生。
(6)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置___________ (填
“E”或“F”)。
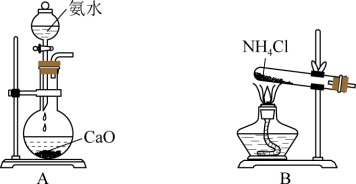
(7)实验室制取氨气,还可采用图中的___________ (填“A”或“B”)。
(2)装置B中的干燥剂是
(3)装置C中的现象是
(4)实验进行一段时间后,挤压装置D中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(5)验满方法
①把湿润的红色石蕊试纸置于试管口,试纸变
②将蘸有浓盐酸的玻璃棒置于试管口,有
(6)为防止过量氨气外逸,需要在上述装置的末端增加一个尾气吸收装置,应选用的装置
“E”或“F”)。
(7)实验室制取氨气,还可采用图中的
您最近一年使用:0次
解题方法
8 . 已知草酸镍晶体( )难溶于水,其在高温下煅烧可制得三氧化二镍。以含镍合金废料(主要成分为镍,含有一定量的铁、铜和硅)为原料生产草酸镍的工艺流程如图:
)难溶于水,其在高温下煅烧可制得三氧化二镍。以含镍合金废料(主要成分为镍,含有一定量的铁、铜和硅)为原料生产草酸镍的工艺流程如图: 、
、 、
、 、
、 、
、 、
、 。
。
②草酸的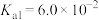 、
、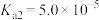 。
。
③氨水的 。
。
回答下列问题:
(1)实验室进行“酸浸”操作时,需要在通风橱中进行,其原因是___________ 。
(2) 的VSEPR模型为
的VSEPR模型为___________ 。
(3)“过滤”后,需要往滤液中加入 溶液制备草酸镍,
溶液制备草酸镍, 溶液呈
溶液呈___________ (填“酸”“碱”或“中”)性,溶液中离子浓度由大到小的顺序是___________ 。
(4)已知常温下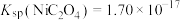 ,当溶液pH=2时,
,当溶液pH=2时, 沉淀完全[
沉淀完全[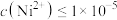
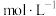 时认为沉淀完全],则此时溶液中草酸的浓度
时认为沉淀完全],则此时溶液中草酸的浓度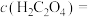
___________ 。
(5)镍钛记忆合金可用于制造飞机和宇宙飞船。已知一种镍钛合金的晶胞结构如图所示,其中Ti原子采用面心立方最密堆积方式,该合金中与Ti原子距离最近且相等的Ni原子个数为___________ ;若该合金的密度为 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是___________ (用含 和
和 的计算式表示,不必化简)pm。
的计算式表示,不必化简)pm。
 )难溶于水,其在高温下煅烧可制得三氧化二镍。以含镍合金废料(主要成分为镍,含有一定量的铁、铜和硅)为原料生产草酸镍的工艺流程如图:
)难溶于水,其在高温下煅烧可制得三氧化二镍。以含镍合金废料(主要成分为镍,含有一定量的铁、铜和硅)为原料生产草酸镍的工艺流程如图: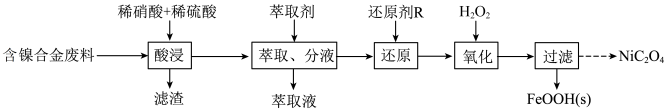
 、
、 、
、 、
、 、
、 、
、 。
。②草酸的
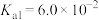 、
、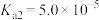 。
。③氨水的
 。
。回答下列问题:
(1)实验室进行“酸浸”操作时,需要在通风橱中进行,其原因是
(2)
 的VSEPR模型为
的VSEPR模型为(3)“过滤”后,需要往滤液中加入
 溶液制备草酸镍,
溶液制备草酸镍, 溶液呈
溶液呈(4)已知常温下
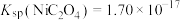 ,当溶液pH=2时,
,当溶液pH=2时, 沉淀完全[
沉淀完全[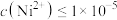
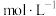 时认为沉淀完全],则此时溶液中草酸的浓度
时认为沉淀完全],则此时溶液中草酸的浓度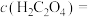
(5)镍钛记忆合金可用于制造飞机和宇宙飞船。已知一种镍钛合金的晶胞结构如图所示,其中Ti原子采用面心立方最密堆积方式,该合金中与Ti原子距离最近且相等的Ni原子个数为
 ,
, 代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是
代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是 和
和 的计算式表示,不必化简)pm。
的计算式表示,不必化简)pm。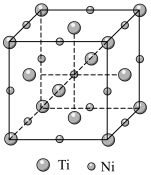
您最近一年使用:0次
7日内更新
|
166次组卷
|
4卷引用:2024届新疆名校联盟高三下学期第二次质量联合监测理科综合试题-高中化学
名校
9 . 某化学课外兴趣小组用如图所示装置进行实验,制备某气体并验证其性质。请回答下列问题:
①装置A中发生反应的化学方程式为___________ 。
②实验中,取一定质量的铜片和一定体积 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
A.有一定量的余酸但未能使铜片完全溶解,你认为原因是___________ 。
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________ (填标号)。
a.铁粉 b. 溶液 c. 银粉 d.
溶液 c. 银粉 d.  溶液
溶液
(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为___________ 。
②设计实验证明装置C中含有 时,所需的试剂有
时,所需的试剂有___________ (填标号)。
a.NaOH溶液 b. 澄清石灰水 c. 品红溶液 d. 酸性 溶液
溶液
(3)反应(1)(2)D中品红溶液褪色,加热试管里已褪色溶液时的现象为:___________ 。
(4)装置D中试管口放置的棉花中浸了一种液体用于吸收尾气,该液体是___________ ,反应的离子方程式为___________ 。

①装置A中发生反应的化学方程式为
②实验中,取一定质量的铜片和一定体积
 的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
的浓硫酸在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。A.有一定量的余酸但未能使铜片完全溶解,你认为原因是
B.下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉 b.
 溶液 c. 银粉 d.
溶液 c. 银粉 d.  溶液
溶液(2)若装置A中分液漏斗盛装浓硫酸,圆底烧瓶盛装木炭。
①装置A中发生反应的化学方程式为
②设计实验证明装置C中含有
 时,所需的试剂有
时,所需的试剂有a.NaOH溶液 b. 澄清石灰水 c. 品红溶液 d. 酸性
 溶液
溶液(3)反应(1)(2)D中品红溶液褪色,加热试管里已褪色溶液时的现象为:
(4)装置D中试管口放置的棉花中浸了一种液体用于吸收尾气,该液体是
您最近一年使用:0次
名校
10 . 可逆反应,在一定条件下达到化学平衡,说明
A. | B.正逆反应停止 |
C. | D. |
您最近一年使用:0次






