1 . 用如图装置可以实现电解K2CrO4溶液制备K2Cr2O7和浓KOH溶液。下列说法不正确的是
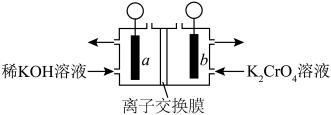
| A.装置中的离子交换膜为阴离子交换膜 |
| B.a室中获得的产品有H2和浓KOH溶液 |
C.b室获得K2Cr2O7的过程中,涉及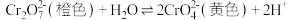 平衡的移动 平衡的移动 |
| D.取少量b室中电解后的溶液,加入乙醇,会看到溶液变绿色 |
您最近一年使用:0次
2 . 制备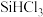 的方程式为
的方程式为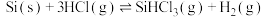 ,同时还有其他副反应发生。当反应体系的压强为
,同时还有其他副反应发生。当反应体系的压强为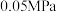 时,分别改变进料比
时,分别改变进料比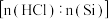 和反应温度,二者对
和反应温度,二者对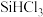 产率影响如图所示。下列说法不正确的是
产率影响如图所示。下列说法不正确的是
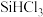 的方程式为
的方程式为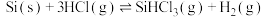 ,同时还有其他副反应发生。当反应体系的压强为
,同时还有其他副反应发生。当反应体系的压强为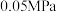 时,分别改变进料比
时,分别改变进料比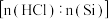 和反应温度,二者对
和反应温度,二者对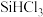 产率影响如图所示。下列说法不正确的是
产率影响如图所示。下列说法不正确的是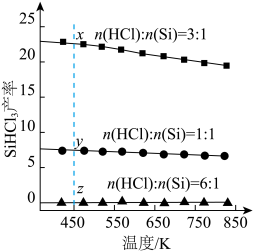
A.增加压强有利于提高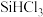 的产率 的产率 |
B.制备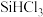 的反应为放热反应 的反应为放热反应 |
C.增加 的用量, 的用量,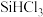 的产率一定会增加 的产率一定会增加 |
D.温度为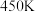 ,平衡常数: ,平衡常数: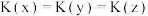 |
您最近一年使用:0次
3 .  与醛、酮反应是制备醇的重要途径。
与醛、酮反应是制备醇的重要途径。 的一种制备方法如图:
的一种制备方法如图:
 与醛、酮反应是制备醇的重要途径。
与醛、酮反应是制备醇的重要途径。 的一种制备方法如图:
的一种制备方法如图:
A. 发生了加成反应 发生了加成反应 |
B. 分子与 分子与 分子中均含有手性碳原子 分子中均含有手性碳原子 |
C. 易溶于水是因为 易溶于水是因为 与水形成分子间氢键 与水形成分子间氢键 |
D.以 和水为原料也可制得 和水为原料也可制得 |
您最近一年使用:0次
名校
解题方法
4 . 高熵合金是指由多种元素(如 等)形成的合金,因其独特的元素组成、微观结构和性能,被认为是极具应用潜力的新型结构材料。
等)形成的合金,因其独特的元素组成、微观结构和性能,被认为是极具应用潜力的新型结构材料。
(1) 是目前采用最多的高熵合金元素组合。
是目前采用最多的高熵合金元素组合。
① 元素与同周期相邻的元素比较,第一电离能由大到小的顺序是
元素与同周期相邻的元素比较,第一电离能由大到小的顺序是_______ (用元素符号表示)。
②基态 原子的价层电子的轨道表示式为
原子的价层电子的轨道表示式为_______ 。
③ 元素位于元素周期表的
元素位于元素周期表的_______ 区。
(2)研究人员发现,在离子液体中可制备均一粒径分布的高熵合金纳米颗粒。离子液体是在室温和接近室温时呈液态的盐类物质,一般由有机阳离子和无机阴离子组成。一种离子液体的结构如图所示。 的空间结构为
的空间结构为________ 。
②研究发现通过改变阳离子侧链可调控离子化合物的熔点。 两种离子液体的结构如图所示。熔点
两种离子液体的结构如图所示。熔点 的原因是
的原因是_______ 。 元素形成的高熵合金,其晶胞结构如图所示,晶胞棱边夹角均为
元素形成的高熵合金,其晶胞结构如图所示,晶胞棱边夹角均为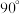 。
。 原子与邻近的
原子与邻近的 原子构成的空间结构为
原子构成的空间结构为_______
②已知阿伏伽德罗常数的值为 ,该晶体的密度为
,该晶体的密度为_______  (列出计算式)。
(列出计算式)。
 等)形成的合金,因其独特的元素组成、微观结构和性能,被认为是极具应用潜力的新型结构材料。
等)形成的合金,因其独特的元素组成、微观结构和性能,被认为是极具应用潜力的新型结构材料。(1)
 是目前采用最多的高熵合金元素组合。
是目前采用最多的高熵合金元素组合。①
 元素与同周期相邻的元素比较,第一电离能由大到小的顺序是
元素与同周期相邻的元素比较,第一电离能由大到小的顺序是②基态
 原子的价层电子的轨道表示式为
原子的价层电子的轨道表示式为③
 元素位于元素周期表的
元素位于元素周期表的(2)研究人员发现,在离子液体中可制备均一粒径分布的高熵合金纳米颗粒。离子液体是在室温和接近室温时呈液态的盐类物质,一般由有机阳离子和无机阴离子组成。一种离子液体的结构如图所示。

 的空间结构为
的空间结构为②研究发现通过改变阳离子侧链可调控离子化合物的熔点。
 两种离子液体的结构如图所示。熔点
两种离子液体的结构如图所示。熔点 的原因是
的原因是
 元素形成的高熵合金,其晶胞结构如图所示,晶胞棱边夹角均为
元素形成的高熵合金,其晶胞结构如图所示,晶胞棱边夹角均为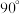 。
。
 原子与邻近的
原子与邻近的 原子构成的空间结构为
原子构成的空间结构为②已知阿伏伽德罗常数的值为
 ,该晶体的密度为
,该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
今日更新
|
158次组卷
|
2卷引用:2024届北京市顺义区高三下学期二模化学试卷
5 . 下列物质性质的比较,与键的极性或分子的极性无关 的是
A.酸性: | B.硬度:金刚石 晶体硅 晶体硅 |
C.硫磺溶解度: 中 中 水中 水中 | D.沸点:环氧乙烷( ) ) |
您最近一年使用:0次
6 . 铁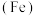 、钴
、钴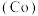 、镍
、镍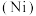 是第四周期第Ⅷ族的元素,称为铁系元素,相关化合物在科研及生产生活中应用广泛。
是第四周期第Ⅷ族的元素,称为铁系元素,相关化合物在科研及生产生活中应用广泛。
I.邻二氮菲 与
与 生成稳定的橙红色邻二氮菲亚铁离子
生成稳定的橙红色邻二氮菲亚铁离子 ,可用于
,可用于 的测定,邻二氮菲的结构简式如图所示。
的测定,邻二氮菲的结构简式如图所示。 中,存在的化学键有
中,存在的化学键有___________ 。
a.配位键 b.离子键 c. 键 d.氢键
键 d.氢键
②用邻二氮菲测定 浓度时应控制
浓度时应控制 为
为 的适宜范围,请解释原因:
的适宜范围,请解释原因:___________ 。
③补铁剂中 易变质,请从结构角度解释其原因
易变质,请从结构角度解释其原因___________ 。
④ 检验补铁剂是否变质,
检验补铁剂是否变质, 中所有原子均满足最外层8电子结构,写出
中所有原子均满足最外层8电子结构,写出 的电子式
的电子式___________ 。
II. 能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如图:
能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如图: 元素在周期表中属于
元素在周期表中属于___________ 区(填“ ”“
”“ ”“
”“ ”或“
”或“ ”)。
”)。
② 元素的第一电离能由大到小的顺序为
元素的第一电离能由大到小的顺序为___________ 。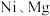 和C三种元素的晶体具有超导性,该晶体的晶胞结构如图所示:
和C三种元素的晶体具有超导性,该晶体的晶胞结构如图所示: 原子最近的
原子最近的 原子有
原子有___________ 个。
②已知该晶体的边长为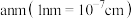 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为___________  。
。
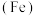 、钴
、钴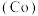 、镍
、镍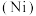 是第四周期第Ⅷ族的元素,称为铁系元素,相关化合物在科研及生产生活中应用广泛。
是第四周期第Ⅷ族的元素,称为铁系元素,相关化合物在科研及生产生活中应用广泛。I.邻二氮菲
 与
与 生成稳定的橙红色邻二氮菲亚铁离子
生成稳定的橙红色邻二氮菲亚铁离子 ,可用于
,可用于 的测定,邻二氮菲的结构简式如图所示。
的测定,邻二氮菲的结构简式如图所示。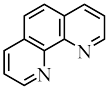
 中,存在的化学键有
中,存在的化学键有a.配位键 b.离子键 c.
 键 d.氢键
键 d.氢键②用邻二氮菲测定
 浓度时应控制
浓度时应控制 为
为 的适宜范围,请解释原因:
的适宜范围,请解释原因:③补铁剂中
 易变质,请从结构角度解释其原因
易变质,请从结构角度解释其原因④
 检验补铁剂是否变质,
检验补铁剂是否变质, 中所有原子均满足最外层8电子结构,写出
中所有原子均满足最外层8电子结构,写出 的电子式
的电子式II.
 能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如图:
能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如图:
 元素在周期表中属于
元素在周期表中属于 ”“
”“ ”“
”“ ”或“
”或“ ”)。
”)。②
 元素的第一电离能由大到小的顺序为
元素的第一电离能由大到小的顺序为③对羟基苯甲醛(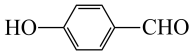 )的沸点为
)的沸点为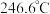 ,而水杨醛(
,而水杨醛(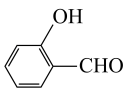 )的沸点为
)的沸点为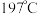 ,请从结构角度解释二者沸点差异的原因
,请从结构角度解释二者沸点差异的原因
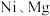 和C三种元素的晶体具有超导性,该晶体的晶胞结构如图所示:
和C三种元素的晶体具有超导性,该晶体的晶胞结构如图所示:
 原子最近的
原子最近的 原子有
原子有②已知该晶体的边长为
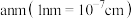 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为 。
。
您最近一年使用:0次
7 . 高分子 的合成方法如图:
的合成方法如图:
 的合成方法如图:
的合成方法如图:
A.高分子 可降解为小分子 可降解为小分子 |
| B.酪氨酸到环二肽的过程中,可能有聚合物生成 |
| C.环二肽可使酸性高锰酸钾溶液褪色,证明其分子中含有羟基 |
| D.以上合成路线中的4种有机物,都既能与酸反应也能与碱反应 |
您最近一年使用:0次
8 . 某种新型储氢材料的晶胞如图,八面体中心为金属离子铁,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性
配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性 )
)
 配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性
配体;四面体中心为硼原子,顶点均为氢原子。下列说法正确的是(已知:元素电负性 )
)
A.该储氢材料的化学式为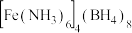 |
B. 金属离子中的未成对电子数为 金属离子中的未成对电子数为 |
| C.晶胞中金属离子的配位数是8 |
| D.基态硼原子的核外电子有5种空间运动状态 |
您最近一年使用:0次
9 . 碳原子的成键特点是有机化合物种类繁多的根本原因。常用球和棍表示有机化合物中碳原子相互结合的方式。例如, 中碳原子的结合方式可用
中碳原子的结合方式可用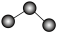 表示。下图显示的是几种烃分子中碳原子相互结合的方式。
表示。下图显示的是几种烃分子中碳原子相互结合的方式。
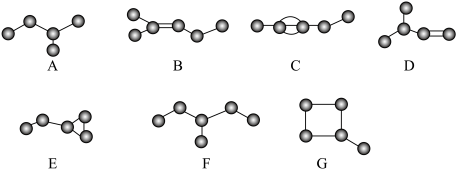
(2)写出烃A的结构简式:
(3)写出烃B的分子式:
(4)上述物质中,与D互为同分异构体的是
(5)用系统命名法,对烃F进行命名:
(6)写出A的另外两种同分异构体的结构简式
(7)写出乙烷一氯取代的化学方程式
您最近一年使用:0次
名校
解题方法
10 . 过渡金属钛(Ti)性能优越,是继铁、铝之后应用广泛的“第三金属”。
(1)钛元素位于周期表的___________ 区;基态 原子核外电子占据的轨道数为
原子核外电子占据的轨道数为___________ 个。
(2)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示。___________ (填字母)。
a.含有手性碳原子
b.2号氧提供孤电子对与钛离子形成配位键
c. 号原子不在同一平面上
号原子不在同一平面上
d.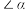 大于
大于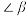
(3)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛矿的晶胞结构如图所示。 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的边长为
,则该晶胞的边长为___________  (用含
(用含 、
、 的式子表示)。
的式子表示)。
(1)钛元素位于周期表的
 原子核外电子占据的轨道数为
原子核外电子占据的轨道数为(2)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示。

a.含有手性碳原子
b.2号氧提供孤电子对与钛离子形成配位键
c.
 号原子不在同一平面上
号原子不在同一平面上 d.
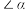 大于
大于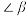
(3)嫦娥三号卫星上的PIC元件(热敏电阻)的主要成分——钡钛矿的晶胞结构如图所示。

 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶胞的边长为
,则该晶胞的边长为 (用含
(用含 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次



