名校
解题方法
1 . 下列叙述不正确的是
| A.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得有机物有6种 |
| B.分子式为C4H8Cl2的有机物只含一个甲基的结构有共有8种(不考虑立体异构) |
| C.含有5个碳原子的某饱和链烃,其一氯取代物可能有3种 |
D.菲的结构简式为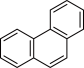 ,其一硝基取代物有5种 ,其一硝基取代物有5种 |
您最近一年使用:0次
名校
2 . 近日,科学家们开发了一类水溶性有机储能小分子(M),并提出在电池充放电过程中实现电化学碳捕获一体化,其反应装置与原理如图所示。
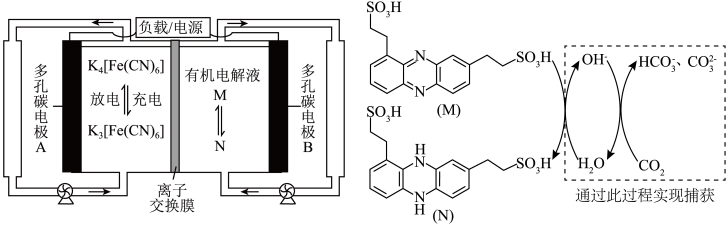
| A.放电时,A电极为负极 |
B.充电时电极B发生的反应为: |
| C.该电池应采用阴离子交换膜 |
D.充电时,外电路通过2mole-,理论上该电池最多能够捕获标况下 |
您最近一年使用:0次
3 . 利用CO2合成甲醇(CH3OH)是实现碳中和的措施之一,其反应方程式为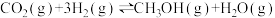 。回答下列问题:
。回答下列问题:
(1)CO2合成甲醇的能量变化如图所示。_______ 反应(填“放热”或“吸热”),反应物的化学键断裂所吸收的总能量_______ 生成物的化学键形成所释放的总能量(填“大于”或“小于”)。
(2)向2L恒容密闭容器中加入4molCO2、10molH2,恒温下发生反应,测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。_______ 逆反应速率(填“>”、“<”或“=”)。
②0~9min内,用H2表示的平均反应速率v(H2)=_______ mol·L-1·min-1。
③下列能说明反应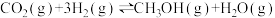 达到平衡状态的是
达到平衡状态的是_______ (填标号)。
A.混合气体的密度保持不变 B.3v正(CH3OH)=v逆(H2)
C.c(CH3OH)=c(H2O) D.2molC=O键断裂的同时生成3molH-H键
(3)以甲醇作燃料的燃料电池如图所示。_______ (填“甲醇”或“空气”);正极的电极反应式为_______ 。
②若有1molCO2生成,理论上通过质子交换膜的H+的物质的量为_______ 。
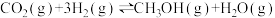 。回答下列问题:
。回答下列问题:(1)CO2合成甲醇的能量变化如图所示。

(2)向2L恒容密闭容器中加入4molCO2、10molH2,恒温下发生反应,测得CO2(g)和CH3OH(g)的物质的量随时间变化如图所示。

②0~9min内,用H2表示的平均反应速率v(H2)=
③下列能说明反应
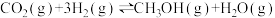 达到平衡状态的是
达到平衡状态的是A.混合气体的密度保持不变 B.3v正(CH3OH)=v逆(H2)
C.c(CH3OH)=c(H2O) D.2molC=O键断裂的同时生成3molH-H键
(3)以甲醇作燃料的燃料电池如图所示。
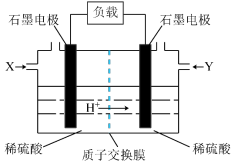
②若有1molCO2生成,理论上通过质子交换膜的H+的物质的量为
您最近一年使用:0次
4 . 下列有关说法正确的是
| A.S与H2、O2、Fe反应过程中S表现氧化性 |
| B.硫、碳在空气中完全燃烧产物分别为SO3、CO2 |
| C.液氨汽化时吸收大量热,可用作制冷剂 |
| D.SO2通入紫色石蕊试液,溶液先变红后褪色,体现了SO2酸性氧化物的性质和漂白性 |
您最近一年使用:0次
名校
解题方法
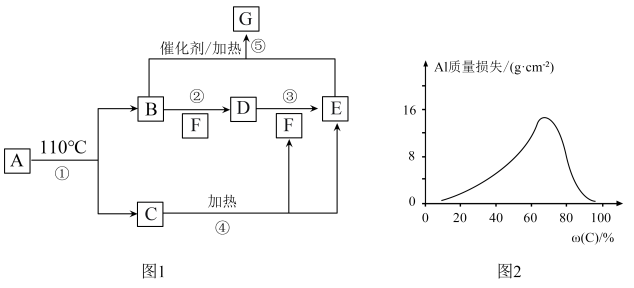
5 . A~G的转化关系如图1所示(部分产物略去),其中E为红棕色气体,G为单质。常温下,将Al片浸在不同质量分数的C溶液中,经过相同时间的腐蚀后,Al片的质量损失情况如图2所示。
(1)A的化学式为_______ 。
(2)实验室中常用_______ 检验B,现象是_______ 。
(3)反应④、⑤的化学方程式依次为_______ 、_______ 。
(4)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为_______ 。
(5)足量Al与一定浓度的C反应,得到H溶液和D、E的混合物,这些混合物与1.68 LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成C.若向所得H溶液中加入5 mol/LNaOH溶液至Al3+恰好完全沉淀,则消耗NaOH溶液的体积是_______ mL。
(1)A的化学式为
(2)实验室中常用
(3)反应④、⑤的化学方程式依次为
(4)图2中Al质量损失随C溶液质量分数的变化先增大后减小,减小的原因为
(5)足量Al与一定浓度的C反应,得到H溶液和D、E的混合物,这些混合物与1.68 LO2(标准状况)混合后通入水中,所有气体恰好完全被水吸收生成C.若向所得H溶液中加入5 mol/LNaOH溶液至Al3+恰好完全沉淀,则消耗NaOH溶液的体积是
您最近一年使用:0次
名校
解题方法
6 . I.某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
[实验原理]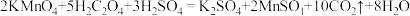
[实验内容及记录]
(1)请完成此实验设计,其中:
_______ ,
_______ 。
(2)实验①、②探究的是_______ 对化学反应速率的影响,根据上表中的实验数据,可以得到的结论是_______ 。
(3)探究温度对化学反应速率的影响,应选择实验_______ (填实验编号)。
(4)利用实验①中的数据,计算用 表示的化学反应速率为
表示的化学反应速率为_______ 。
Ⅱ.某小组同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像 那样还原
那样还原 呢?他们设计实验制取氨气并探究上述问题:
呢?他们设计实验制取氨气并探究上述问题:
①制取氨气
(5)实验室除可用氯化铵和熟石灰制备氨气外,还有多种快速制氨气的方法,写出实验室用生石灰和浓氨水取氨气的化学方程式_______ 。
(6)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的?_______ (填“能”或“否”),理由是_______ 。
②该小组中某同学设计了如下实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:_______ 。
(8)利用改进后的装置进行实验,观察到 变为红色物质,无水
变为红色物质,无水 变蓝色,同时生成一种无污染的气体。写出氨气与
变蓝色,同时生成一种无污染的气体。写出氨气与 反应的化学方程式
反应的化学方程式_______ 。
[实验原理]
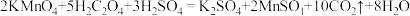
[实验内容及记录]
实验编号 | ① | ② | ③ | |
实验温度/ | 25 | 25 | 50 | |
试管中所加试剂及其用量/ |
| 3.0 | 2.0 | 2.0 |
|
| 3.0 |
| |
| 2.0 | 2.0 | 2.0 | |
| 3.0 | 3.0 | 3.0 | |
溶液褪至无色所需时间/ | 1.5 | 2.7 | 1.0 | |
(1)请完成此实验设计,其中:


(2)实验①、②探究的是
(3)探究温度对化学反应速率的影响,应选择实验
(4)利用实验①中的数据,计算用
 表示的化学反应速率为
表示的化学反应速率为Ⅱ.某小组同学在学习了氨的性质后讨论:运用类比的思想,既然氨气具有还原性,能否像
 那样还原
那样还原 呢?他们设计实验制取氨气并探究上述问题:
呢?他们设计实验制取氨气并探究上述问题:①制取氨气
(5)实验室除可用氯化铵和熟石灰制备氨气外,还有多种快速制氨气的方法,写出实验室用生石灰和浓氨水取氨气的化学方程式
(6)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为他能否达到目的?
②该小组中某同学设计了如下实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:
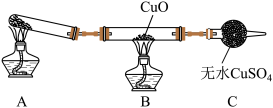
(8)利用改进后的装置进行实验,观察到
 变为红色物质,无水
变为红色物质,无水 变蓝色,同时生成一种无污染的气体。写出氨气与
变蓝色,同时生成一种无污染的气体。写出氨气与 反应的化学方程式
反应的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 在一定容积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度t的关系如表:
,其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为
_______ 。
(2)某温度下,各物质的平衡浓度符合关系式: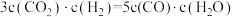 ,试判断此时的温度为
,试判断此时的温度为_______ 。
(3)若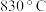 时,向容器中充入
时,向容器中充入 、
、 ,反应达到平衡后,其化学平衡常数K
,反应达到平衡后,其化学平衡常数K_______ 1.0(填“大于”“小于”或“等于”)。
(4)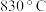 时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡
时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡_______ 移动(填“向正反应方向”“向逆反应方向”或“不”)。
(5)若 时,在某时刻反应体系中
时,在某时刻反应体系中 的浓度分别为
的浓度分别为 ,则此时上述反应
,则此时上述反应_______ (填“向正反应方向进行”“向逆反应方向进行”或“处于平衡状态”)。
(6)甲醇( )燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为
)燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为_______ ;碱性甲醇燃料电池中,负极的电极反应式为_______ 。
 ,其化学平衡常数K和温度t的关系如表:
,其化学平衡常数K和温度t的关系如表:t/ | 700 | 800 | 830 | 1000 | 12000 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为

(2)某温度下,各物质的平衡浓度符合关系式:
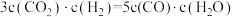 ,试判断此时的温度为
,试判断此时的温度为(3)若
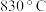 时,向容器中充入
时,向容器中充入 、
、 ,反应达到平衡后,其化学平衡常数K
,反应达到平衡后,其化学平衡常数K(4)
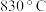 时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡
时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡(5)若
 时,在某时刻反应体系中
时,在某时刻反应体系中 的浓度分别为
的浓度分别为 ,则此时上述反应
,则此时上述反应(6)甲醇(
 )燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为
)燃料电池具有很多优点,引起了人们的研究兴趣,现有以下三种甲醇燃料电池:碱性甲醇燃料电池、酸性甲醇燃料电池、熔融碳酸盐甲醇燃料电池,熔融碳酸盐甲醇燃料电池中正极电极反应式为
您最近一年使用:0次
名校
解题方法
8 . 肼( )是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。 ,放出
,放出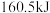 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为_______ ,消耗 液态肼放出的热量为
液态肼放出的热量为_______ 。
(2)已知: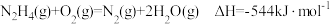 ,键能数据如下表:
,键能数据如下表:
则氮氮三键的键能为_______ ;若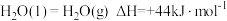 ,则
,则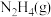 的燃烧热为
的燃烧热为_______ 。
(3)已知: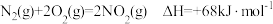 ,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为_______ 。
 )是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
 ,放出
,放出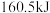 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为 液态肼放出的热量为
液态肼放出的热量为(2)已知:
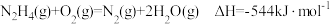 ,键能数据如下表:
,键能数据如下表:化学键 |
|
|
|
|
键能/( | 193 | 391 | 497 | 463 |
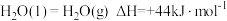 ,则
,则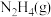 的燃烧热为
的燃烧热为(3)已知:
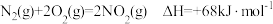 ,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
您最近一年使用:0次
9 . 我国力争2030年前实现碳达峰,2060年前实现碳中和。 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚(
加氢可转化为二甲醚( ),反应原理为
),反应原理为 。该反应的能量变化如图所示。
。该反应的能量变化如图所示。
(1)该反应为_______ (填“放热”或“吸热”)反应。
(2)在固定体积的绝热密闭容器中发生该反应,能说明该反应达到平衡状态的是_______ (填字母)。
a. 的含量保持不变 c.容器内温度不变
的含量保持不变 c.容器内温度不变
b.混合气体的密度不变 d.混合气体的平均相对分子质量不变
e.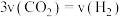
(3)恒温条件下,在体积为 密闭容器中充入
密闭容器中充入 和
和 ,测得
,测得 、
、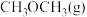 的物质的量随时间变化如图甲所示。
的物质的量随时间变化如图甲所示。
①反应到达 时,
时,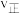
_______  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
②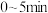 内,
内,
_______ 。
③反应达到平衡状态时,容器内的压强与起始压强之比为_______ 。
④“二甲醚( )酸性燃料电池”的工作原理示意图如图乙所示。
)酸性燃料电池”的工作原理示意图如图乙所示。
X电极为_______ (填“正”或“负”)极;X电极的电极反应式为_______ ;Y电极的电极反应式为_______ 。
 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚(
加氢可转化为二甲醚( ),反应原理为
),反应原理为 。该反应的能量变化如图所示。
。该反应的能量变化如图所示。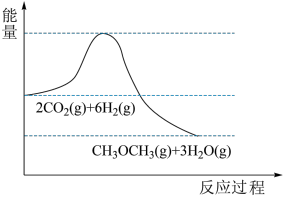
(1)该反应为
(2)在固定体积的绝热密闭容器中发生该反应,能说明该反应达到平衡状态的是
a.
 的含量保持不变 c.容器内温度不变
的含量保持不变 c.容器内温度不变b.混合气体的密度不变 d.混合气体的平均相对分子质量不变
e.
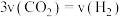
(3)恒温条件下,在体积为
 密闭容器中充入
密闭容器中充入 和
和 ,测得
,测得 、
、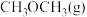 的物质的量随时间变化如图甲所示。
的物质的量随时间变化如图甲所示。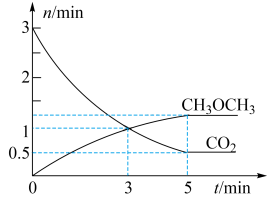
①反应到达
 时,
时,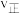
 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。②
 内,
内,
③反应达到平衡状态时,容器内的压强与起始压强之比为
④“二甲醚(
 )酸性燃料电池”的工作原理示意图如图乙所示。
)酸性燃料电池”的工作原理示意图如图乙所示。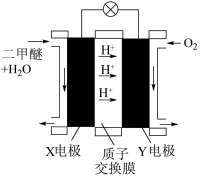
X电极为
您最近一年使用:0次
名校
10 . 在一定条件下,将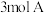 和
和 投入容积为
投入容积为 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: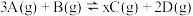 。
。 末测得此时容器中C和D的浓度为
末测得此时容器中C和D的浓度为 和
和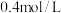 。下列叙述正确的是
。下列叙述正确的是
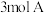 和
和 投入容积为
投入容积为 的密闭容器中,发生如下反应:
的密闭容器中,发生如下反应: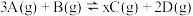 。
。 末测得此时容器中C和D的浓度为
末测得此时容器中C和D的浓度为 和
和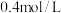 。下列叙述正确的是
。下列叙述正确的是A. |
B. 时,B的浓度为 时,B的浓度为 |
C. 内B的反应速率为 内B的反应速率为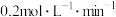 |
D.此时A的转化率为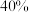 |
您最近一年使用:0次




 溶液
溶液


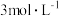 稀
稀 溶液
溶液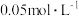





 )
)

