A. 能溶于水,可用于制备 能溶于水,可用于制备 | B. 受热易分解,可用来制造抗酸药物 受热易分解,可用来制造抗酸药物 |
C.浓硫酸具有脱水性,可用于干燥 | D.铁粉能与 反应,可用作食品保存的脱氧剂 反应,可用作食品保存的脱氧剂 |
| 序号 | 实验现象 | 解释和结论 |
| ① | 钠浮在水面上 | 钠的密度比水小 |
| ② | 钠熔成小球 | 钠与水反应放热且钠的熔点低 |
| ③ | 钠四处游动,嘶嘶作响 | 产生了气体 |
| ④ | 向反应后的溶液中滴加酚酞,溶液变红 | 生成了碱性物质 |
| A.①②③ | B.①②③④ | C.①③④ | D.②③④ |
| 选项 | 固体X | 液体Y | 检测方法 |
| A | CaO | 浓氨水 | 蘸有浓盐酸的玻璃棒 |
| B | Cu | 浓硫酸 | 干燥的红色石蕊试纸 |
| C | Na2O2 | 水 | 带火星的木条 |
| D | Na2CO3 | 稀硫酸 | 滴有澄清石灰水的玻璃片 |
| A.A | B.B | C.C | D.D |
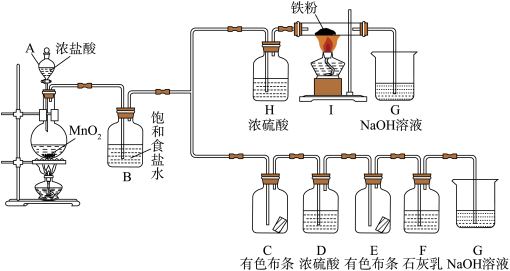
(1)实验室制备氯气的反应的化学方程式
(2)B中饱和食盐水的作用是
(3)广口瓶C、E中,有色布条褪色的是
(4)装置F可用于制漂白粉,漂白粉的有效成分是_____。
A. | B. | C. | D. 和 和 |
 中反应的离子方程式
中反应的离子方程式(6)写出装置Ⅰ中反应的化学方程式
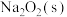 是一种重要的化学原料,有着重要的用途,可与
是一种重要的化学原料,有着重要的用途,可与 、
、 、
、 、
、 等多种物质反应。回答下列问题:
等多种物质反应。回答下列问题:(1)将
 、
、 、
、 放入一个真空密闭容器中,在150℃下用电火花不断引燃反应,恰好完全反应,生成物之一为
放入一个真空密闭容器中,在150℃下用电火花不断引燃反应,恰好完全反应,生成物之一为 ,压强为零,则
,压强为零,则 、
、 、
、 的物质的量之比为
的物质的量之比为(2)
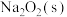 与
与 之间也能进行反应,某科研小组对其反应产物进行了探究分析。
之间也能进行反应,某科研小组对其反应产物进行了探究分析。第1步:用如图1所示装置制取
 ,用98.3%浓硫酸吸收(
,用98.3%浓硫酸吸收( 可溶于浓硫酸,加热后又会逸出),得到无色吸收液。
可溶于浓硫酸,加热后又会逸出),得到无色吸收液。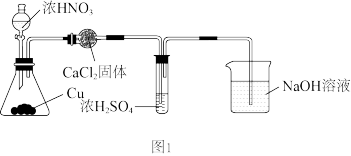
第2步:用如图2所示装置加热浓硫酸吸收液,使
 挥发,通入盛有
挥发,通入盛有 的试管中,至固体颜色不变后,再通入
的试管中,至固体颜色不变后,再通入 ,气体2min。
,气体2min。
第3步:称取图2中反应后的固体0.5g,加水溶解,配制100mL待测溶液。
①
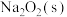 与
与 可能发生反应的化学方程式为
可能发生反应的化学方程式为 、
、②上述“第3步”中配制100mL待测溶液,需要的玻璃仪器有烧杯、玻璃棒、
③图1、图2中的NaOH溶液用于尾气处理,则反应中氧化产物与还原产物的物质的量之比为
(3)某科研兴趣小组运用数字化实验对
 、
、 的反应过程进行探究(如图3所示)。
的反应过程进行探究(如图3所示)。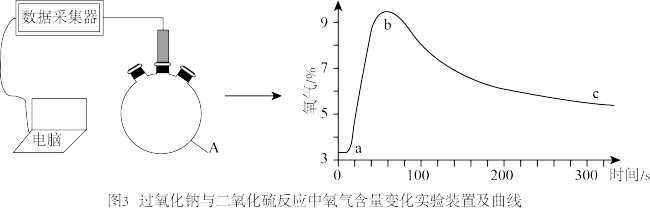
步骤如下:
Ⅰ.将计算机、数据采集器、氧气传感器依次相连。
Ⅱ.用无水
 与浓
与浓 (70%)反应制取并用仪器A收集
(70%)反应制取并用仪器A收集 气体。
气体。Ⅲ.将氧气传感器塞入仪器A中间接口,进行数据采集,用药匙取少量
 从仪器A右端加入,迅速塞紧瓶塞。
从仪器A右端加入,迅速塞紧瓶塞。①仪器A的名称为
②ab段氧气的含量迅速升高,对应的化学方程式为
③bc段氧气的含量慢慢降低,可能发生反应的化学方程式为
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是
(1)
 属于
属于(2)将包有少量
 固体的棉花放在石棉网上,用滴管向棉花上滴几滴水,棉花立刻燃烧起来。由该实验你能得出的结论是
固体的棉花放在石棉网上,用滴管向棉花上滴几滴水,棉花立刻燃烧起来。由该实验你能得出的结论是(3)在潜水艇和消防员的呼吸面具中,
 所发生反应的化学方程式为
所发生反应的化学方程式为 的作用是
的作用是(4)某潜水艇上有50人,如果每人每分钟消耗的O2在标准状况下体积为0.80L(标准状况下O2的密度为1.429g/L),假设所需要的O2全部由
 来提供,则该潜水艇一天所需要的
来提供,则该潜水艇一天所需要的 的质量是
的质量是 在生产和生活中有着广泛用途,某化学小组在实验室制备
在生产和生活中有着广泛用途,某化学小组在实验室制备 并探究其性质。请回答:
并探究其性质。请回答:(一)
 的制备,分步骤Ⅰ、Ⅱ两步进行。
的制备,分步骤Ⅰ、Ⅱ两步进行。步骤Ⅰ.先利用下图所示装置制备

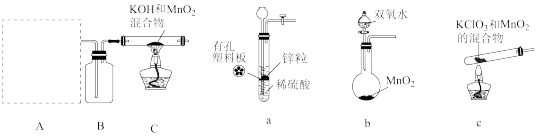
(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成
 的化学方程式为
的化学方程式为步骤Ⅱ.由
 制备
制备 。已知:
。已知: 易溶于水,水溶液呈墨绿色。主要过程如下:
易溶于水,水溶液呈墨绿色。主要过程如下:①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的
 ;
;⑧将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得
 晶体。
晶体。(4)过程②向滤液中通入足量
 ,可观察到的现象为
,可观察到的现象为(二)KMnO4的性质
已知:KMnO4具有强氧化性,可与草酸
 反应。
反应。(5)写出
 酸性溶液与草酸反应的离子方程式
酸性溶液与草酸反应的离子方程式(6)基于(5)的反应原理,选择适当试剂探究浓度对化学反应速率的影响。
可供选择的试剂有:①
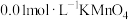 酸性溶液;②
酸性溶液;②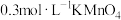 酸性溶液;③
酸性溶液;③ 溶液;④
溶液;④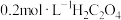 溶液,为了更好的观察现象,应选择的试剂为
溶液,为了更好的观察现象,应选择的试剂为9 . 硫及其化合物在科学研究工农业生产、农药的制备等方面具有广泛用途。某化学实验兴趣小组在实验室利用浓硫酸与Na2SO3反应制取SO2,并进行了性质探究实验装置如图所示。
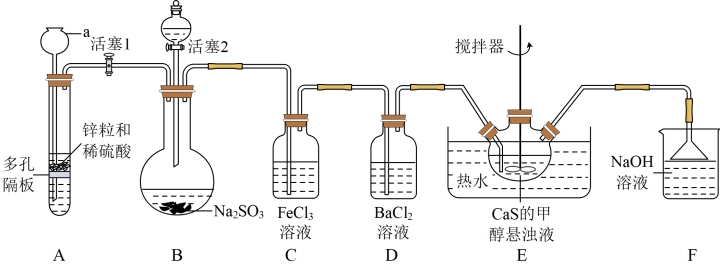
已知:Na2 SO3 + S+5H2O=Na2S2O3·5H2O,Na2S2O3·5H2O不易溶于酒精。
回答下列问题:
(1)仪器a的名称是
(2)打开活塞2进行实验,一段时间后发现C中的溶液变为浅绿色,则C中发生反应的离子方程式为
(3)先打开活塞1,向装置内通入足量的H2后,再打开活塞2,发现D中的溶液无明显变化;若只打开活塞2,不通入H2,发现D中产生白色沉淀,分析产生白色沉淀的可能原因
(4)E中生成物有S和CaSO3,则E中发生反应的化学方程式为
(5)从E的滤渣中萃取回收单质S时应选用的最佳试剂是
A.酒精 B.热NaOH溶液 C. CS2
(6)某同学用回收的S和装置F中得到的含Na2SO3吸收液制备Na2S2O3·5H2O晶体。在水溶液中,相关物质的溶解度曲线如图所示,请将实验方案补充完整:
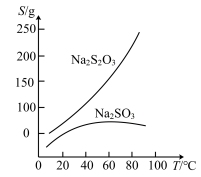
称取稍过最硫粉放入三颈烧瓶中然后加入Na2SO3吸收液,加热沸腾并不断搅拌,反应至液面只有少量硫粉时,趁热过滤、
(1)在试管中加入少量该绿矾样品,加水溶解,分别滴加稀硫酸和KSCN溶液,溶液颜色无明显变化,由此得出的结论是
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按图示连接好装置进行实验。
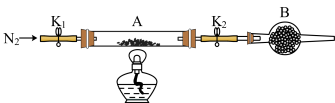
①仪器B的名称是
a.Al2O3 b.Ca(OH)2 c.CuSO4 d.NaCl
②打开K1和K2,缓缓通入N2,点燃酒精灯,加热,接下来的实验操作步骤正确排序是
a.熄灭酒精灯 b.关闭K1和K2
c.称量A d.冷却到室温



