1 . 一位同学在复习时遇到这样一道习题:某无色溶液中可能含有H+、OH-、Na+、NO ,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。已知:铝与稀硝酸反应时,主要生成气体NO,NO在空气中会进一步氧化为红棕色气体的NO2。
,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。已知:铝与稀硝酸反应时,主要生成气体NO,NO在空气中会进一步氧化为红棕色气体的NO2。
(1)未开始实验前,_______ (选填“能”、“不能”)确定溶液的酸碱性;加入铝粉产生H2,说明铝具有_______ (填“氧化性”或“还原性”)。
(2)该同学分析:若H+大量存在,则NO 就不能大量存在。设计实验证实如下:
就不能大量存在。设计实验证实如下:
①盐酸溶解Al2O3薄膜的离子方程式是_______ 。
②根据现象ⅱ,推测溶液中产生了NO,将生成NO的离子方程式补充完整:_______ 。
_______Al+_______NO +_______=_______Al3++_______NO↑+_______。
+_______=_______Al3++_______NO↑+_______。
(3)再假设:若OH-大量存在,NO 也可能大量存在。重新设计实验证实如下:
也可能大量存在。重新设计实验证实如下:
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是_______ ,该反应的氧化剂为:_______
(5)由上述实验得出:该溶液的溶质为_______ 。
 ,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。已知:铝与稀硝酸反应时,主要生成气体NO,NO在空气中会进一步氧化为红棕色气体的NO2。
,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。已知:铝与稀硝酸反应时,主要生成气体NO,NO在空气中会进一步氧化为红棕色气体的NO2。(1)未开始实验前,
(2)该同学分析:若H+大量存在,则NO
 就不能大量存在。设计实验证实如下:
就不能大量存在。设计实验证实如下:| 装置 | 现象 |
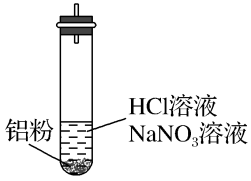 | ⅰ.实验初始,未见明显现象 ⅱ.过一会儿,出现气泡,液面上方呈浅棕色 ⅲ.试管变热,溶液沸腾 |
②根据现象ⅱ,推测溶液中产生了NO,将生成NO的离子方程式补充完整:
_______Al+_______NO
 +_______=_______Al3++_______NO↑+_______。
+_______=_______Al3++_______NO↑+_______。(3)再假设:若OH-大量存在,NO
 也可能大量存在。重新设计实验证实如下:
也可能大量存在。重新设计实验证实如下:| 装置 | 现象 |
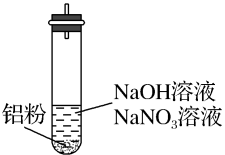 | ⅰ.实验初始,未见明显现象 ⅱ.过一会儿,出现气泡,有刺激性气味,经检验该气体含NH3 |
(5)由上述实验得出:该溶液的溶质为
您最近一年使用:0次
2021-01-06更新
|
537次组卷
|
3卷引用:第二节 金属材料 第1课时 合金
第二节 金属材料 第1课时 合金四川省南充高级中学2020-2021学年高一上学期第二次月考化学试题(已下线)5.2.3 硝酸 酸雨及其防治-2021-2022学年高一化学课后培优练(人教版2019必修第二册)
2 . 实验小组制备高铁酸钾(K2FeO4)并探究其性质。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)
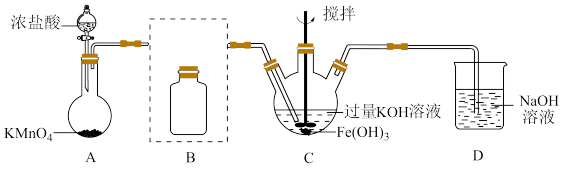
①A为氯气发生装置。A中反应方程式是________________ (锰被还原为Mn2+)。
②将除杂装置B补充完整并标明所用试剂。_______
③C中得到紫色固体和溶液,C中Cl2发生的反应有
3Cl2+2Fe(OH)3+10KOH 2K2FeO4+6KCl+8H2O,另外还有
2K2FeO4+6KCl+8H2O,另外还有________________ 。
(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
Ⅰ.由方案Ⅰ中溶液变红可知a中含有______ 离子,但该离子的产生不能判断一定是K2FeO4将Cl-氧化,还可能由________________ 产生(用方程式表示)。
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是________________ 。
②根据K2FeO4的制备实验得出:氧化性Cl2________  (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是________________ 。
③资料表明,酸性溶液中的氧化性 >
> ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
> 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:________________ 。
资料:K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4(夹持装置略)

①A为氯气发生装置。A中反应方程式是
②将除杂装置B补充完整并标明所用试剂。
③C中得到紫色固体和溶液,C中Cl2发生的反应有
3Cl2+2Fe(OH)3+10KOH
 2K2FeO4+6KCl+8H2O,另外还有
2K2FeO4+6KCl+8H2O,另外还有(2)探究K2FeO4的性质
①取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否K2FeO4氧化了Cl-而产生Cl2,设计以下方案:
| 方案Ⅰ | 取少量a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
Ⅱ.方案Ⅱ可证明K2FeO4氧化了Cl-。用KOH溶液洗涤的目的是
②根据K2FeO4的制备实验得出:氧化性Cl2
 (填“>”或“<”),而方案Ⅱ实验表明,Cl2和
(填“>”或“<”),而方案Ⅱ实验表明,Cl2和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是③资料表明,酸性溶液中的氧化性
 >
> ,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性
,验证实验如下:将溶液b滴入MnSO4和足量H2SO4的混合溶液中,振荡后溶液呈浅紫色,该现象能否证明氧化性 >
> 。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
。若能,请说明理由;若不能,进一步设计实验方案。理由或方案:
您最近一年使用:0次
2018-06-09更新
|
9677次组卷
|
31卷引用:高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 高考帮
高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 高考帮人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 高考帮2018年全国普通高等学校招生统一考试化学(北京卷)(已下线)2018年高考题及模拟题汇编 专题16 化学实验综合题(已下线)高考母题题源18 化学实验设计与探究(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第3讲 铁及其化合物 (教学案)(已下线)2019年高考总复习巅峰冲刺-专题03 氧化还原反应 离子反应应试策略(已下线)《2019年高考总复习巅峰冲刺》专题10 化学实验基础应试策略吉林省吉林市第五十五中学2018-2019学年高二下学期期末考试化学试题(已下线)专题10.3 化学实验方案的设计与评价 (讲)-《2020年高考一轮复习讲练测》宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题(已下线)专题3.3 铁及其重要化合物(讲)——2020年高考化学一轮复习讲练测(已下线)专题3.3 铁及其重要化合物(练)——2020年高考化学一轮复习讲练测(已下线)第11讲 铁及其重要化合物(精讲)——2021年高考化学一轮复习讲练测(已下线)专题讲座(三)“铁三角”综合实验题解题策略(精讲)——2021年高考化学一轮复习讲练测河南省洛阳市第一高级中学2021届高三上学期10月月考化学试题(已下线)易错22 气体实验装置的设计-备战2021年高考化学一轮复习易错题(已下线)专题讲座(九) 热点实验综合探究 (精练)-2021年高考化学一轮复习讲练测(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点33 物质的定性与定量分析-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第7讲 铁及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向14 物质制备探究-备战2022年高考化学一轮复习考点微专题四川省遂宁市射洪中学2021-2022学年高一下学期第一次月考化学试题(强基班)(已下线)第07讲 铁及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)第28讲 定性、定量实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)天津市耀华中学2023届高三第一次统练化学试题云南省玉溪市华宁县第二中学2021-2022年高一下学期开学考试化学试题第三章 金属及其化合物 第14讲 铁及其化合物的转化关系(已下线)第一部分 化学综合实验 热点6 物质性质探究实验北京一零一中学2023-2024学年高一上学期11月统练三化学试卷河北省石家庄二中实验学校2023-2024学年高一上学期12月月考化学试题
3 . 新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验:
(1) 不稳定,见光易分解生成
不稳定,见光易分解生成 和
和 。请设计实验证明有
。请设计实验证明有 生成:
生成:_______________________ 。
(2)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
(1)
 不稳定,见光易分解生成
不稳定,见光易分解生成 和
和 。请设计实验证明有
。请设计实验证明有 生成:
生成:(2)氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
| 提出问题 | 收集资料 | 提出假设 | 验证假设 | 得出结论 |
| 氯水中哪种物质能使湿润的红色布条褪色 | ①氯气有强氧化性; ②氯气与冷水反应生成盐酸和次氯酸; ③次氯酸有强氧化性 | ① ② ③ | 实验①:把红色干布条放入充满干燥氯气的集气瓶中,布条不褪色; 实验②: 实验③:把红色布条放入稀盐酸中,布条不褪色 |
您最近一年使用:0次
2020-09-01更新
|
198次组卷
|
2卷引用:苏教版(2020)高一必修第一册专题3第一单元课时2 氯气的性质及应用
4 . 绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:
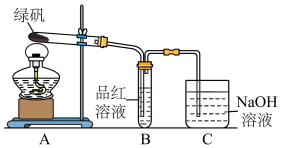
(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是_____________________________________________ ,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是______________________________ 。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中______ 。
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置 和下图部分装置 设计出了一套检验绿矾分解气态产物的装置:
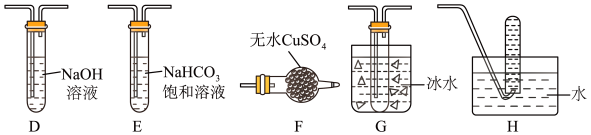
丙组同学的实验装置中,依次连接的合理顺序为A→_______ ;其中仪器F的名称___________ 。

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用

丙组同学的实验装置中,依次连接的合理顺序为A→
您最近一年使用:0次
解题方法
5 . 硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。
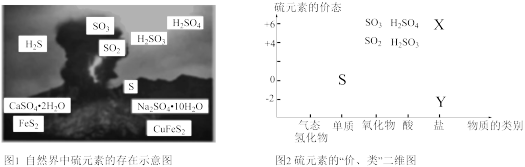
(1)从图1中选择符合图2要求的X、Y代表的物质:X_______ ,Y_______ 。
(2)硫酸是重要的化工原料,查阅资料,工业制硫酸的过程如图:
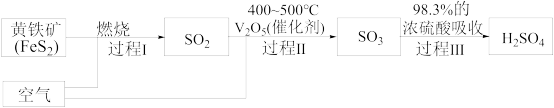
①上述过程中,没有发生氧化还原反应的是_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
②过程Ⅰ的化学反应方程式为_______ 。
③下列对浓硫酸的叙述正确的是_______ (填字母)。
A.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
B.浓硫酸具有吸水性,故能使蔗糖炭化
C.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
D.浓硫酸与亚硫酸钠反应制取 时,浓硫酸表现出强氧化性
时,浓硫酸表现出强氧化性
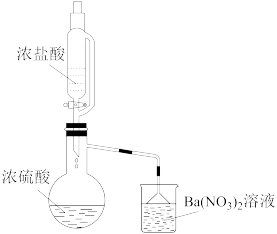
(3)某兴趣小组为验证浓硫酸的性质进行实验,如图实验中观察到蒸馏烧瓶内有白雾,原因是_______ ;烧杯中出现白色沉淀,原因是_______ 。

(1)从图1中选择符合图2要求的X、Y代表的物质:X
(2)硫酸是重要的化工原料,查阅资料,工业制硫酸的过程如图:
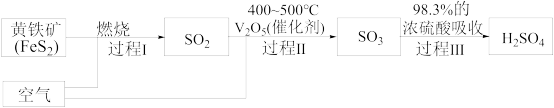
①上述过程中,没有发生氧化还原反应的是
②过程Ⅰ的化学反应方程式为
③下列对浓硫酸的叙述正确的是
A.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
B.浓硫酸具有吸水性,故能使蔗糖炭化
C.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
D.浓硫酸与亚硫酸钠反应制取
 时,浓硫酸表现出强氧化性
时,浓硫酸表现出强氧化性(3)某兴趣小组为验证浓硫酸的性质进行实验,如图实验中观察到蒸馏烧瓶内有白雾,原因是

您最近一年使用:0次
名校
解题方法
6 . 某兴趣小组利用下列试剂:铁粉、锌粉、0.1mol/LFeCl2溶液、KSCN溶液、双氧水,探究Fe2+、Fe3+的氧化性、还原性,并利用实验结论解决一些问题。
(1)用所给试剂写出体现Fe2+具有还原性的反应的离子反应方程式:___________ 。
(2)设计实验方案,完成下列表格。
(3)该兴趣小组未说明“Fe2+具有氧化性”,提出了向FeCl2溶液中加入锌粉,观察实验现象的方案,该反应的离子方程式为___________ 。
(4)电子工业中用过量的FeCl3溶液溶解电路板,产生的废液中含FeCl3、CuCl2和FeCl2.由该废液回收铜并得到净水剂(FeCl3·6H2O)的步骤如下:
Ⅰ. 废液中加入过量铁粉,过滤;
Ⅱ. 向Ⅰ的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
Ⅲ. 合并Ⅰ和Ⅱ中的滤液,通入足量氯气;
Ⅳ ……,得到FeCl3·6H2O晶体。
①试剂A是___________ ;
②取少量步骤Ⅲ所得的溶液于试管中,能够证明通入氯气足量的是___________ ;
a.检验Cl2的存在 b.检验Fe3+的存在 c.检验Fe2+的不存在
(1)用所给试剂写出体现Fe2+具有还原性的反应的离子反应方程式:
(2)设计实验方案,完成下列表格。
| 探究内容 | 实验方案 | 实验现象 |
| 探究Fe3+的化学性质 | 取少量0.1mol/LFeCl3溶液,往溶液中加入足量铁粉,再加入少量KSCN溶液 | 加入铁粉后,溶液变成 |
| 结论:Fe3+具有 | ||
(4)电子工业中用过量的FeCl3溶液溶解电路板,产生的废液中含FeCl3、CuCl2和FeCl2.由该废液回收铜并得到净水剂(FeCl3·6H2O)的步骤如下:
Ⅰ. 废液中加入过量铁粉,过滤;
Ⅱ. 向Ⅰ的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
Ⅲ. 合并Ⅰ和Ⅱ中的滤液,通入足量氯气;
Ⅳ ……,得到FeCl3·6H2O晶体。
①试剂A是
②取少量步骤Ⅲ所得的溶液于试管中,能够证明通入氯气足量的是
a.检验Cl2的存在 b.检验Fe3+的存在 c.检验Fe2+的不存在
您最近一年使用:0次
2021-12-13更新
|
178次组卷
|
2卷引用:第3课时 铁及其化合物之间的转化关系
7 . 已知70%的浓硫酸可与亚硫酸钠固体反应产生 、为探究
、为探究 的性质,某同学按如图所示的装置进行实验。
的性质,某同学按如图所示的装置进行实验。
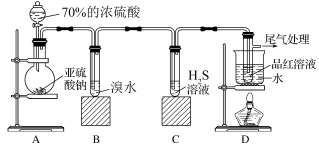
完成下列填空:
(1)实验开始后,装置B中的现象是____________ ,说明 具有
具有____________ (填序号);装置C中发生反应的化学方程式是________________________ 说明 具有
具有____________ (填序号)。
a 氧化性 b 还原性 c 漂白性 d 酸性
(2)装置D的目的是探究 与品红作用的可逆性,写出实验操作及现象
与品红作用的可逆性,写出实验操作及现象________ ;尾气可采用___________ 溶液吸收。
 、为探究
、为探究 的性质,某同学按如图所示的装置进行实验。
的性质,某同学按如图所示的装置进行实验。
完成下列填空:
(1)实验开始后,装置B中的现象是
 具有
具有 具有
具有a 氧化性 b 还原性 c 漂白性 d 酸性
(2)装置D的目的是探究
 与品红作用的可逆性,写出实验操作及现象
与品红作用的可逆性,写出实验操作及现象
您最近一年使用:0次
8 . 浓硫酸分别和三种钠盐反应,下列分析正确的是
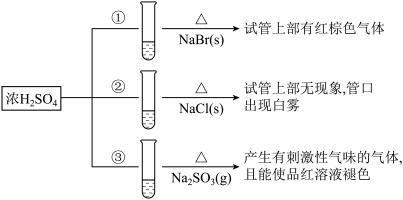
| A.对比①和②可以说明还原性Br->Cl- |
| B.①和③相比可说明氧化性Br2>SO2 |
| C.②中试管口白雾是HCl遇水蒸气所致,说明酸性H2SO4>HCl |
| D.③中浓H2SO4被还原成SO2 |
您最近一年使用:0次
2020-11-07更新
|
1201次组卷
|
33卷引用:专题4 第一单元 第2课时硫酸的制备与性质-高中化学苏教2019版必修第一册
专题4 第一单元 第2课时硫酸的制备与性质-高中化学苏教2019版必修第一册(已下线)5.1.3 不同价态含硫物质的转化(能力提升)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)2016-2017学年甘肃省天水市第一中学高一下学期第一阶段考试化学试卷上海市徐汇区2018届高三化学二模试卷(已下线)2019年8月19日《每日一题》2020年高考一轮复习—— 浓硫酸的性质山西大学附中2020届高三上学期第二次模块诊断化学试题安徽省怀宁中学2020届高三上学期第二次月考化学试题夯基提能2020届高三化学选择题对题专练——氧化还原反应的基本概念(基础过关)山东省淄博市2020届高三下学期第二次网考化学试题山东省济宁市汶上圣泽中学2019-2020学年高一下学期第二次月考化学试题北京首都师范大学第二附属中学2021届高三9月月考化学试题广东省汕头市金山中学2021届高三下学期学科素养测试化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高一下学期第一次考试化学试题河北省承德市隆化县存瑞中学2020-2021学年高二下学期期末联考化学试题(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点11 硫及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)黑龙江省双鸭山市第一中学2020-2021学年高一下学期第一次月考化学试题新疆哈密市第十五中学2021-2022学年高三上学期第一次月考化学试题山东省泰安市2021-2022年高三上学期期中统考化学试题山东省泰安市2022届高三上学期期中考试化学试题(已下线)4.1.2 硫酸的工业制备 浓硫酸的性质(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)上海外国语大学附属浦东外国语学校2021-2022学年高一下学期线上诊断化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高一下学期期中考试化学试题上海市川沙中学2020-2021学年高一下学期期中线上测试化学试题广州大学附属中学2021-2022学年高一下学期5月月考化学试题(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)3.1.2 浓硫酸和硫酸盐-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)河南省安阳市第二中学2021-2022学年高一下学期第一次段考化学试题(已下线)第15讲 硫酸-【暑假自学课】2023年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)考点10 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 浓硫酸 不同价态含硫物质的转化上海市川沙中学2023-2024学年高一下学期期中考试化学试卷 吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷
名校
9 . 某小组同学欲探究H2O2的性质,经历如下探究过程:
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是_________ 。
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。
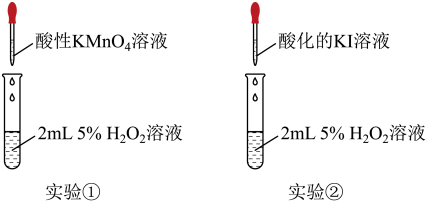
(2)实验①利用了酸性高锰酸钾的_________ 性质,该实验中,证明KMnO4溶液与H2O2反应的现象除了溶液颜色变浅或褪色外,还有________ 。
(3)实验②是为了验证H2O2的_________ 性质,在反应后的溶液中加入淀粉溶液,可观察到溶液变蓝,写出该反应的离子方程式____________ 。
解释和结论:
(4)以上实验可得出的结论是______________________ 。
预测:聚焦H2O2中的O作为核心元素,因此预测H2O2既具有氧化性,也具有还原性。
(1)预测其具有氧化性的思路是
实验和观察:小组同学分别选用酸性KMnO4溶液、酸化的KI溶液与5% H2O2溶液反应以验证预测。

(2)实验①利用了酸性高锰酸钾的
(3)实验②是为了验证H2O2的
解释和结论:
(4)以上实验可得出的结论是
您最近一年使用:0次
2020-01-10更新
|
614次组卷
|
8卷引用:专题3 本专题达标检测-高中化学苏教2019版必修第一册
名校
解题方法
10 . 向溴水中加入足量的乙醛溶液,可以看到溴水褪色,对产生该现象的原因有如下三种猜想:①溴水与乙醛发生取代反应;②由于乙醛分子中有不饱和键,溴水与乙醛发生加成反应;③由于乙醛具有还原性,溴水将乙醛氧化为乙酸。为探究哪种猜想正确,一研究性学习小组提出了如下两种实验方案:
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中 Br2 的物质的量和反应后溶液中 Br—离子的物质的量。
(1)方案一是否可行__________ 填(“是”或“否”),理由是____________________ 。
(2)假设测得反应前溴水中 Br2 的物质的量为 amol,
若测得反应后 n(Br-)=__________ mol,则说明溴水与乙醛发生取代反应;
若测得反应后 n(Br-)=__________ mol,则说明溴水与乙醛发生加成反应;
若测得反应后 n(Br-)=__________ mol,则说明溴水将乙醛氧化为乙酸。
(3)按物质的量之比为 1︰5 配制 1000mLKBrO3-KBr 溶液,该溶液在酸性条件下完全反应可生成 0.5molBr2。取该溶液 10mL 加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为 100mL,准确量取其中 10mL,加入过量的 AgNO3溶液,过滤、洗涤、干燥后称量得到固体 0.188g。若已知 CH3COOAg 易溶于水,试通过计算判断溴水与乙醛发生反应的类型为__________ (选填猜想序号)。
(4)写出上述测定过程中的三个反应的离子方程式:
①KBrO3和KBr 在酸性条件下的反应:______________________________ ;
②溴水与乙醛的反应:______________________________ ;
③测定 Br-离子含量的反应:______________________________ ;
方案一:检验褪色后溶液的酸碱性;
方案二:测定反应前溴水中 Br2 的物质的量和反应后溶液中 Br—离子的物质的量。
(1)方案一是否可行
(2)假设测得反应前溴水中 Br2 的物质的量为 amol,
若测得反应后 n(Br-)=
若测得反应后 n(Br-)=
若测得反应后 n(Br-)=
(3)按物质的量之比为 1︰5 配制 1000mLKBrO3-KBr 溶液,该溶液在酸性条件下完全反应可生成 0.5molBr2。取该溶液 10mL 加入足量乙醛溶液,使其褪色,然后将所得溶液稀释为 100mL,准确量取其中 10mL,加入过量的 AgNO3溶液,过滤、洗涤、干燥后称量得到固体 0.188g。若已知 CH3COOAg 易溶于水,试通过计算判断溴水与乙醛发生反应的类型为
(4)写出上述测定过程中的三个反应的离子方程式:
①KBrO3和KBr 在酸性条件下的反应:
②溴水与乙醛的反应:
③测定 Br-离子含量的反应:
您最近一年使用:0次
2019-01-30更新
|
324次组卷
|
3卷引用:天津市南开中学人教版高中化学选修5预习练习:第三章 第二节 醛



