1 . 硝酸银是常用化学试剂,见光或受热会分解。某兴趣小组开展以下探究活动。
I.资料查阅
①AgOH不稳定,极易分解生成 和
和 。
。
②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解为单质。
③银晶体是银白色金属光泽的固体,粉末是黑色固体,与硝酸反应的情况和铜类似。
Ⅱ.久置的硝酸银溶液底部有黑色固体甲,探究甲的成分
【猜想】固体甲中含有Ag、 中的一种或两种。
中的一种或两种。
【实验】i.取少量固体甲于试管中,加入过量稀硝酸振荡;
ii.另取少量固体甲于试管中,加入过量氨水振荡。
【结论】固体甲为Ag和 的混合物。
的混合物。
(1)①步骤i反应的离子方程式___________ 。
②写出步骤ii观察到的现象为___________ 。
【应用】
(2)实验室保存硝酸银溶液采取的措施为___________ (写出两条)。
Ⅲ.利用如图装置探究硝酸银固体受热分解的产物 至
至___________ (填现象)后再加热。
(4)加热后观察到实验现象:A中有银白色金属光泽的固体生成,出现红棕色气体。A中反应的化学方程式为___________ 。
(5)停止加热后,应再通入 一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、
一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、___________ 。
I.资料查阅
①AgOH不稳定,极易分解生成
 和
和 。
。②氧化银为棕黑色粉末,难溶于水,可溶于氨水和稀硝酸,见光或200℃左右分解为单质。
③银晶体是银白色金属光泽的固体,粉末是黑色固体,与硝酸反应的情况和铜类似。
Ⅱ.久置的硝酸银溶液底部有黑色固体甲,探究甲的成分
【猜想】固体甲中含有Ag、
 中的一种或两种。
中的一种或两种。【实验】i.取少量固体甲于试管中,加入过量稀硝酸振荡;
ii.另取少量固体甲于试管中,加入过量氨水振荡。
【结论】固体甲为Ag和
 的混合物。
的混合物。(1)①步骤i反应的离子方程式
②写出步骤ii观察到的现象为
【应用】
(2)实验室保存硝酸银溶液采取的措施为
Ⅲ.利用如图装置探究硝酸银固体受热分解的产物
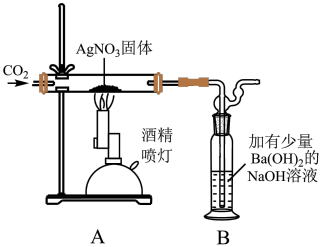
 至
至(4)加热后观察到实验现象:A中有银白色金属光泽的固体生成,出现红棕色气体。A中反应的化学方程式为
(5)停止加热后,应再通入
 一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、
一段时间再拆卸装置,目的是防止倒吸、避免固体产物与空气反应、
您最近一年使用:0次
2 . 某化学兴趣小组利用铜跟浓硫酸反应,探究 的部分性质。
的部分性质。___________ 。
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是___________ (填序号);
①水 ②饱和的 溶液 ③饱和的
溶液 ③饱和的 溶液 ④酸性
溶液 ④酸性 溶液
溶液
(3)装置C和D中产生的现象相同,但原因却不同。C中是由于 与溶液中的
与溶液中的 反应使碱性减弱,而D中则是由于
反应使碱性减弱,而D中则是由于 具有
具有___________ 性。
(4)若实验中用一定质量的铜片和
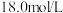 的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为
的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为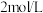 ,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾___________ mol。
 的部分性质。
的部分性质。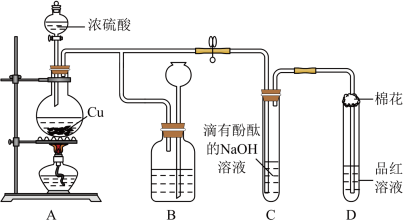
(2)装置B的作用是贮存多余的气体,B中广口瓶内应盛放的液体是
①水 ②饱和的
 溶液 ③饱和的
溶液 ③饱和的 溶液 ④酸性
溶液 ④酸性 溶液
溶液(3)装置C和D中产生的现象相同,但原因却不同。C中是由于
 与溶液中的
与溶液中的 反应使碱性减弱,而D中则是由于
反应使碱性减弱,而D中则是由于 具有
具有(4)若实验中用一定质量的铜片和

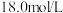 的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为
的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为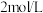 ,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾
您最近一年使用:0次
3 . 某化学研究性学习小组利用以下装置制取并探究氨气的性质,回答下列问题:___________ 。
(2)B装置中的干燥剂成分是___________ 。气流通过C、D装置时候分别观察到的现象:C. ___________ 、D.___________ 。
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到E装置中的现象是产生___________ 。
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是___________ (填“F”或“G”)。

(2)B装置中的干燥剂成分是
(3)当实验进行一段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到E装置中的现象是产生
(4)为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是
您最近一年使用:0次
4 . 某化学自主实验小组利用如图所示装置(K1、K2为止水夹,夹持装置已略去)探究NO2能否被NH3还原。
(1)a仪器名称为_______ 。
(2)甲中盛放的试剂的名称是_______ ,乙中盛放的试剂的化学式为_______ 。
(3)C中铜与浓硝酸反应时,体现的浓硝酸的性质为_______ ,C中实验现象为_______ 。
(4)实验过程中观察到B中红棕色气体逐渐变淡至无色,经检测发现尾气中的有害气体只有未完全反应的反应物,则B中发生反应的化学方程式为_______ ,其中n(还原产物):n(氧化产物)=_______ 。
(5)NaOH溶液可吸收过量的NO2,二者反应生成两种钠盐,则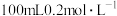 NaOH溶液最多能吸收
NaOH溶液最多能吸收_______ mol NO2.(忽略气体在水中的溶解及气体与水的反应)

(1)a仪器名称为
(2)甲中盛放的试剂的名称是
(3)C中铜与浓硝酸反应时,体现的浓硝酸的性质为
(4)实验过程中观察到B中红棕色气体逐渐变淡至无色,经检测发现尾气中的有害气体只有未完全反应的反应物,则B中发生反应的化学方程式为
(5)NaOH溶液可吸收过量的NO2,二者反应生成两种钠盐,则
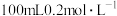 NaOH溶液最多能吸收
NaOH溶液最多能吸收
您最近一年使用:0次
5 . 非金属元素硫在化工生产中扮演重要角色,实验室制备及探究某些含硫化合物。
Ⅰ.利用 和
和 反应合成硫酰氯
反应合成硫酰氯 ,已知
,已知 的熔点为
的熔点为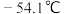 ,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成
,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成 和
和 。实验室合成
。实验室合成 的原理:
的原理: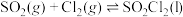 ,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:_____ 。
(2)装置戊上方分液漏斗中最好选用_____ (填字母)。
a.蒸馏水 b.饱和食盐水 c. 盐酸 d.浓氢氧化钠溶液
盐酸 d.浓氢氧化钠溶液
(3)装置乙和丁盛放的试剂均是浓硫酸,其作用是_____ 。
(4)装置丙放置在冰水浴中的原因是_____ 。
Ⅱ.探究 使品红溶液褪色的原因
使品红溶液褪色的原因
操作1:将 通入品红溶液中,品红溶液褪色。
通入品红溶液中,品红溶液褪色。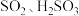 、
、_____ 。
已知:品红是一种棕红色晶体状有机染料,微溶于水,溶于乙醇和酸,溶液呈红色。
②实验设计:小组结合以上信息,设计如下实验证明使品红褪色的微粒不是 请完成表格。
请完成表格。
Ⅰ.利用
 和
和 反应合成硫酰氯
反应合成硫酰氯 ,已知
,已知 的熔点为
的熔点为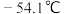 ,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成
,沸点为69.1℃,在空气中遇水蒸气发生剧烈反应,并产生大量HCl白雾,100℃以上分解生成 和
和 。实验室合成
。实验室合成 的原理:
的原理: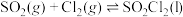 ,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题:
,且反应会放出大量的热。实验装置如图所示(夹持仪器已省略),请回答下列问题: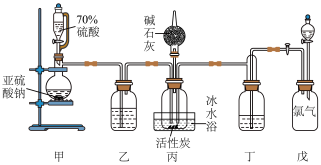
(2)装置戊上方分液漏斗中最好选用
a.蒸馏水 b.饱和食盐水 c.
 盐酸 d.浓氢氧化钠溶液
盐酸 d.浓氢氧化钠溶液(3)装置乙和丁盛放的试剂均是浓硫酸,其作用是
(4)装置丙放置在冰水浴中的原因是
Ⅱ.探究
 使品红溶液褪色的原因
使品红溶液褪色的原因操作1:将
 通入品红溶液中,品红溶液褪色。
通入品红溶液中,品红溶液褪色。
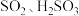 、
、已知:品红是一种棕红色晶体状有机染料,微溶于水,溶于乙醇和酸,溶液呈红色。
②实验设计:小组结合以上信息,设计如下实验证明使品红褪色的微粒不是
 请完成表格。
请完成表格。| 操作2 | 现象 |
| 不褪色 |
您最近一年使用:0次
6 . NH3一种重要的化工原料,可用于制氮肥、HNO3、铵盐、纯碱等。某实验小组设计了如下实验装置制取NH3,回答下列问题:
(1)NH3的制备___________ 。
②实验室用装置D作为制取氨气的发生装置,该反应的化学方程式为___________ ;若用装置B作为制取氨气的发生装置,分液漏斗中盛装的试剂名称为___________ 。
③欲收集一瓶干燥的氨气,选择上图中的装置。其连接顺序为:发生装置→___________ (按气流方向,用小写字母表示)。
(2)工业上NH3经一系列反应可制取硝酸,某校课外活动小组为了探究铜与稀硝酸反应产生的气体是NO,设计了如图实验,实验过程中同时用石灰水吸收产生的氮氧化物获得应用广泛的Ca(NO3)2,实验装置如图所示:___________ 。
②在①操作后将装置A中铜丝插入稀硝酸,溶液显蓝色,有无色气体生成,其中发生反应的离子方程式是___________ ;该反应体现了硝酸的___________ 性。
③装置B中用注射器压入空气之后现象是___________ ;反应的化学方程式是___________ 。
④D装置的作用是___________ 。
(1)NH3的制备

②实验室用装置D作为制取氨气的发生装置,该反应的化学方程式为
③欲收集一瓶干燥的氨气,选择上图中的装置。其连接顺序为:发生装置→
(2)工业上NH3经一系列反应可制取硝酸,某校课外活动小组为了探究铜与稀硝酸反应产生的气体是NO,设计了如图实验,实验过程中同时用石灰水吸收产生的氮氧化物获得应用广泛的Ca(NO3)2,实验装置如图所示:

②在①操作后将装置A中铜丝插入稀硝酸,溶液显蓝色,有无色气体生成,其中发生反应的离子方程式是
③装置B中用注射器压入空气之后现象是
④D装置的作用是
您最近一年使用:0次
7 . 某小组同学利用下图所示装置完成碳与浓硫酸反应的实验,并验证所得全部产物。请完成下列空白。___________ ;
(2)写出浓硫酸和木炭粉发生反应的化学方程式:___________ ,在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“强氧化”)性;。
(3)如果用图中的装置检验上述反应的全部产物,请回答下列问题:
①A中加入的试剂___________ ,B作用是___________ 。
②C中应观察到的现象是___________ ,体现了SO2的性质是___________ 。
a.漂白性 b.氧化性 c.还原性
(4)浓硫酸具有:a.脱水性;b.酸性;c.强氧化性;d.吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加___________ 。
②浓硫酸与铜共热,浓硫酸表现的性质是___________ 。

(2)写出浓硫酸和木炭粉发生反应的化学方程式:
(3)如果用图中的装置检验上述反应的全部产物,请回答下列问题:
①A中加入的试剂
②C中应观察到的现象是
a.漂白性 b.氧化性 c.还原性
(4)浓硫酸具有:a.脱水性;b.酸性;c.强氧化性;d.吸水性;下列各项分别表现浓硫酸的什么性质,请将字母填于空白处:
①盛有浓硫酸的烧杯敞口放置一段时间后,质量增加
②浓硫酸与铜共热,浓硫酸表现的性质是
您最近一年使用:0次
名校
8 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。_______ ,仪器组装完成后,关闭两端活塞,向装置B的长颈漏斗内注入液体至形成段液柱,若_______ 则整个装置气密性良好。
(2)A中如果用浓硫酸和铜反应,也可制得 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为_______ 。
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀
溶液,产生白色沉淀
上述方案合理的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”); 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为_______ 。
(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为_______ 溶液。

(2)A中如果用浓硫酸和铜反应,也可制得
 进行实验,反应的化学方程式为
进行实验,反应的化学方程式为(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行实验:
方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀
溶液,产生白色沉淀上述方案合理的是方案
 通入KMnO4溶液中发生的主要反应的离子方程式为
通入KMnO4溶液中发生的主要反应的离子方程式为(5)装置E的作用是做安全瓶,防止F中的液体倒吸入D中,装置F中为
您最近一年使用:0次
名校
9 . Ⅰ.某同学完成了如下系列实验,探究元素周期表中元素性质的递变规律.
(1)为验证金属与稀酸的反应速率,将Na、Lⅰ、Fe、Al各0.28mol分别投入到足量的2.2mol/L的硫酸中,实验结果为:___________ 与硫酸反应速率最慢,___________ 与硫酸反应产生的气体最多;(填元素符号)
(2)向 溶液中通入适量氯气出现黄色浑浊,可证明Cl的非金属性比S强,但是氯气过量后会发现黄色浑浊减少甚至消失,在此溶液中检测到有两种强酸,黄色浑浊减少甚至消失反应的离子方程式为
溶液中通入适量氯气出现黄色浑浊,可证明Cl的非金属性比S强,但是氯气过量后会发现黄色浑浊减少甚至消失,在此溶液中检测到有两种强酸,黄色浑浊减少甚至消失反应的离子方程式为___________ 。
Ⅱ.验证主族元素非金属性的变化规律设计了如图装置
(3)某研究小组想用该装置一次性验证 的非金属性的变化规律,则装置A、C中所装药品分别为
的非金属性的变化规律,则装置A、C中所装药品分别为___________ 、___________ .该实验采用的理论依据为___________ ;
(4)铝用途广泛,可与强碱溶液反应,请书写铝与氢氧化钠溶液反应的化学方程式:___________ ;
Ⅳ.粮食安全问题很重要,储存环节要避免虫蛀.工业上可用以下方法制备粮食储备的强效熏虫剂 .
. 为
为___________ (填“一”、“二”或“三”)元酸.
(6)不考虑产物的损失,标准状况下若有 参加反应,则整个工业流程中共生成
参加反应,则整个工业流程中共生成___________ 升 气体.
气体.
(1)为验证金属与稀酸的反应速率,将Na、Lⅰ、Fe、Al各0.28mol分别投入到足量的2.2mol/L的硫酸中,实验结果为:
(2)向
 溶液中通入适量氯气出现黄色浑浊,可证明Cl的非金属性比S强,但是氯气过量后会发现黄色浑浊减少甚至消失,在此溶液中检测到有两种强酸,黄色浑浊减少甚至消失反应的离子方程式为
溶液中通入适量氯气出现黄色浑浊,可证明Cl的非金属性比S强,但是氯气过量后会发现黄色浑浊减少甚至消失,在此溶液中检测到有两种强酸,黄色浑浊减少甚至消失反应的离子方程式为Ⅱ.验证主族元素非金属性的变化规律设计了如图装置
(3)某研究小组想用该装置一次性验证
 的非金属性的变化规律,则装置A、C中所装药品分别为
的非金属性的变化规律,则装置A、C中所装药品分别为
(4)铝用途广泛,可与强碱溶液反应,请书写铝与氢氧化钠溶液反应的化学方程式:
Ⅳ.粮食安全问题很重要,储存环节要避免虫蛀.工业上可用以下方法制备粮食储备的强效熏虫剂
 .
.
 为
为(6)不考虑产物的损失,标准状况下若有
 参加反应,则整个工业流程中共生成
参加反应,则整个工业流程中共生成 气体.
气体.
您最近一年使用:0次


 与
与



