名校
解题方法
1 . 下图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电的关系的装置图。
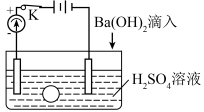
首先在水槽中加入200 mL 2 mol·L-1的H2SO4溶液,同时将一个表面光滑的小球放入溶液中,小球悬浮在溶液中央,闭合开关K,电流计发生偏转,然后再进行以下操作。请回答问题。
(1)向溶液中逐滴加入与H2SO4溶液密度相同的Ba(OH)2溶液至反应完全,观察到的现象是___________ ,反应的化学方程式是___________ ;
(2)将Ba(OH)2溶液换成浓度相同(假设密度也相同)的以下三种溶液(设反应后的体积为两溶液的体积和):
A.Ba(NO3)2 B.Na2SO4 C.Na2CO3
①滴加A的过程中,观察到的现象是___________ ,反应的化学方程式是___________ ;
②滴加B的过程中,小球的位置___________ ,电流计的偏转程度___________ ;
③滴加C的过程中,观察到的现象是___________ ,反应的化学方程式是___________ ,生成的Na2SO4的物质的量浓度为___________ 。

首先在水槽中加入200 mL 2 mol·L-1的H2SO4溶液,同时将一个表面光滑的小球放入溶液中,小球悬浮在溶液中央,闭合开关K,电流计发生偏转,然后再进行以下操作。请回答问题。
(1)向溶液中逐滴加入与H2SO4溶液密度相同的Ba(OH)2溶液至反应完全,观察到的现象是
(2)将Ba(OH)2溶液换成浓度相同(假设密度也相同)的以下三种溶液(设反应后的体积为两溶液的体积和):
A.Ba(NO3)2 B.Na2SO4 C.Na2CO3
①滴加A的过程中,观察到的现象是
②滴加B的过程中,小球的位置
③滴加C的过程中,观察到的现象是
您最近一年使用:0次
名校
解题方法
2 . 某同学做同周期元素性质递变实验时,自己设计了一套实验方案,并记录了有关实验现象如下表。
(1)请从表中实验现象(Ⅱ)中分别选出(I)对应的现象,将其序号(A、B、C……)填入(Ⅲ)中,并写出相应的化学方程式:
(2)通过以上实验分析同周期元素的符号是___________ ;
(3)从实验结果可以得出的结论是___________ ;
(4)从结构理论上简单说明具有上述结论的原因___________ 。
(1)请从表中实验现象(Ⅱ)中分别选出(I)对应的现象,将其序号(A、B、C……)填入(Ⅲ)中,并写出相应的化学方程式:
| 实验方案(I) | 实验现象(Ⅱ) | 答案(Ⅲ) | ||
| I | Ⅱ | 化学方程式 | ||
| 1.用砂纸擦过的镁带与沸水反应,再向反应液中滴加酚酞试液 | A.浮于水面,熔成小球,在水面上不定向移动,随之消失,溶液变成红色 | 1 | ||
| 2.钠与滴有酚酞试液的冷水反应 | B.产生大量可在空气中燃烧的气体,溶液变成浅红色 | 2 | ||
3.镁带与2 的盐酸反应 的盐酸反应 | C.反应不十分剧烈,产生的气体可在空气中燃烧 | 3 | ||
4.铝与2 的盐酸反应 的盐酸反应 | D.剧烈反应,产生的气体可在空气中燃烧 | 4 | ||
(3)从实验结果可以得出的结论是
(4)从结构理论上简单说明具有上述结论的原因
您最近一年使用:0次
名校
3 . 人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图1装置制备氨气,探究其相关性质。

I.实验室制取氨气。
(1)图1装置中生成 的化学方程式为
的化学方程式为___________ 。
II.用图2所示装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(2)仪器b的名称是___________ ,b中无水硫酸铜的作用是___________ 。
(3)实验中观察到a中粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为___________ 。
(4)若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为_____ g(保留小数点后一位)。
III.按下图装置进行 其他性质实验,A、B容器的容积相同。
其他性质实验,A、B容器的容积相同。

(5)先打开旋塞1,B瓶中的现象是___________ ,原因是___________ ;稳定后,关闭旋塞1,再打开旋塞2,B瓶中的现象是___________ 。

I.实验室制取氨气。
(1)图1装置中生成
 的化学方程式为
的化学方程式为II.用图2所示装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

(2)仪器b的名称是
(3)实验中观察到a中粉末变红(一种单质),b中无水硫酸铜变蓝,并收集到一种单质气体。则该反应的化学方程式为
(4)若向a中通入标准状况下3.36L的氨气,最终得到铜的质量为
III.按下图装置进行
 其他性质实验,A、B容器的容积相同。
其他性质实验,A、B容器的容积相同。
(5)先打开旋塞1,B瓶中的现象是
您最近一年使用:0次
解题方法
4 . 实验室用如图所示装置制备干燥纯净的 并验证氯气没有漂白性。
并验证氯气没有漂白性。
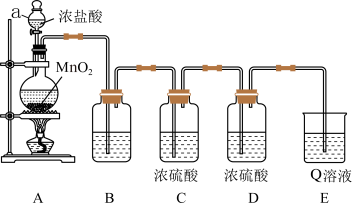

回答下列问题:
(1)仪器 的名称是
的名称是_________ ,装置 中制备氯气的离子方程式为
中制备氯气的离子方程式为____________________________________ 。
(2)装置 中盛放的试剂是
中盛放的试剂是_________ ;欲证明氯气没有漂白性,装置 应置于装置
应置于装置_________ 之间(填字母)。
(3)若Q溶液是 溶液(滴有2滴淀粉试液),则
溶液(滴有2滴淀粉试液),则 中的现象是
中的现象是___________________________ ;若 溶液是
溶液是 溶液且当其恰好反应完后,向
溶液且当其恰好反应完后,向 中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是
中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是_______ ,写出 溶液吸收
溶液吸收 反应的化学方程式:
反应的化学方程式:__________________ 。
 并验证氯气没有漂白性。
并验证氯气没有漂白性。

回答下列问题:
(1)仪器
 的名称是
的名称是 中制备氯气的离子方程式为
中制备氯气的离子方程式为(2)装置
 中盛放的试剂是
中盛放的试剂是 应置于装置
应置于装置(3)若Q溶液是
 溶液(滴有2滴淀粉试液),则
溶液(滴有2滴淀粉试液),则 中的现象是
中的现象是 溶液是
溶液是 溶液且当其恰好反应完后,向
溶液且当其恰好反应完后,向 中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是
中加入2滴酚酞试液,溶液先变红后褪色,由此说明所得溶液具有的化学性质是 溶液吸收
溶液吸收 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
解题方法
5 . 草酸(乙二酸)存在于自然界的植物中,草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。甲组同学按照如图所示的装置检验草酸晶体的分解产物。实验过程中,装置C、G中均出现浑浊。

回答下列问题:
(1)装置A试管口向上而不向下倾斜的原因是_______ 。
(2)装置B的主要作用是_______ 。若无装置B,则不能证明草酸晶体的分解产物中含有CO2,其原因是_______ 。
(3)装置D的主要作用是_______ 。为证明装置D的作用,可以在装置D和装置E之间,增加一个盛放_______ (填试剂名称)的洗气瓶。
(4)能证明草酸晶体分解产物中有CO的现象是_______ 。
(5)根据草酸晶体的性质和实验可知,草酸晶体分解的化学方程式为_______ 。

回答下列问题:
(1)装置A试管口向上而不向下倾斜的原因是
(2)装置B的主要作用是
(3)装置D的主要作用是
(4)能证明草酸晶体分解产物中有CO的现象是
(5)根据草酸晶体的性质和实验可知,草酸晶体分解的化学方程式为
您最近一年使用:0次
6 . 水垢的主要成分是 和
和 ,某同学为测定水垢中
,某同学为测定水垢中 的质量分数,称取了mg水垢,设计如图所示装置进行实验。
的质量分数,称取了mg水垢,设计如图所示装置进行实验。
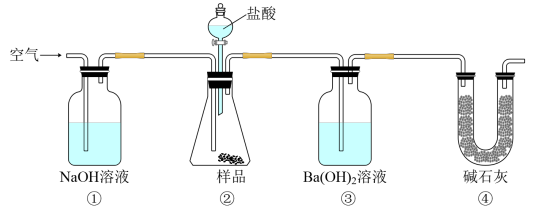
下列说法错误的是
 和
和 ,某同学为测定水垢中
,某同学为测定水垢中 的质量分数,称取了mg水垢,设计如图所示装置进行实验。
的质量分数,称取了mg水垢,设计如图所示装置进行实验。
下列说法错误的是
A.装置③中的离子方程式为 |
B.装置④能防止空气中的 进入装置③中 进入装置③中 |
| C.反应完全后如果不通入空气,则会使测量结果偏高 |
D.称量装置③中产生沉淀的质量即可计算出水垢中 的质量分数 的质量分数 |
您最近一年使用:0次
2022-01-13更新
|
106次组卷
|
2卷引用:海南省2021-2022学年高一上学期期末学业水平诊断化学试题
7 . 某化学兴趣小组欲制取氯酸钾和氯水并进行有关探究实验。
实验一:制取氯酸钾和氯水。
利用如图所示的实验装置(部分夹持装置已省略)进行实验。
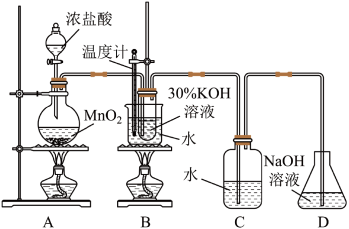
(1)将Cl2通入B装置中得到的含氯产物为KClO3和KCl,该反应的离子方程式为___ 。
(2)制取实验结束后,取出B中试管冷却结晶、过滤洗涤。过滤时需要用到的玻璃仪器有烧杯、玻璃棒、___ 。
实验二:比较Cl2、Br2、I2的氧化性强弱。
为比较Cl2、Br2、I2的氧化性强弱,设计了如图所示的实验步骤:
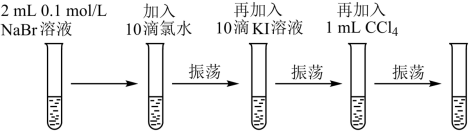
(3)加入10滴氯水时发生反应的离子方程式为___ 。
(4)加入10滴KI溶液时,溶液的颜色由橙黄色变为橙红色,说明氧化性:___ (填“Br2”或“I2”,下同)>___ 。
(5)加入1mLCCl4后,振荡静置,最终试管中的现象为___ 。
实验一:制取氯酸钾和氯水。
利用如图所示的实验装置(部分夹持装置已省略)进行实验。

(1)将Cl2通入B装置中得到的含氯产物为KClO3和KCl,该反应的离子方程式为
(2)制取实验结束后,取出B中试管冷却结晶、过滤洗涤。过滤时需要用到的玻璃仪器有烧杯、玻璃棒、
实验二:比较Cl2、Br2、I2的氧化性强弱。
为比较Cl2、Br2、I2的氧化性强弱,设计了如图所示的实验步骤:

(3)加入10滴氯水时发生反应的离子方程式为
(4)加入10滴KI溶液时,溶液的颜色由橙黄色变为橙红色,说明氧化性:
(5)加入1mLCCl4后,振荡静置,最终试管中的现象为
您最近一年使用:0次
8 . 利用如图所示的装置和其他必要的仪器用品,完成下列实验。

已知2NH3+3CuO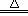 N2+3Cu+3H2O,该实验证明氨气具有还原性。
N2+3Cu+3H2O,该实验证明氨气具有还原性。
(1)碱石灰的作用是______________ ,倒扣漏斗的作用是___________________ 。
(2)浓氨水与固体NaOH接触,会逸出大量氨气原因是______________________ 。
(3)硬质玻璃管中可观察到的实验现象是_________________________________ 。
(4)常温下,若氨水与稀硫酸恰好完全中和,则所得溶液中各离子浓度的大小顺序为_________ 。

已知2NH3+3CuO
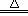 N2+3Cu+3H2O,该实验证明氨气具有还原性。
N2+3Cu+3H2O,该实验证明氨气具有还原性。(1)碱石灰的作用是
(2)浓氨水与固体NaOH接触,会逸出大量氨气原因是
(3)硬质玻璃管中可观察到的实验现象是
(4)常温下,若氨水与稀硫酸恰好完全中和,则所得溶液中各离子浓度的大小顺序为
您最近一年使用:0次
2016-12-09更新
|
418次组卷
|
5卷引用:2016届海南省文昌中学高三上学期期末考试化学试卷
解题方法
9 . 在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。
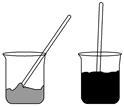
请回答:
(1) 生成的黑色(单质)物质是________ (填化学式)。
(2) 这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是________ (填名称),实验室经常用________ 溶液进行吸收,写出生成这种气体的化学方程式分别为:__________________ ;
(3) 据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有_______________ (填序号)。
(4) 将实验(2)产生的刺激性气味气体通入品红溶液,可以看到品红溶液________ ,加热后________ 。
(5) 能否用澄清石灰水鉴别这两种气体?____________ (填“能”或“不能”)若不能填写两种能鉴别的试剂是________________________ 。

请回答:
(1) 生成的黑色(单质)物质是
(2) 这种黑色物质继续与浓硫酸作用会产生两种气体,其中一种气体有刺激性气味,是大气的主要污染物之一,这种刺激性气味的气体成分是
(3) 据蔗糖与浓硫酸反应的实验现象,说明浓硫酸具有
| A.酸性 | B.吸水性 | C.脱水性 | D.强氧化性 |
(5) 能否用澄清石灰水鉴别这两种气体?
您最近一年使用:0次
2016-12-09更新
|
227次组卷
|
2卷引用:海南省海口市海南枫叶国际学校2019-2020学年高一下学期期末考试化学试题
解题方法
10 . 按下图装置进行如下实验,请用你所学知识完成下题:
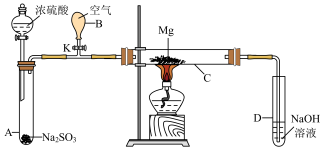
先关闭K,使A中反应进行,加热玻璃管C,可观察到C管中发生耀眼白光,产生白烟,管壁上附有淡黄色物质。实验完成后将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。
(1)停止实验时,先打开K,再停止滴加浓硫酸并熄灭酒精灯,橡胶气胆B在实验中的作用是___________ 。
(2)C中全部反应产物有___________ 、___________ 、___________ (填化学式)。

先关闭K,使A中反应进行,加热玻璃管C,可观察到C管中发生耀眼白光,产生白烟,管壁上附有淡黄色物质。实验完成后将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。
(1)停止实验时,先打开K,再停止滴加浓硫酸并熄灭酒精灯,橡胶气胆B在实验中的作用是
(2)C中全部反应产物有
您最近一年使用:0次



