名校
解题方法
1 . 为了探究元素周期律,设计实验验证卤素单质氧化性的相对强弱,实验如下:
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
(1)a中反应的离子方程式是___________ 。
(2)实验I中b可以得出的氧化性强弱是___________ 。
(3)①甲同学认为:实验Ⅱ观察到___________ 现象,得出氧化性Br2>I2。
②乙同学对上述实验进行反思,认为实验II不能充分证明氧化性Br2>I2,他补做了实验Ⅲ.
补做实验Ⅲ的目的是___________ 。
综合实验I和Ⅲ,得出氧化性Cl2>Br2>I2.由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐减弱
资料:稀溴水呈黄色;浓溴水呈红棕色;碘水呈棕黄色。
| 实验I | 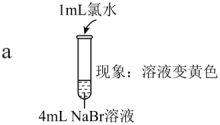 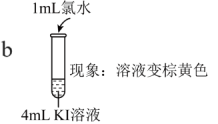 |
| 实验II | 取a中的黄色溶液少许,加入KI溶液,再加入淀粉溶液。 |
(1)a中反应的离子方程式是
(2)实验I中b可以得出的氧化性强弱是
(3)①甲同学认为:实验Ⅱ观察到
②乙同学对上述实验进行反思,认为实验II不能充分证明氧化性Br2>I2,他补做了实验Ⅲ.
| 实验III | 另取a中黄色溶液少许,加入足量NaBr固体,振荡,然后加入KI溶液和淀粉溶液。 |
综合实验I和Ⅲ,得出氧化性Cl2>Br2>I2.由此实验得出的结论:同主族元素从上到下,原子的得电子能力逐渐减弱
您最近一年使用:0次
2024-02-13更新
|
75次组卷
|
2卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
2 . 下图是实验室制备氯气并进行一系列相关实验的部分装置(夹持设备已略)。
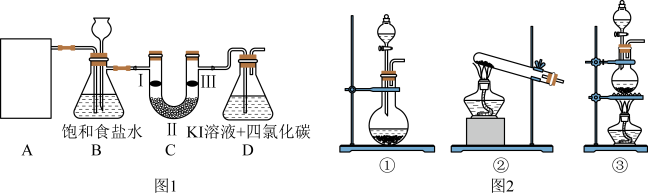
(1)实验室可以用 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为_______ 。该实验中,A部分的发生装置可选图2中的_______ (填序号)。
(2)装置B中饱和食盐水的作用是_______ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,写出发生堵塞时B中的现象_______ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入_______ (填字母)。
(4)设计装置D的目的是比较氯、碘单质的氧化性。当向D中缓缓通入一定量氯气时,观察到D中_______ ,即可证明 氧化性大于
氧化性大于 。
。
(5)该实验装置存在明显的缺陷,应进行的改进措施是_______ (用离子方程式表示)。

(1)实验室可以用
 与浓盐酸反应制备氯气,发生反应的化学方程式为
与浓盐酸反应制备氯气,发生反应的化学方程式为(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,则C中I、Ⅱ、Ⅲ应依次放入
| 选项 | a | b | c | d |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 浓硫酸 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
 氧化性大于
氧化性大于 。
。(5)该实验装置存在明显的缺陷,应进行的改进措施是
您最近一年使用:0次
2023-07-31更新
|
311次组卷
|
3卷引用:宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题
宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题陕西省汉中市2020-2021学年高一上学期期末考试化学试题(已下线)期末测试卷02-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
3 . 资料显示:“氨气可在纯氧中安静燃烧……”。某校化学小组学生设计如图装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验。
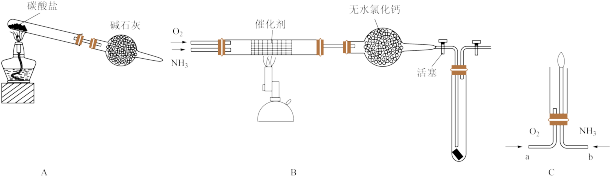
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是__________ ;碱石灰的作用是________________________ 。
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:氨催化氧化的化学方程式是_________________________ ;试管内气体变为红棕色,该反应的化学方程式是______________ 。
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是________ ,其理由是_____________ 。
②氨气燃烧的化学方程式是_______________________________ 。

(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:氨催化氧化的化学方程式是
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通入到装置C中,并在b管上端点燃氨气:
①两气体通入的先后顺序是
②氨气燃烧的化学方程式是
您最近一年使用:0次
2016-12-09更新
|
225次组卷
|
2卷引用:宁夏石嘴山三中2015-2016学年上学期高一(上)期末化学试卷(解析版)
4 . 如图装置可用于收集SO2并验证其某些化学性质,下列说法正确的是
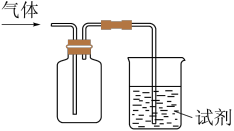
| 选项 | 试剂 | 现象 | 结论 |
| A | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | 品红溶液 | 溶液褪色 | SO2有漂白性 |
| C | 滴有酚酞的NaOH溶液 | 溶液褪色 | SO2有漂白性 |
| D | 硫化氢水溶液 | 溶液变浑浊 | SO2有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-01-28更新
|
630次组卷
|
9卷引用:宁夏银川一中2019-2020学年高一上学期期末考试化学试题
宁夏银川一中2019-2020学年高一上学期期末考试化学试题【全国百强校】山东省济南市第一中学2018-2019学年高一上学期期末考试化学试题苏教版(2020)高一必修第一册专题4第一单元课时1 硫、二氧化硫和三氧化硫鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时1 硫、二氧化硫和三氧化硫高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时1 硫和二氧化硫辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期开学考试化学试题广东省深圳聚龙科学中学2022-2023学年高一下学期第一次段考(学业水平)化学试题河南省实验中学2023-2024学年高一上学期月考 化学试卷陕西省西安市蓝田县田家炳中学大学区联考2023-2024学年高一下学期4月月考化学试题
名校
5 . 某研究性学习小组设计了如图装置制取和验证SO2的性质。
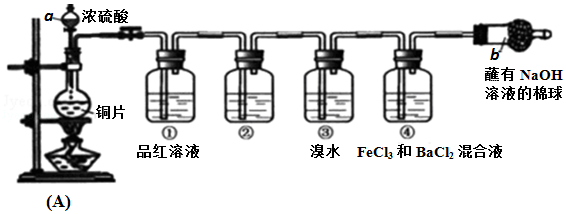
请回答:
(1)写出A反应装置中的化学方程式:____________
(2)棉球中NaOH溶液的作用是________________
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是_________ 。
A.澄清石灰水 B.无色酚酞试液 C.碘水 D.紫色石蕊试液
(4)下列说法正确的是____________ 。
A.先向装置中加入试剂(药品),再进行气密性检查
B.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
C.实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)写出洗气瓶③中反应的化学方程式:_____________

请回答:
(1)写出A反应装置中的化学方程式:
(2)棉球中NaOH溶液的作用是
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是
A.澄清石灰水 B.无色酚酞试液 C.碘水 D.紫色石蕊试液
(4)下列说法正确的是
A.先向装置中加入试剂(药品),再进行气密性检查
B.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
C.实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)写出洗气瓶③中反应的化学方程式:
您最近一年使用:0次
2019-01-17更新
|
143次组卷
|
2卷引用:【全国百强校】宁夏回族自治区银川一中2018-2019学年高一上学期期末考试化学试题
6 . 某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:
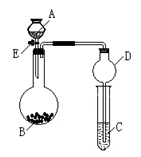
(1)若A为水,B为过氧化钠,C中盛有稀硫酸和FeCl2混合溶液,旋开 活塞E后,C中溶液颜色变化为____________________ ,烧瓶中发生反应的化学方程式为_____________________ 。
(2)若A为盐酸、B为大理石(主要成分为CaCO3粉末)、C中盛有水玻璃,则小试管中的现象是__________ ,固体的主要成分为(写化学式)_________________ 。
(3)利用上述装置可以验证SO2的性质, 若A为浓硫酸,B为亚硫酸钠粉末,那么C中盛有_________ 溶液时可验证其具有漂白性;而C中盛有______________ 溶液时可验证其具有还原性(各填一种物质名称)。

(1)若A为水,B为过氧化钠,C中盛有稀硫酸和FeCl2混合溶液,旋开 活塞E后,C中溶液颜色变化为
(2)若A为盐酸、B为大理石(主要成分为CaCO3粉末)、C中盛有水玻璃,则小试管中的现象是
(3)利用上述装置可以验证SO2的性质, 若A为浓硫酸,B为亚硫酸钠粉末,那么C中盛有
您最近一年使用:0次
7 . 实验室中用浓硫酸与亚硫酸钠制备SO2并探究其相关性质,所用实验装置如图所示。(CCl4是一种密度比水大的有机溶剂,SO2不溶于CCl4)下列叙述不正确的是


| A.装置①可用于实验室制备CO2 |
| B.装置②中溴水褪色说明SO2具有漂白性 |
| C.装置③中会出现浑浊现象,体现SO2的氧化性 |
| D.装置④中CCl4的作用是防倒吸 |
您最近一年使用:0次
2022-03-14更新
|
400次组卷
|
4卷引用:宁夏石嘴山市平罗中学2021-2022学年高一上学期期末考试化学试题
名校
8 . 某兴趣小组探究SO2气体还原Fe3+、I2,它们使用的药品和装置如图所示

(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是___________ 、___________ 。
(2)下列实验方案适用于在实验室制取所需SO2的是______________________ 。
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.硫化氢在纯氧中燃烧
(3)装置C的作用是_________________________________ 。
(4)装置B中反应的离子方程式____________________________________________ 。
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿色,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的方案是___________ ,原因是___________ 。

(1)SO2气体和Fe3+反应的氧化产物、还原产物分别是
(2)下列实验方案适用于在实验室制取所需SO2的是
A.Na2SO3溶液与HNO3 B.Na2SO3固体与浓硫酸
C.固体硫在纯氧中燃烧 D.硫化氢在纯氧中燃烧
(3)装置C的作用是
(4)装置B中反应的离子方程式
(5)在上述装置中通入过量的SO2为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入酸性KMnO4溶液,紫红色褪去。
方案②:往第二份试液中加入NaOH溶液,产生白色沉淀,并迅速转为灰绿色,最后呈红褐色。
方案③:往第三份试液中加入用稀盐酸酸化的BaCl2,产生白色沉淀。
上述方案不合理的方案是
您最近一年使用:0次
2019-01-30更新
|
163次组卷
|
6卷引用:【市级联考】宁夏回族自治区吴忠市2019届高三上学期期末考试化学试题



